ВВЕДЕНИЕ
Оказание качественной междисциплинарной медицинской помощи мультиморбидным пациентам – одно из приоритетных направлений современного здравоохранения, особенно на уровне первичного звена. Подбор адекватной, эффективной, основанной на доказательствах медикаментозной терапии и постоянный ее контроль должны осуществляться индивидуально с учетом пола, возраста пациента и сопутствующей патологии, поскольку мультиморбидность ассоциирована с неблагоприятным исходом ведущего заболевания.
Одной из основных причин инвалидизации и смертности лиц пожилого и старческого возраста являются заболевания, ассоциированные с тромбозами как артериального (острое нарушение мозгового кровообращения, инфаркт миокарда), так и венозного происхождения (тромбоз глубоких вен, тромбоэмболия ветвей легочной артерии), риск которых увеличивается по мере старения организма и требует назначения антитромботической терапии.
СИСТЕМА ГЕМОСТАЗА И СТАРЕЮЩИЙ ОРГАНИЗМ
По мере старения организма в системе гемостаза наблюдаются существенные изменения в виде повышения содержания прокоагулянтных факторов (фибриногена, факторов VII, VIII) и ингибиторов фибринолиза (ингибитора активатора плазминогена-1, ингибитора фибринолиза), что увеличивает тромбогенный потенциал плазмы крови и снижает фибринолитическую активность.
Оксидативный стресс, который нарастает с возрастом, наличие хронического провоспалительного состояния на фоне мультиморбидности, изменение реологических свойств крови, ригидности эритроцитов и эндотелиальная дисфункция вносят вклад в развитие ассоциированного с возрастом повышенного тромбообразования [1, 2].
Существуют и гендерные особенности в этом плане. Так, еще в 1995 г. было показано, что концентрация естественных антикоагулянтов (протеина C, антитромбина и ингибитора пути тканевого фактора) выше в группе лиц женского пола (р <0,0002), чем среди мужчин [3] (табл. 1).

ВОЗРАСТ-АССОЦИИРОВАННЫЕ ИЗМЕНЕНИЯ ОРГАНИЗМА И АНТИТРОМБОТИЧЕСКАЯ ТЕРАПИЯ
Антитромботическая терапия – важнейшая составляющая комплексной терапии пациентов с высоким риском тромбоэмболических осложнений (ТЭО). Возраст оказывает существенное влияние на фармакокинетические и фармакодинамические эффекты антитромботических препаратов. Несмотря на преимущества антитромботической фармакотерапии, категория пациентов старшего возраста чувствительна к побочным эффектам этой группы лекарственных препаратов, особенно к развитию кровотечений. Высокая уязвимость обусловлена множественными факторами, которые могут непосредственно влиять на терапевтическую эффективность (например, снижение функции почек и метаболизма в печени, изменение соотношения количества воды и жировой массы тела и др.) и быть тесно связанными с тромбообразованием (дисфункция тромбоцитов, нарушения свертывания крови, высокая ригидность эритроцитов и др.) [4].
Старение организма ассоциировано с молекулярными, структурными и функциональными изменениями в разных органах и системах организма. В результате инволютивных изменений печени (снижения внутрипеченочного кровотока, функциональной массы гепатоцитов, изменения архитектоники) снижается эффект первого прохождения лекарственного средства через печень, уменьшается активность ряда изоферментов цитохрома Р450, принимающих участие в метаболизме антитромботических препаратов [5, 6].
При старении организма изменяется строение и функция почек. Объем коркового вещества почек прогрессивно снижается с возрастом, а мозгового увеличивается до 50 лет, что приводит к снижению общего объема почек в возрасте старше 50 лет у здоровых людей. В целом разница в массе почек в 30 и 80 лет достигает около 20–25% [7]. С возрастом также уменьшается количество функционирующих нефронов, меняется их строение, замедляется почечный кровоток, снижается количество воды в организме. Эти изменения приводят к нарушению элиминации лекарственных средств, снижению объема распределения и увеличению концентрации в плазме гидрофильных лекарственных веществ [8].
Мультиморбидность, полипрагмазия и частые обострения хронических неинфекционных заболеваний нередко вызывают снижение скорости клубочковой фильтрации (СКФ), что способствует изменению фармакокинетики антитромботических препаратов с почечным путем выведения (низкомолекулярный гепарин, фондапаринукс, бивалирудин, эптифибатид, дабигатрана этексилат). Подобные изменения индивидуальны и весьма вариабельны.
Снижение мышечной массы и увеличение жировой ткани в организме способствуют увеличению объема распределения и периода полувыведения жирорастворимых лекарственных препаратов [9].
Замедление висцерального кровотока, опорожнения желудка, снижение моторики желудочно-кишечного тракта и незначительное увеличение рН желудка приводят к изменению биодоступности/растворимости рН-чувствительных лекарств [10].
В старшем возрасте увеличивается вероятность развития и прогрессирования многих заболеваний, включая артериальную гипертензию, ишемическую болезнь сердца (ИБС), сердечную недостаточность, ожирение, сахарный диабет, хроническую болезнь почек и другое, а также гериатрических синдромов и ассоциированных с ними последствий [11], влияющих на эффективность и безопасность антитромботической терапии.
Кроме того, генетические особенности пациентов определяют их индивидуальную чувствительность к пероральным антикоагулянтам, активное изучение которых на фармакокинетические параметры проводится в наши дни [12, 13].
ПРОФИЛАКТИКА ТРОМБОЭМБОЛИЧЕСКИХ ОСЛОЖНЕНИЙ
На сегодняшний день исследовательским «золотым стандартом» считаются рандомизированные контролируемые исследования (РКИ) как наиболее надежный инструмент анализа и оценки воздействия терапии на клинические исходы при постоянном наблюдении за пациентами. В последние годы все больше внимания уделяется наблюдательным исследованиям, позволяющим получить достаточно быстро результат и включить в анализ большое количество больных без ограничений по их исходным характеристикам [14].
Не вызывает сомнений значение возраста как фактора риска развития инсульта при фибрилляции предсердий; так, возраст 75 лет и старше рассматривается как одна из важнейших предпосылок развития инсульта, что нашло отражение в широко применяемой шкале оценки инсульта CHA2DS2-VASc, где этому показателю присвоено 2 балла [15].
Мультиморбидность, гериатрические синдромы, в частности старческая астения (frailty), с одной стороны, повышают вероятность любых ТЭО и летального исхода при отсутствии своевременно назначенной антитромботической терапии, а с другой – ассоциируются с высокой вероятностью развития кровотечений на фоне лечения антикоагулянтов [16].
С возрастом значительно увеличивается встречаемость дегенеративно-дистрофических заболеваний суставов, риск локомоторных падений и переломов бедренной кости. Ортопедические операции чаще всего выполняются именно пациентам пожилого и старческого возраста, что определяет высокую актуальность профилактики ТЭО после таких хирургических вмешательств. В свою очередь, эндопротезирование тазобедренного и коленного суставов, операции при переломах шейки бедренной кости ассоциированы с очень высоким риском венозных тромбоэмболических осложнений [17].
При принятии решения о профилактике ТЭО с помощью антикоагулянтов следует оценить соотношение угрозы развития ТЭО без лечения и риска развития кровотечения, особенно внутричерепного, как одного из наиболее опасных осложнений антикоагулянтной терапии (он зависит не только от возраста, но и от многих других факторов) и выяснить предпочтения пациента [18].
В качестве антикоагулянтных средств с благоприятным профилем безопасности рассматриваются новые оральные антикоагулянты (НОАК). К несомненным их преимуществам относятся отсутствие необходимости лабораторного контроля показателей гемостаза и независимость эффекта действия от приема пищи, что упрощает профилактику ТЭО. Кроме того, НОАК удобны в применении в силу фиксированной дозировки, имеют минимальные нежелательные лекарственные и пищевые взаимодействия. Явное преимущество НОАК над антагонистами витамина K – почечный путь элиминации [19, 20].
Результаты целенаправленных исследований свидетельствуют о том, что пожилой и старческий возраст не являются абсолютным противопоказанием к проведению пероральной антикоагулянтной терапии, включая и пациентов с хрупкостью, нарушенной функцией почек и другими коморбидными состояниями. В целом абсолютные противопоказания к применению антитромботической терапии редко встречаются в пожилом возрасте, а польза от лечения пероральными антикоагулянтами с возрастом существенно повышается.
НАСКОЛЬКО БЕЗОПАСНО НАЗНАЧАТЬ ОРАЛЬНЫЕ АНТИКОАГУЛЯНТЫ ПОЖИЛЫМ МУЛЬТИМОРБИДНЫМ ПАЦИЕНТАМ?
В отличие от антагонистов витамина К, которые блокируют образование нескольких факторов свертывания крови (факторы II, VII, IX, X), НОАК влияют на активность одного этапа коагуляции. В частности, ривароксабан ингибирует Xа-фактор свертывания крови, который принимает участие в образовании протромбиназы за счет комплекса с фактором Vа, кальцием и тромбоцитарным фосфолипидом для преобразования протромбина в тромбин. Особенность действия ривароксабана – уменьшение образования тромбина за счет блокирования именно активности фактора Xа, а не подавления непосредственно тромбина. Такой механизм действия с большей эффективностью предотвращает фибринообразование, чем инактивация тромбина, поскольку одна молекула фактора Xа вызывает синтез около 1000 молекул этого фермента [21, 22].
В международном двойном слепом РКИ ROCKET AF с участием 14 264 пациентов с неклапанной фибрилляцией предсердий из 1178 центров 45 стран мира эффект от приема ривароксабана в дозе 20 мг/ сут (или 15 мг/сут при клиренсе креатинина 30–49 мл/мин) и варфарина в подобранной по международному нормализованному отношению (МНО) дозе был сопоставим по риску возникновения больших кровотечений. Так, в группе ривароксабана этот показатель составил 14,9%, в группе варфарина – 14,5% пациентов в год (отношение шансов (ОШ) 1,03; 95% доверительный интервал (ДИ): 0,96–1,11; р=0,44). Помимо этого, при приеме ривароксабана по сравнению с варфарином наблюдалось статистически значимо меньшее количество случаев внутричерепных (0,5 против 0,7%; р=0,02) и фатальных кровотечений (0,2 против 0,5%; р=0,003) [23]. Оценивая клиническую характеристику пациентов, включенных в исследование ROCKET-AF, следует отметить, что это были мультиморбидные больные пожилого возраста (медиана возраста 73 года, интерквартильный размах 65–78 лет, 39,7% лица женского пола) с наличием сердечно-сосудистых осложнений в виде инсульта и транзиторной ишемической атаки (54% участников), сердечной недостаточности (62%), сахарного диабета (40%); они имели высокий риск инсульта в будущем (3,5 балла по шкале CHADS2) и кровотечений (у 62% пациентов более 3 баллов по шкале HAS-BLED).
Результаты другого международного проспективного рандомизированного двойного слепого исследования – COMPASS, в которое вошли 27 395 пациентов в возрасте 18 лет и старше из 602 центров 33 стран мира, подтвердили эффективность ривароксабана как средства вторичной профилактики сердечно-сосудистых осложнений у пациентов с ИБС и атеросклеротическим поражением периферических артерий [24]. Средний возраст участников исследования составил 68,2 года, 22% были лицами женского пола. ИБС в анамнезе имелась у 90,6%. Среднее систолическое артериальное давление (АД) соответствовало 136 мм рт.ст., диастолическое АД – 78 мм рт.ст., а средний уровень общего холестерина составил 4,2 ммоль/л. Липидоснижающую терапию получали 89,8% пациентов, блокаторы ренин-ангиотензин-альдостероновой системы – 71,2%. Комбинация ривароксабана в дозе 2,5 мг 2 раза/сут и АСК 100 мг 1 раз/сут способствовала статистически значимому снижению риска развития инсульта (на 42%) и сердечно-сосудистой смерти (на 22%), включая статистически незначимое снижение риска развития инфаркта миокарда (на 14%) [25].
Результаты этого исследования в 2018 г. легли в основу решения Европейской комиссии об одобрении применения ривароксабана (Ксарелто®, производство Bayer, изучение эффектов препарата совместно с Janssen Research & Development) в дозе 2,5 мг 2 раза/сут в сочетании с АСК (по 75–100 мг 1 раз/сут) для профилактики атеротромботических событий у взрослых пациентов с ИБС или с клинически выраженным заболеванием периферических артерий, имеющих высокий риск развития ишемических осложнений [26].
В настоящее время показания для назначения ривароксабана включают профилактику венозной тромбоэмболии у лиц, перенесших крупные оперативные вмешательства на опорно-двигательном аппарате; профилактику кардиоэмболического инсульта и системной тромбоэмболии при неклапанной фибрилляции предсердий; терапию и профилактику рецидивов тромбоза глубоких вен (ТГВ) и тромбоэмболии легочной артерии (ТЭЛА); профилактику летального исхода вследствие сердечно-сосудистых причин, инфаркта миокарда и тромбоза стента после острого коронарного синдрома, протекающего с повышением концентрации кардиоспецифических биомаркеров (в комбинированной терапии с АСК); профилактику инсульта, инфаркта миокарда и смерти вследствие сердечно-сосудистых причин; профилактику острой ишемии конечностей и общей смертности у пациентов с ИБС или заболеваниями периферических артерий [27–31].
Ривароксабан первым среди НОАК получил одобрение к применению у пациентов с венозными тромбоэмболиями с первого же дня лечения. Возможность применения препарата по 20 мг 1 раз/сут для длительной профилактической терапии после перенесенной ТЭЛА повышает приверженность пациентов к лечению и улучшает профилактику повторных венозных тромбоэмболий [32].
Объединенный анализ четырех исследований RECORD с участием 12 729 пациентов в возрасте 18 лет и старше, которым было проведено эндопротезирование тазобедренного и коленного суставов, показал преимущество ривароксабана в дозе 10 мг 1 раз/сут над эноксапарином натрия в дозе 40 мг 1 раз/сут или 30 мг каждые 12 ч подкожно (p=0,001) [33] в отношении предупреждения развития эпизодов венозных ТЭО и летального исхода от любых причин. Ценность этого исследования заключается в дополнительном анализе эффективности ривароксабана у лиц пожилого возраста и подтверждении эффективности дозы ривароксабана 10 мг/сут, рекомендуемой для профилактики венозных ТЭО после ортопедических операций и не требующей коррекции в зависимости от возраста и функции почек.
В соответствии с согласованным мнением экспертов Российской ассоциации геронтологов и гериатров и Национального общества профилактической кардиологии для профилактики венозных ТЭО рекомендуется первый прием ривароксабана через 6–10 ч после операции. При оперативном вмешательстве на коленном суставе рекомендовано применение препарата в течение 2 нед (при высоком риске тромбоза его продлевают до 5 нед), на тазобедренном суставе – 5 нед [10].
При выборе конкретного препарата всегда следует учитывать его фармакокинетические особенности. Ривароксабан не рекомендован к применению у пациентов при клиренсе креатинина <15 мл/ мин. Если этот показатель находится в пределах 15–49 мл/мин, то следует снизить дозу ривароксабана с 20 до 15 мг однократно из-за возможности увеличения концентрации препарата в кровотоке в 1,5–1,6 раза [34].
Преимуществом препарата является отсутствие необходимости корректировать дозу в зависимости от возраста. Кроме того, пол человека и масса тела не влияют на фармакокинетику ривароксабана [35].
При приеме ривароксабана межлекарственные взаимодействия практически отсутствуют. Такие препараты, как АСК, варфарин, клопидогрел, варфарин, дигоксин, аторвастатин, не влияют на фармакокинетику ривароксабана, что позволяет использовать их совместно. Поскольку ривароксабан метаболизируется через CYP3A4, следует помнить, что ингибиторы CYP3A4 и P-gp/BCRP (кетоконозал и ритонавир) увеличивают его концентрацию и могут приводить к развитию кровотечений. Эритромицин, кларитромицин и флуконазол практически не влияют на концентрацию ривароксабана, однако назначение индукторов CYP3A4 и P-gp/BCRPр требует осторожности из-за риска снижения эффективности ривароксабана [36, 37].
В качестве иллюстрации возможности применения этого НОАК в реальной медицинской практике приводим наше клинической наблюдение.
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Пациентка И., 69 лет, индекс массы тела (ИМТ) 22,3 кг/м2, наблюдается у врача-терапевта поликлиники с октября 2020 г. со следующим диагнозом: «ИБС: постинфарктный кардиосклероз. Стенокардия напряжения II функционального класса (ФК). Гипертоническая болезнь III стадии. Контролируемая артериальная гипертензия. Риск 4 (очень высокий). Целевой уровень артериального давления (АД) менее 130/80 мм рт.ст. Хроническая болезнь почек III Б стадии. Первичный остеопороз бедра (минеральная плотность кости (МПК) 0,655 г/см2; Т-критерий: -2,8), остеопения позвоночника (минеральная плотность кости 0,907 г/см2; Т-критерий: -2,3). Патологический перелом шейки левой бедренной кости. Хронический гастрит, вне обострения. Недостаточность витамина D».
В марте 2020 г., находясь дома, пациентка упала с высоты собственного роста. Произошел перелом шейки левой бедренной кости. Госпитализирована в травматологическое отделение, где ей было выполнено тотальное эндопротезирование левого тазобедренного сустава. Длительность госпитализации составила 15 дней. Выписана с улучшением, передвигалась с помощью ходунков. В дальнейшем, после 10 дней пребывания в домашних условиях, госпитализирована в реабилитационный центр для продолжения лечения, где находилась 21 день.
В период госпитализации по поводу травмы в марте 2020 г. пациентка получала нестероидные противовоспалительные препараты и ривароксабан в дозе 10 мг для профилактики венозной тромбоэмболии в связи с иммобилизацией и эндопротезированием тазобедренного сустава. Выбор ривароксабана в качестве антикоагулянта был продиктован наличием перенесенного инфаркта миокарда.

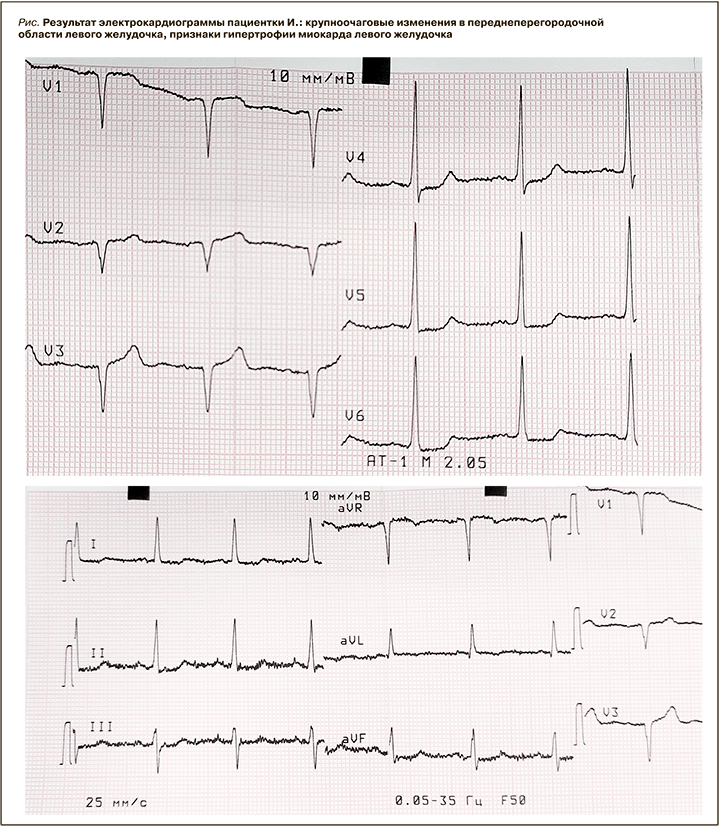
Результаты клинического и биохимического анализов крови представлены в таблицах 2, 3 и 4.

Данные электрокардиограммы (ЭКГ): ритм синусовый с частотой сердечных сокращений (ЧСС) 76 уд./мин, крупноочаговые изменения миокарда переднеперегородочной области левого желудочка. Горизонтальная электрическая ось сердца (рис. 1).
Данные двухфотонной рентгеновской абсорбциометрии: остеопороз с поражением шейки бедра (МПК 0,655 г/см2; Т-критерий: -2,8) и остеопения поясничного отдела позвоночника (МПК 0,907 г/ см2; Т-критерий: -2,3).
После выписки из стационара под наблюдение врача-терапевта по месту жительства пациентка в составе комплексной терапии (ингибитор АПФ, бета-адреноблокатор, статин) продолжала прием ривароксабана по 10 мг в сочетании с АСК по 100 мг. В настоящее время также принимает эти препараты в указанных дозах. На фоне приема ривароксабана не отмечалось побочных эффектов, переносимость терапии хорошая. Терапевт проводит регулярный контроль функции почек и печени пациентки, отклонений от нормы в результатах лабораторных исследований не наблюдается.
ЗАКЛЮЧЕНИЕ
Выбор рациональной антитромботической терапии для пациента старшего возраста с учетом сопутствующей патологии и полипрагмазии является сложной задачей. Это обусловлено небольшим количеством специальных исследований с участием лиц пожилого и старческого возраста, а также ограниченностью соответствующих данных во многих крупномасштабных РКИ.
Немаловажную роль в лечении мультиморбидного пациента старшего возраста играет врач амбулаторного звена, главные задачи которого – своевременная верификация диагноза, долговременное ведение больного, регулярная оценка функции печени и почек, постоянная переоценка риска кровотечений. Данный факт нельзя недооценивать, поскольку это важный первый шаг к выбору тактики лечения пациента в составе мультидисциплинарной команды в рутинной клинической практике.
Лица, перенесшие низкоэнергетические переломы, имеют высокий риск повторных переломов. В связи с этим важна их медикаментозная и немедикаментозная профилактика, в рамках которой антитромботической терапии, в частности ривароксабану, отводится немаловажное место. Это обусловлено тем, что с возрастом риск тромбоза превалирует над риском кровотечения и коэффициент «польза/риск» антикоагуляции в целом остается положительным.
Пероральная форма ривароксабана, отсутствие необходимости лабораторного мониторинга гемостаза, низкая частота геморрагических осложнений позволяют рассматривать этот НОАК в качестве препарата выбора у амбулаторных пациентов для профилактики ТЭО.
С целью внедрения в систему здравоохранения России систематического подхода к лечению остеопоротических переломов для восстановления функции и предотвращения повторных переломов костей скелета профессиональными медицинскими ассоциациями (Российской ассоциацией по остеопорозу, Российской ассоциацией геронтологов и гериатров, АО «Травма Россия» и Союзом реабилитологов России), а также обществом пациентов ОСТЕОРУС предложен «ортогериатрический подход». Миссия этого подхода заключается в содействии продвижению в системе здравоохранения нашей страны мультидисциплинарного ведения пожилого пациента с переломом, включая его вторичную профилактику [38].



