Нарушение венозного кровообращения головного мозга можно назвать «Золушкой» в церебральной сосудистой патологии. Ее игнорируют клиницисты из-за трудности верификации и не любят исследователи из-за сложности методических подходов к ее изучению. Вместе с тем венозный отдел составляет 85% церебрального сосудистого русла [1]. Причину недостаточной изученности венозной патологии головного мозга можно объяснить значительной ее вариабельностью и отсутствием до недавнего времени объективных методов диагностики.
Венозная дисциркуляция может сопровождать артериальную хроническую ишемию мозга, и недоучет этого фактора способствует неэффективности лечения больных. У 71,5% больных с артериальной гипертензией (АГ) методом УЗИ обнаружена компрессия внутренних яремных, брахиоцефальных, позвоночных вен, у многих больных – гипотония вен, недостаточность клапанов в устьях вен и аномалии их строения [2]. По данным МР-венографии у больных с тяжелой и злокачественной АГ признаки нарушения венозного оттока головного мозга встречаются в 91% случаев, а у больных с АГ 1–2-й стадии – в 55% случаев [3].
Роль венозной системы в кровоснабжении мозга очень значима, и поэтому практикующему интернисту нужно знать особенности ее строения, функционирования, патологических изменений и способов коррекции соответствующих нарушений.
В классификации МКБ-10 отражены острые формы церебральных венозных нарушений. Вместе с тем, по данным различных авторов, хроническая венозная дисциркуляция головного мозга является одной из самых распространенных форм цереброваскулярной патологии [4–7].
Большой вклад в изучение венозного компонента хронической недостаточности мозгового кровообращения сделан отечественными неврологами [8–10]. Подчеркивается, что зачастую венозные церебральные расстройства компенсированы, они могут сочетаться с другой патологией, что приводит к стертости клинической картины и трудностям их своевременного выявления [11]. По мнению ряда авторов, церебральные венозные дистонии встречаются намного чаще, чем диагностируются. Актуальность изучения венозной патологии головного мозга определяется не только ее высокой распространенностью (более 80% пациентов с АГ и атеросклеротическим поражением сосудов головного мозга имеют признаки нарушения венозного оттока), но и отсутствием четких критериев диагностики и недостаточной разработанностью терапевтических подходов [12, 13].
В единой морфофункциональной сосудистой системе головного мозга различают 5 уровней:
- магистральные артерии головы;
- интрацеребральные артерии;
- сосуды микроциркуляторного русла;
- внутричерепную венозную систему (венулы, малые вены, венозные сплетения, синусы);
- внечерепные яремные, позвоночные вены, шейные венозные сплетения, верхнюю полую вену.
В венозной системе головного мозга выделяют несколько уровней: поверхностные и глубокие вены, синусы твердой мозговой оболочки, вены – выпускники и сплетения основания черепа.
Вены основания мозга образуют базальный венозный круг, аналогичный виллизиеву. Они дренируют кровь, в основном в базальные вены Розенталя, и считаются частью глубокой дренажной системы.
В венах, обеспечивающих венозный отток от мозговой ткани, нет клапанов, но между ними отмечается очень большое количество анастомозов. Отсутствие жесткого каркаса в церебральных венах приводит к тому, что при отеке мозговой ткани и увеличении внешнего давления на стенки вен они сдавливаются, и возникает нарушение венозной циркуляции крови.
Синусы твердой мозговой оболочки, образованные листками твердой мозговой оболочки, являются коллекторами для венозной крови мозга и его оболочек. В синусы впадают вены мозга и диплоические вены черепа.
Из синусов кровь поступает во внутренние яремные вены, которые выступают в качестве магистрального пути венозного оттока от головного мозга. Существуют также экстраюгулярные пути венозного оттока в интраспинальные и продольные венозные сплетения, расположенные на наружной поверхности тел позвонков, и глубокие вены шеи. В норме у лежащего человека основной объем венозной крови от головы оттекает по яремным венам, позвоночные вены расцениваются как «запасной клапан». При переходе в вертикальное положение отток крови происходит как во внутреннюю яремную вену, так и в позвоночное венозное сплетение и позвоночные вены. Помимо этого, имеется связь синусов с венами наружной поверхности черепа посредством эмиссариев – резервных венозных выпускников, расположенных внутри плоских костей черепа (рис. 1).
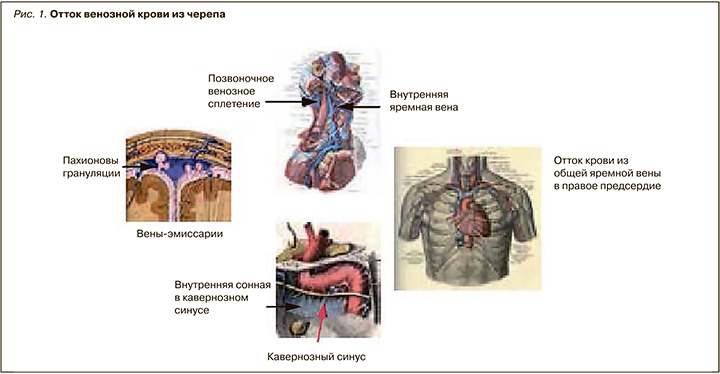
Внутреннюю сонную артерию, расположенную в кавернозном синусе, образно называют «венозное сердце мозга», поскольку ее сильная пульсация передается на твердую мозговую оболочку, что заставляет головной мозг пульсировать (см. рис. 1). Поэтому головной мозг является «пульсирующим органом», и колебания внутричерепного давления осуществляются в такт пульсации артерии.
Церебральное венозное давление зависит от внечерепных причин, и поэтому легочно-сердечная недостаточность, хроническая обструктивная болезнь легких, опухоли средостения и сдавления внечерепных вен в области шеи и верхней апертуры грудной клетки могут ухудшать венозную циркуляцию внутри черепа.
Венозная система головного мозга служит не только для оттока венозной крови, но и для всасывания ликвора. Резорбция ликвора осуществляется через пахионовы грануляции в венозные синусы головного мозга (см. рис. 1).
ПРИЧИНЫ И ФОРМЫ ВЕНОЗНОЙ ЭНЦЕФАЛОПАТИИ
Объем венозной крови – одна из величин, составляющих внутричерепное давление. Это объясняет характер жалоб, предъявляемых больными с венозной энцефалопатией (ВЭ), которые по своей сути являются гипертензионными, т.е. связанными с повышением внутричерепного давления. Различные причины, затрудняющие отток венозной крови из полости черепа, приводят к переполнению сосудистого русла головного мозга кровью и повышению внутричерепного венозного давления. И, в свою очередь, повышение внутричерепного давления вследствие различных причин сопровождается повышением церебрального венозного давления. К таким причинам относятся:
- острый гипертензивный срыв ауторегуляции мозгового кровотока, при котором среднее артериальное давление (АД) поднимается выше 150 мм. рт.ст. (острая гипертоническая энцефалопатия, тяжелые инсульты);
- «масс-эффект» при появлении дополнительного объема в паренхиме мозга (отек, опухоль, кровоизлияние и др.);
- хроническая артериальная гиперемия при стойкой АГ и недостаточности регуляторных механизмов поддержания постоянства церебрального перфузионного давления;
- повышение давления цереброспинальной жидкости при гиперсекреторной гидроцефалии.
У пациентов с гипертонической энцефалопатией отмечается расширение нижней луковицы внутренней яремной вены, что можно рассматривать как необратимые нарушения венозной циркуляции, возникающие вследствие повышенной нагрузки объемов при артериальной гипертонии [14]. При повышении давления в синусах мозга (венозный застой) рефлекторно суживаются магистральные артерии, что может приводить к системному повышению АД.
Хронические формы нарушения венозного кровообращения мозга могут вызываться как системными (нарушения центральных механизмов оттока, системная флебогипертензия), так и регионарными причинами, которые подразделяются на интракраниальные и экстракраниальные [15].
Системная церебральная венозная дистония (венозный застой) является наиболее частой хронической формой расстройств венозного мозгового кровообращения [10]. В формировании внутричерепного венозного застоя участвуют дистония и гипотония вен мозга, сопровождающееся различными патологическими процессами в виде церебральной венозной дистонии, уменьшении просвета вен с дальнейшим развитием церебральных венозных дистонических дизрегуляторных и застойно-гипоксических нарушений [7]. Предрасполагающими факторами венозной церебральной дистонии выступают АГ или артериальная гипотензия, особенно в случаях недостаточности церебральной ауторегуляции сосудистого тонуса. Часто у больных одновременно выявляются признаки системной венозной недостаточности (варикозное расширение вен нижних конечностей, геморрой, варикоцеле), возможно ее наследование. Венозная дистония мозга может быть одним из признаков недифференцированной дисплазии соединительной ткани.
Наряду с системной флебогипертензией интракраниальными причинами могут быть последствия перенесенных травм черепа, арахноидитов, тромбозов вен и синусов твердой мозговой оболочки, опухоли головного мозга, сдавление внутричерепных вен при водянке мозга и краниостенозе и др. Интракраниальная патология может вызывать «манжеточное» сдавление мостиковых вен с затруднением оттока от поверхностных вен и компенсаторной активизацией оттока по глубоким венам мозга [16].
Экстракраниальная (брахиоцефальная) патология может быть связана с аномалиями строения брахиоцефальных вен, сдавлением внечерепных вен в области шеи и верхней апертуры грудной клетки (компрессия спазмированными мышцами, дистопированными костными и связочными структурами при травме, опухолью и другие патологическими процессами в средостении, гиперплазированной щитовидной железой, аневризмой аорты, спазмированными мышцами). Она может быть следствием сердечной (ишемическая болезнь сердца, кардиомиопатии, аритмии и т.д.) или легочно-сердечной недостаточности (хроническая обструктивная болезнь легких, пневмонии и т.д.).
Патология брахиоцефальных вен может быть врожденной (аномалии строения или их размера в виде гипоплазии, аневризмы, аномальное взаиморасположение артерий и вен с компрессией последних) или приобретенной (компрессии, тромбозы, вторичная недостаточность клапанов) [17].
Нарушения венозного оттока в вертебробазилярной системе чаще всего обусловлены дегенеративно-дистрофическими изменениями на уровне шейного отдела позвоночника. Это связано с тем, что большая часть экстракраниального отдела позвоночной артерии в сопровождении вегетативного сплетения и позвоночных вен проходит в подвижном узком костном канале, образованном отверстиями в поперечных отростках шейных позвонков. Поэтому даже незначительные разрастания крючковидных отростков могут травмировать сосудисто-нервный пучок, непосредственно сдавливая или раздражая симпатическое сплетение. На сосудисто-нервный пучок могут оказывать влияние межпозвонковые диски, передняя и задняя продольные связки. Основными процессами, определяющими эту патологию, являются остеохондроз, деформирующий спондилез, деформирующий спондилоартроз, первичный деформирующий остеоартроз позвоночника и оссифицирующий лигаментоз позвоночника (фиксирующий лигаментоз, болезнь Форестье). При дегенеративных изменениях на уровне шейного отдела позвоночника наиболее частыми непосредственными причинами патологического воздействия на позвоночные артерии и вены являются унковертебральный артроз, а также патологическая подвижность в позвоночном сегменте. Мышечно-тонические расстройства на уровне шейного отдела позвоночника оказывают рефлекторные и непосредственные физические влияния на экстракраниальные вены и являются одной из возможных причин формирования церебральной венозной дисциркуляции. Это обусловлено компрессией позвоночной артерии в результате тонического сокращения нижней косой мышцы головы и передней лестничной мышцы.
На рисунке 2 показаны основные причины вертеброгенного нарушения венозного оттока из черепа.
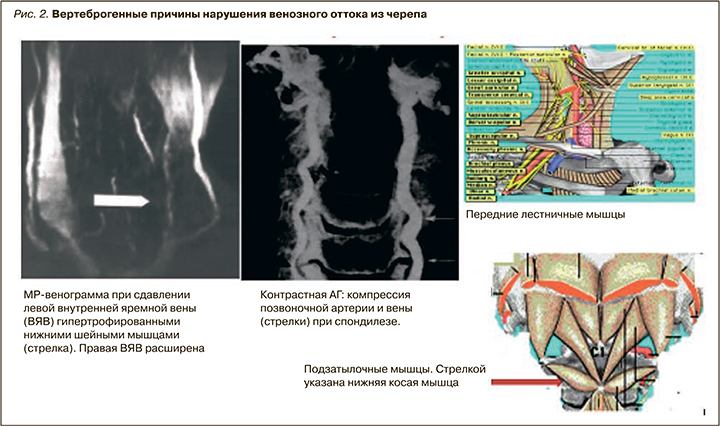
Во многих исследованиях показана высокая степень зависимости хронической ишемии мозга (ХИМ) от венозного застоя [7, 18]. Как известно, ведущими этиологическими факторами ХИМ являются церебральный артериосклероз и гипертоническая болезнь. Атеросклеротическое поражение магистральных артерий и головы и крупных интракраниальных артерий сопровождается окклюзиями, стенозами и атеротромбозами. При гипертонической болезни излюбленной локализацией поражения являются зона терминального кровообращения на уровне терминальных артерий и артериол. При нарушениях кровообращения в артериях мозга в той или иной степени страдает венозный отток; равным образом патология вен мозга приводит к нарушению артериальной гемодинамики и метаболизма мозга.
Венозные дисгемии, в свою очередь, играют важную роль в патогенезе ХИМ, так как функциональная венозная дистония рефлекторно вызывает сужение интрацеребральных артерий, уменьшая приток крови к мозгу [10, 19]. Эти два процесса тесно взаимосвязаны. Гипертензия в венозном колене капиллярной системы затрудняет кровоток в ее артериальном секторе. Это способствует открытию артериоловенулярных анастомозов, в связи с чем поступление крови в венозное русло осуществляется по более короткому пути. Юкстакапиллярный кровоток приводит к артериализации венозной крови и гипоксии тканей. Прогрессирование церебральной венозной дистонии приводит к значительным изменениям мозгового метаболизма, гипоксии и ишемии. Для уменьшения венозного застоя дополнительные пути оттока по глубокой венозной системе начинают работать с перегрузкой [12].
При затруднении венозного оттока наблюдается вторичное повышение ликворного давления. Основной ток жидкости происходит под влиянием положительного градиента гидростатического давления между спинномозговой жидкостью и венозной кровью, причем арахноидальные ворсины действуют наподобие клапанов, позволяющих жидкости продвигаться из ликворного пространства в кровь, но не в обратном направлении. Таким образом, венозно-артериальный дисбаланс может приводить к венозно-ликворному дисбалансу со вторичным повышением ликворного давления. Суммарно это проявляется в повышении внутричерепного давления [15].
При гипоксии мозга, независимо от вызвавших ее причин, как в случаях острой, так и хронической патологии развивается ишемический каскад, заключающийся в связанных между собой патологических реакциях. Основными звеньями патогенеза ВЭ вследствие гипоксии являются нарушение церебральной микрогемоциркуляции, неадекватность энергетических ресурсов для обеспечения функционирования мозга, глутаматный эксайтоксикоз. Избыточная активация глутуматэргических рецепторов приводит к массивному поступлению в нейроны ионов кальция и натрия, деполяризации клеточных мембран, активации вольтаж-зависимых кальциевых каналов и внутриклеточному накоплению кальция, в результате чего происходит каскад неблагоприятных патобиохимических процессов с лактатацидозом, активацией внутриклеточных ферментов, повышением синтеза оксида азота и развитием окислительного стресса [12].
Избыточное свободно-радикальное окисление – универсальный патофизиологический феномен при многих патологических состояниях в неврологии [20]. Кислород для любой клетки, особенно нейрона, является ведущим энергоакцептором в дыхательной митохондриальной цепи. Связываясь с атомом железа цитохромоксидазы, молекула кислорода подвергается четырехэлектронному восстановлению и превращается в воду. Но в условиях нарушения энергообразующих процессов при неполном восстановлении кислорода происходит образование высокореактивных, а потому токсичных свободных радикалов или продуктов, их генерирующих. Эти вещества вызывают повреждение фосфолипидов клеточных мембран.
Важную роль в инициации и прогрессировании венозной энцефалопатии играет микроциркуляторный блок, составными компонентами которого являются гемореологические изменения крови, связанные с повышением гематокрита, вязкости, фибриногена, агрегации и адгезии тромбоцитов, агрегации эритроцитов, адгезии лейкоцитов и др. [21]. При этом особое патогенетическое значение с учетом неблагоприятного соотношения диаметров капилляров и эритроцитов имеют изменения морфофункционального состояния эритроцитов. Улучшение вязкостно-эластичных свойств эритроцитов благоприятствует транспорту кислорода через эритроцитарную мембрану, а их нарушение коррелирует с ухудшением оксигенации тканей. Напротив, ухудшение деформируемости эритроцитов обусловливает развитие застойных явлений в микроциркуляторном русле и, как следствие, возникновение тканевой гипоксии [22–24].
КЛИНИЧЕСКИЕ ОСОБЕННОСТИ ВЕНОЗНОЙ ЭНЦЕФАЛОПАТИИ
Многие больные с хроническим венозным застоем не предъявляют жалоб, которые можно было бы объяснить поражением мозга. Это связано с высокой устойчивостью их нервной системы к изменениям кровообращения и нарушению газообмена. Компенсаторные возможности головного мозга и его системы кровообращения так велики, что даже серьезные затруднения оттока венозной крови могут длительное время не вызывать клинических проявлений повышения внутричерепного давления и нарушения мозговых функций. Развитие симптомов болезни свидетельствует о нарушении приспособления мозга к условиям затрудненного кровообращения и недостаточности физиологических мер защиты, направленных на преодоление венозного застоя в мозге.
В клинических проявлениях заболевания характер жалоб занимает одно из первых мест. В литературе, посвященной изучению венозной патологии головного мозга, описаны так называемые венозные жалобы. К ним, помимо характерной утренней или ночной головной боли, относят усиление головной боли, головокружения, шума в голове, зрительных расстройств при ношении тугих воротников или галстуков (симптом «тугого воротника»), во время сна с низким изголовьем (симптом «высокой подушки»), ощущение «засыпанности глаз песком» в утренние часы (симптом «песка в глазах»), пастозность лица и век в утренние часы. Для описания этого клинического синдрома с появлением или усилением жалоб в ночные или утренние часы («как только открыл глаза после сна») предложен термин «энцефалопатия пробуждения» [25].
Наиболее частое клиническое проявление ВЭ – головная боль, которая имеет ряд характерных черт, позволяющих выделить ее среди других видов головной боли (табл).

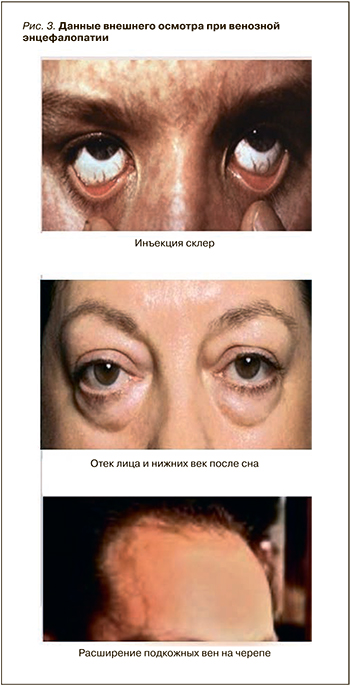 При внешнем осмотре обращает на себя внимание инъекция склер, цианотичная окраска кожи всего лица, локальный цианоз губ, синева под глазами, легкая синюшность шеи, кончика носа, мочек ушей, мягкого нёба, выраженная отечность лица и век в утренние часы после ночного сна, которая значительно уменьшается к вечеру при достаточной физической активности, расширение подкожных вен на черепе (рис. 3). Эти симптомы объясняются сопутствующим нарушением венозного оттока в системе наружной яремной вены, а также расширением подкожных вен в области черепа вследствие компенсаторного функционирования вен-эмиссариев при повышении внутричерепного венозного давления (ВЧД).
При внешнем осмотре обращает на себя внимание инъекция склер, цианотичная окраска кожи всего лица, локальный цианоз губ, синева под глазами, легкая синюшность шеи, кончика носа, мочек ушей, мягкого нёба, выраженная отечность лица и век в утренние часы после ночного сна, которая значительно уменьшается к вечеру при достаточной физической активности, расширение подкожных вен на черепе (рис. 3). Эти симптомы объясняются сопутствующим нарушением венозного оттока в системе наружной яремной вены, а также расширением подкожных вен в области черепа вследствие компенсаторного функционирования вен-эмиссариев при повышении внутричерепного венозного давления (ВЧД).
Неврологические очаговые симптомы при ВЭ непостоянны и выявляются при достаточно выраженной венозной дисгемии. Характерны при этом признаки мелкоочагового рассеянного поражения мозга. К ним относятся непостоянный нистагм, недостаточность конвергенции глазных яблок, снижение корнеальных рефлексов. В рамках «синдрома поперечного синуса» описана болезненность в точках выхода Ι, реже ΙΙ ветвей тройничного нерва с формированием гипестезии в зоне иннервации первой ветви тройничного нерва, что обусловлено нейропатией, вызванной венозным застоем и нарушением микроциркуляции в системе vaza nervorum этой ветви. Типична диссоциация коленных и ахилловых рефлексов, вероятно, связанная с отеком спинальных корешков и периферических нервов и развитием нисходящих тормозных влияний ретикулярной формации ствола мозга при венозном застое в мозге.
Одним из наиболее часто встречающихся синдромов при ВЭ является астенический синдром. В этих случаях больные предъявляют жалобы на нарушения сна, раздражительность, слезливость, снижение памяти и внимания, трудность усвоения информации, потребность в дополнительном отдыхе, не приносящем облегчения, сексуальные расстройства.
При тяжелой ВЭ может развиваться псевдотуморозный синдром, который характеризуется клиническими признаками ВЧД в отсутствие очаговых неврологических симптомов, наличием застойных дисков зрительного нерва. Однако при тяжелой форме ВЭ встречаются и более грубые нарушения: когнитивные, двигательные, чувствительные, координаторные и др. Например, может развиться паркинсоноподобный синдром с общей скованностью, замедленностью движений, повышением мышечного тонуса, дрожанием головы, рук и ног.
Возможны хронический, эпизодический и ремиттирующий варианты течения ВЭ. Имеют значение конституциональный и наследственный факторы в формировании венозных дисгемий. У пациентов с семейным «венозным» анамнезом обычно отмечается несколько типичных локализаций венозной патологии — варикозное расширение вен и флеботромбоз нижних конечностей, геморрой, варикоцеле, варикозное расширение вен пищевода, нарушение венозного оттока из полости черепа.
 Диагнозу помогают часто обнаруживаемые у больных с ВЭ признаки недифференцированной дисплазии соединительной ткани: скелетные изменения (астеническое телосложение, непропорционально длинные конечности, арахнодактилия, различные виды деформации грудной клетки, сколиозы, кифозы и лордозы позвоночника, синдром «прямой спины», плоскостопие); изменения со стороны кожи (гиперэластичность, истончение); поражение сосудов (аневризматические расширения артерий среднего и мелкого калибра, варикозное расширение вен нижних конечностей); бронхолегочные поражения, касающиеся как бронхиального дерева, так и альвеол (бронхоэктазы, простая и кистозная гипоплазия, буллезная эмфизема и спонтанный пневмоторакс); патология почек (нефроптоз и реноваскулярные изменения).
Диагнозу помогают часто обнаруживаемые у больных с ВЭ признаки недифференцированной дисплазии соединительной ткани: скелетные изменения (астеническое телосложение, непропорционально длинные конечности, арахнодактилия, различные виды деформации грудной клетки, сколиозы, кифозы и лордозы позвоночника, синдром «прямой спины», плоскостопие); изменения со стороны кожи (гиперэластичность, истончение); поражение сосудов (аневризматические расширения артерий среднего и мелкого калибра, варикозное расширение вен нижних конечностей); бронхолегочные поражения, касающиеся как бронхиального дерева, так и альвеол (бронхоэктазы, простая и кистозная гипоплазия, буллезная эмфизема и спонтанный пневмоторакс); патология почек (нефроптоз и реноваскулярные изменения).
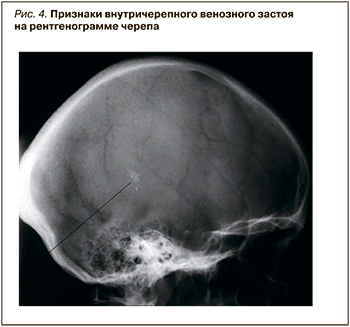
Косвенные признаки ВЭ могут проявляться на обзорной рентгенограмме черепа, при этом видны расширенные диплоические каналы, что рассматривается как признак венозно-ликворной внутричерепной гипертензии и включения в патологический процесс внутричерепных вен-эмиссариев (рис. 4).
ДИАГНОСТИКА ВЕНОЗНОЙ ЭНЦЕФАЛОПАТИИ
Для диагностики ВЭ обязательно проведение офтальмологического обследования. Как известно, центральная вена сетчатки впадает в кавернозный синус, и венозный застой в этом синусе приводит к венозной дисциркуляции в сетчатке глаза. В этих случаях развивается венозная ангиопатия сетчатки, проявляющаяся расширением вен, их извитостью и неравномерностью калибра. При более выраженных изменениях венозного кровотока вены резко расширены и извиты, «тонут в отечной ткани», при этом артерии узкие.
При клинических признаках шейной дорсопатии для уточнения характера патологического процесса проводят 5 рентгенограмм шейного отдела позвоночника: прямой и профильный, прямой через открытый рот и два функциональных снимка с максимальным разгибанием и сгибанием шеи. Особое внимание необходимо уделить функциональной оценке рентгенограмм. Неоптимальный двигательный стереотип, компенсаторные двигательные паттерны, замещение ими физиологических паттернов с последующим формированием патологических двигательных проявляются множеством рентгенологических изменений. Могут быть выявлены смещение суставных поверхностей в пределах анатомического барьера, клинически значимые функциональные дистопии костей, обусловленные суставно-капсулярными и миофасциальными дисфункциями различного генеза, а также другая патология. Важная трансоральная спондилография, которая может выявить подвывихи в сегменте С1–С2.
 Современные ультразвуковые технологии позволяют одновременно визуализировать и оценивать количественные параметры кровотока по венам и синусам головного мозга, что недоступно другим методам диагностики [26]. Поиск мозговых вен и синусов осуществляется на основании их анатомического близкого расположения по отношению к уже известным артериям, типичных характеристик венозного кровотока и его направления, а также на основании анатомических ориентиров структур головного мозга и костей черепа.
Современные ультразвуковые технологии позволяют одновременно визуализировать и оценивать количественные параметры кровотока по венам и синусам головного мозга, что недоступно другим методам диагностики [26]. Поиск мозговых вен и синусов осуществляется на основании их анатомического близкого расположения по отношению к уже известным артериям, типичных характеристик венозного кровотока и его направления, а также на основании анатомических ориентиров структур головного мозга и костей черепа.
По данным различных авторов, глубокие средние мозговые вены определяются ультразвуковыми методами в 21–88% исследований, вены Розенталя – в 88–100%, большая мозговая вена Галена – в 34–64%, прямой синус – в 50–85%, верхний сагиттальный синус – в 0–54%, поперечные синусы – 20–73%, область слияния синусов – в 17–53% случаев [27]. При венозном застое выявляется ретроградный кровоток в глазных венах вследствие повышения давления в кавернозном синусе. Увеличение линейной скорости кровотока в прямом синусе и венах Розенталя свидетельствует о недостаточности венозного оттока из полости черепа (рис. 5). Ретроградный кровоток по вене Галена может указывать на непроходимость прямого синуса.
Магнитно-резонансная венография (МРВ) брахиоцефальных вен и мозговых синусов является достаточно информативным методом выявления нарушений венозного оттока из полости черепа, а также причин обструкции вен [28]. При МРВ на мультипланарных изображениях можно визуализировать верхний сагиттальный, прямой, поперечные, сигмовидные и затылочный венозные синусы головного мозга, а также внутренние и наружные яремные вены с двух сторон, бифуркации внутренних яремных, подключичных и безымянных вен с двух сторон, обе безымянные вены, бифуркацию безымянных вен, верхнюю полую и позвоночные вены. Дренажная система головного мозга отличается большими компенсаторными возможностями благодаря механизмам перетока венозной крови в обширной сети коллатералей и шунтов.
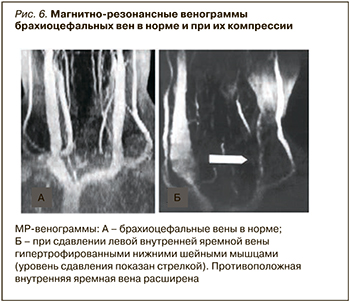 При выраженном и длительном нарушении оттока по одной из внутренних яремных вен ее диаметр уменьшается, а площадь поперечного сечения контралатеральной внутренней яремной вены увеличивается в среднем 5 раз (рис. 6).
При выраженном и длительном нарушении оттока по одной из внутренних яремных вен ее диаметр уменьшается, а площадь поперечного сечения контралатеральной внутренней яремной вены увеличивается в среднем 5 раз (рис. 6).
При гемодинамически значимом сдавлении наблюдается выраженное увеличение площади поперечного сечения, а также усиление сигнала не только контралатеральной внутренней яремной вены, но и других венозных коллекторов, появляются коллатерали и шунты между венами как проявление механизма компенсации венозного оттока из полости черепа.
При тромбозе интракраниальных венозных синусов сигнал на магнитно-резонансных венограммах в пораженных отделах синусов отсутствует. В случае одностороннего тромбоза поперечного и сигмовидного венозных синусов сигнал в их проекции отсутствует, но визуализируется гомолатеральный расширенный верхний каменистый синус, который обычно не виден. Кровоток в гомолатеральной внутренней яремной вене при этом очень низкий [29].
ВЭ как хроническая форма нарушения мозгового кровообращения не отражена в МКБ-10. Вместе с тем указание на венозное нарушение мозгового кровообращения очень важно для патогенетически обоснованного лечения больных. Компромиссным вариантом может быть использование шифра другого заболевания, синдромом которого является венозная дисциркуляция. В качестве примера можно привести гипертоническую болезнь, при которой особо при плохо контролируемой артериальной гипертензии с большим постоянством отмечаются венозные жалобы и при дополнительных исследованиях выявляются затруднения венозного оттока из полости черепа. В этих случаях можно выставить диагноз «I67.4 Гипертензивная энцефалопатия. Хроническая недостаточность венозного кровообращения головного мозга». У больных с хронической ишемией мозга могут также определяться признаки венозной недостаточности. Будет правомерным поставить диагноз «I67.8 Хроническая ишемия мозга с недостаточностью венозного кровообращения». Часто венозная дисциркуляция связана с компрессией спазмированными мышцами позвоночного венозного сплетения и других шейных вен при шейной дорсопатии. У больных наряду с миофасциальной болью может развиваться и венозная головная боль, что должно быть отражено в клиническом диагнозе, к примеру: «М47 Шейная дорсопатия. Краниоцервикалгия, шейный миофасциальный синдром. Недостаточность церебрального венозного кровообращения». Такие же примеры формулировок клинических диагнозов можно отметить при венозной дисциркуляции у больных с последствиями черепно-мозговой травмы, хронической внутричерепной гипертензии другой этиологии.
ЛЕЧЕНИЕ ВЕНОЗНОЙ ЭНЦЕФАЛОПАТИИ
Лечение ВЭ в первую очередь связано с воздействием на заболевания, которые могут осложниться венозным застоем в мозге. Следует учитывать причину, особенности проявлений и течения патологического процесса. Если установлена причина расстройств венозного кровообращения в мозге, то лечение направляется на ее ликвидацию или смягчение. Так, например, при сердечной недостаточности основными являются лекарственные средства, направленные на ее коррекцию; при хронической обструктивной болезни легких требуется ее лечение; при сдавлении вен опухолью или рубцом (после травмы или воспаления), затрудняющих отток крови из полости черепа, решается вопрос о хирургическом вмешательстве.
Патогенетически обоснованным при ВЭ является применение венотонизирующих препаратов, повышающих тонус венозной стенки и усиливающих венозный отток из полости черепа.
Учитывая взаимосвязь венозной и ликворовыводящей системы полезно при застойно-отечной форме заболевания назначение препаратов, ограничивающих продукцию спинномозговой жидкости. Вследствие венозного застоя происходят нарушения микрогемоциркуляции в ее венозном, а затем и артериальном звене, что является показанием для применения лекарств, способствующих улучшению кровообращения в системе микрогемоциркуляции. С целью улучшения фукционального состояния мозга показаны нейрометаболические препараты. Вследствие развития при ВЭ ишемического каскада и неблагоприятного воздействия окислительного стресса обосновано применение антиоксидантной терапии. Большую роль при ВЭ играют и немедикаментозные методы лечения.
При ВЭ, характеризующейся венозным застоем, не рекомендуются препараты, увеличивающие объем артериальной крови в полости черепа, применение которых может приводить к повышению внутричерепного давления. С этой точки зрения из антигипертензивных препаратов не рекомендованы блокаторы медленных кальциевых каналов (амлодипин). Амлодипин обладает сосудорасширяющим действием за счет блокады поступления ионов кальция через мембраны в гладкомышечные клетки сосудов, снижает тонус сосудистой стенки и уменьшает общее периферическое сопротивление. Его фармакологический механизм направлен на расслабление артерий при неизменном тонусе венозной системы.
Нецелесообразно назначать при ВЭ и цереброваскулярные препараты с выраженным сосудорасширяющим действием. В эту разнообразную по фармакологическому действию группу входят алкалоиды спорыньи (ницерголин, эрголоида мезилат), блокаторы кальциевых каналов (циннаризин, нимодипин), производные пурина (пентоксифиллин), корректоры нарушений мозгового кровообращения (винпоцетин, интестенон), ингибиторы фосфодиэстеразы (папаверин, дротаверин, бенциклан), адреноблокаторы (пропранолол, атенолон, метопролоп).
Никотиновая кислота относится к группе ферментов, выступающих переносчиками водорода НАД и НАДФ, регулирует окислительно-восстановительные процессы, тканевое дыхание, синтез белков и жиров, распад гликогена. Она оказывает сосудорасширяющее действие, в том числе на сосуды головного мозга. Таким же, но менее выраженным действием обладают ее производные (ксантинола никотинат и никотинамид).
В лечении больных с ВЭ важное место занимает медикаментозная терапия, направленная на улучшение интракраниального венозного оттока. К сожалению, вопросы фармакотерапии расстройств венозного мозгового кровообращения до сих пор остаются спорными и недостаточно изученными. При ВЭ применяются венотонические препараты, используемые флебологами при лечении периферической и системной венозной недостаточности.
Венотонизирующие препараты по своему составу подразделяются на несколько фармакологических групп:
- содержащие растительные экстракты – флавоноиды и сапонины;
- содержащие рутозид;
- комбинированные и синтетические.
Флавоноиды – это растительные биологически активные вещества (класс растительных полифенолов), содержащиеся в овощах, фруктах, красном вине, зеленом чае и т.д. К известным венотоникам этой группы относятся препараты, содержащие гесперидин + диосмин, диосмин, сухой экстракт красных листьев винограда.
Сапонины – природные органические соединения (гликозиды), которые находятся во многих растениях, в том числе лекарственных (солодка, конский каштан, аралия маньчжурская, хвощ полевой, календула лекарственная и др.). Сапонины обладают гемолитической активностью. Представителями этой группы являются венотоники на основе эсцина и др.
Рутозиды (гликозид флавоноида кверцетина) выделены в отдельную группу из-за своей высокой Р-витаминной активности. Добывают рутозиды из листьев и цветов гречихи, руты пахучей, софоры японской, листьев чая, зеленых плодов грецкого ореха (мякоти). Эти венотонизирующие средства оказывают достаточно сильный стимулирующий эффект на гладкомышечные элементы стенок вен. Из рутозидсодержащих препаратов в медицине используют рутозид, троксерутин. Но чаще рутозиды используют в комбинированных препаратах, что позволяет увеличить биодоступность и усилить полезные свойства биоактивных веществ. Комбинированные препараты содержат как средства растительного происхождения, так и их комплексы с синтетическими или полусинтетическими веществами. Их действие связано с уменьшением воспалительных процессов, возникающих при заболеваниях венозной системы, укреплением сосудистой стенки и уменьшением отечности. К комбинированным препаратам относится экстракт гингко билоба, содержащий флавоноидные гликозиды, гингколиды и билобалид. Наряду с улучшением венозного кровообращения и реологических свойств крови гингко билоба обладает нейрометаболическим действием.
К синтетическим венотоникам относятся препараты, включающие такие лекарственные вещества, как кальция добезилат, трибенозид. Считается, что механизм их действия при хронической патологии вен идет по пути угнетения медиаторов воспаления и боли.
Как правило, венотонические препараты назначаются длительными курсами по 2–3 мес.
К новым лекарственным веществам с противоотечным и венотонизирующим действием относится L-лизина эсцинат, являющийся водорастворимым соединением сапонина эсцина из плодов каштана конского и аминокислоты L-лизина. Эсцин проявляет свою антиэкссудативную активность опосредованно, стимулируя выработку и высвобождение простагландиноподобного вещества (ПГ‑2). Существует предположение, что противовоспалительное действие эсцина обусловлено его влиянием на кору надпочечников и способностью стимулировать секрецию глюкокортикоидов. Кроме того, эсцин, угнетая активность лизосомальных гидролаз, препятствует расщеплению мукополисахаридов в стенках капилляров и окружающей их соединительной ткани и уменьшает повышенную сосудисто-тканевую проницаемость. Венотонизирующее действие эсцина обусловлено стимуляцией синтеза и высвобождения простагландина F2a в венозной стенке [30].
Одним из патогенетически обоснованных методов лечения ВЭ служит ограничение продукции спинномозговой жидкости, поскольку ее резобция осуществляется в венозные синусы.
Продукция ликвора в эпендиме желудочков мозга, как и других секреторных процессов, осуществляется с помощью карбоангидразы, цинковового металлофермента, который катализируют превращение карбоксида в угольную кислоту. Этот фермент обнаружен также на внешней поверхности глиальных клеток. Учитывая роль карбонангидразы в секреторных процессах и образовании ликвора, показано при гипертензионно-гидроцефальным синдроме применение препаратов, ингибирующих действие этого фермента. К ингибиторам карбоангидразы относится ацетазоламид.
Ацетазоламид снижает ВЧД, которое может повышаться при выраженной венозной гиперемии мозга. В проспективном исследовании (Mohamad et. al., 2013) при прямом измерении ВЧД выявлено снижение ВЧД через 4 ч после перорального введения 500 мг препарата [31]. В приведенном наблюдении ни у одного больного не было выявлено гипокалиемии после длительного применения ацетазоламида. Использование этого препарата совместно с сердечными гликозидами вызывает снижение скорости ликворобразования на 95% [32].
Применение инъекций ацетазоламида рекомендовано в начале лечения у больных с выраженной ВЭ [33]. Оптимальная его доза при тяжелой ВЭ с псевдотуморозным течением у взрослых пациентов составляет 750 мг/сут в первую неделю лечения, далее возможно применение поддерживающей дозы 250 мг в течение трех недель. Перерывов на каждый четвертый день при использовании ацетазоламида делать не нужно. Одновременно желательно применение препаратов с калием.
ЗАКЛЮЧЕНИЕ
ВЭ вследствие разнообразных причин ее возникновения является распространенной патологией в клинической практике врачей первичного звена здравоохранения. Ее своевременная диагностика и патогенетически обоснованное лечение способствуют улучшению качества жизни пациентов.



