ВВЕДЕНИЕ
Тубулоинтерстициальные нефриты (ТИН) входят в группу тубулоинтерстициальных болезней почек (ТИБ), которая представляет собой врожденные или приобретенные болезни почек, проявляющиеся поражением тубулоинтерстиция и характеризующиеся острым или хроническим течением.
Выделяют острую и хроническую формы ТИН – ОТИН и ХТИН.
ХТИН – хроническое заболевание почек, которое развивается в ответ на длительное воздействие экзогенных и/или эндогенных факторов и проявляется воспалительными изменениями тубулоинтерстициальной ткани с формированием интерстициального фиброза и тубулярной атрофии с частым развитием хронической болезни почек (ХБП) [1].
В клинической практике ТИН встречаются часто в качестве приобретенных форм, преимущественно по причине лекарственного воздействия или инфекционного воспаления ткани почки (пиелонефрит). При выполнении пункционной нефробиопсии ХТИН выявляется в 1,8–2,5% случаев. Однако, по данным клинических исследований, удельный вес ХТИН несколько выше и составляет от 4 до 12%, а в случае необъяснимых заболеваний почек его частота достигает 27% [2].
ЭТИОЛОГИЯ
Выделяют наследственные формы ТИБ (например, аутосомно-доминантная тубулоинтерстициальная болезнь почек), которые регистрируются крайне редко, и приобретенные формы.
Причины развития ОТИН и ХТИН схожи, и нередко хронические формы представляют собой трансформацию рецидивирующих острых форм. ХТИН развиваются в ответ на воздействие лекарств, солей тяжелых металлов и ряда других химических веществ, радиации, а также при опухолях крови и внутренних органов, нарушениях обмена веществ (подагра, сахарный диабет, гиперурикемия и т.д.), наследственных (болезнь Фабри и др.) и инфекционных болезнях (бактериальных, вирусных, грибковых) [3, 4].
К причинам развития приобретенных форм ТИН относятся:
- лекарства;
- инфекции (бактерии, грибы, вирусы, паразиты);
- аутоиммунные болезни (саркоидоз, IgG4-ассоциированные болезни, синдром Шегрена, синдром тубулоинтерстициального нефрита-увеита, системная красная волчанка, системные васкулиты, болезнь Крона, артропатии, в том числе ревматоидный артрит и подагра);
- метаболические нарушения (острая и хроническая уратная нефропатия, оксалатная нефропатия, болезни накопления, нефрокальциноз);
- системные заболевания (холестериновая атероэмболия, парапротеинемии, лимфопролиферативные заболевания, тромботические микроангиопатии, комплементопатии);
- опухолевые заболевания (злокачественные, реже доброкачественные опухоли);
- поствакцинальные реакции;
- посттрансплантационные реакции;
- другие факторы (заболевания печени, хронический панкреатит, гемолитические анемии, заболевания, проявляющиеся миоглобинурией, следствие приема некоторых биологически активных добавок, в частности аристолохиевая нефропатия).
Перечень препаратов, в отношении которых описаны нефротоксические эффекты, представлен в таблице 1 [1].
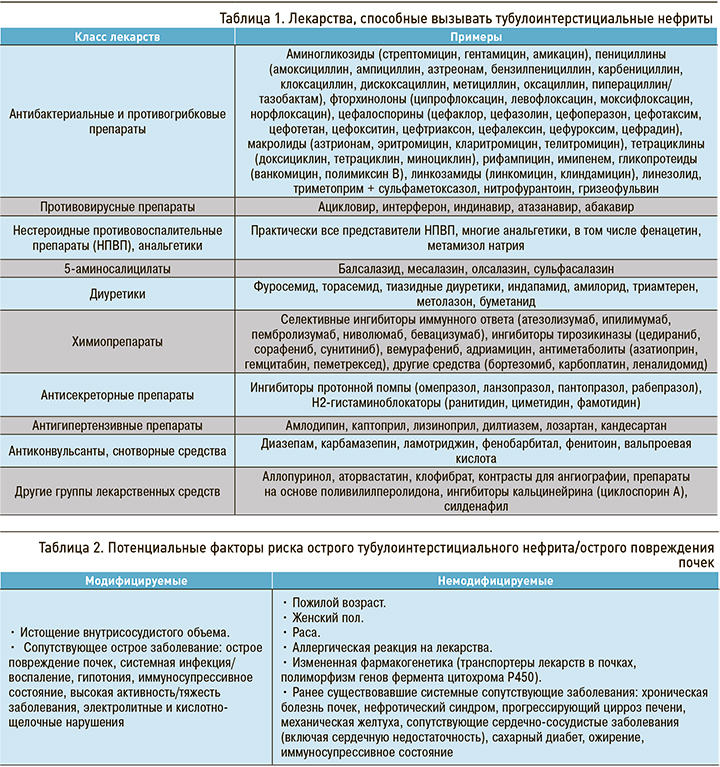
ПАТОГЕНЕЗ
К факторам, способствующим развитию поражения почек при воздействии причинного агента, относятся пожилой возраст, наличие лекарственной аллергии, гиповолемия и др. (табл. 2) [5].
Разнообразие причин ХТИН формирует широту патогенетических механизмов повреждения почки. Выделяют как прямое тубулотоксическое действие повреждающего агента (аминогликозидов, токсинов, инфекций), так и опосредованное, реализующееся через иммунные или иные механизмы (при системной красной волчанке, паранеопластическом синдроме, болезни Фабри, приеме анальгетиков и др.) или путем воздействия цитокинов, обладающих провоспалительными, профибротическими, цитотоксическими эффектами (при гиперурикемии, применении некоторых лекарств) [6].
В патогенезе ХТИН выделяют несколько этапов: интраренальная вазоконстрикция; блокада микроциркуляции за счет отека интерстициальной ткани и/или развития тромботической микроангиопатии (ТМА); прямая тубулотоксичность с некрозом и атрофией канальцевого аппарата; воспаление интерстициальной ткани, в том числе за счет реакций гиперчувствительности замедленного типа и др.
Предполагаются следующие механизмы развития ТИН в ответ на лекарственное воздействие [7]:
- компонент лекарственного средства (гаптен) связывается с базальной мембраной канальцев, и они вместе инициируют иммунный ответ;
- антиген лекарственного происхождения (часто продукт конъюгации лекарственного средства или его метаболит, связанный с белком хозяина), находящийся в кровотоке, будучи структурно подобен компоненту базальной мембраны канальцев (молекулярный имитатор), запускает иммунный ответ, который нацелен на мембрану (эндогенный антиген);
- антиген лекарственного происхождения, попавший в интерстициальное пространство, вызывает иммунный ответ in situ, опосредованный Т-клетками или медикаментозными антителами;
- полученный из лекарственного средства циркулирующий иммунный комплекс антиген + антитело попадает в ловушку в интерстиции, где вызывает воспалительную реакцию.
Однако, несмотря на очевидную связь развития ХТИН с рядом факторов, далеко не всегда их повреждающее действие детально исследовано.
КЛИНИКА И ДИАГНОСТИКА
В клинической практике проявления ХТИН могут иметь как яркую клиническую манифестацию с симптомами, не имеющими отношения к повреждению почек (лихорадка, интоксикация, сыпь, артралгии), так и исключительно проявления, обусловленные поражением почек.
Проявления мочевого синдрома наблюдаются чаще всего в виде персистирующей эритроцитурии, протеинурии донефротического уровня, реже – абактериальной или бактериальной (при пиелонефрите) лейкоцитурии. Артериальная гипертензия (АГ) является частым спутником ХТИН и требует обязательной верификации и лечения. Следует заметить, что синдром АГ не имеет каких-либо диагностически значимых отличий от такового при гипертонической болезни. У больных с ХТИН, как правило, не происходит изменения объема суточного диуреза, в ряде случаев может наблюдаться полиурия, реже – олигурия (например, в период обострения при уратной нефропатии, пиелонефрите и др.). Отмечается постепенное угасание почечной функции, которое выражается в постепенном снижении скорости клубочковой фильтрации (СКФ).
Важный аспект диагностики ХТИН – наличие в большинстве случаев этиологического фактора в дебюте и в процессе развития заболевания. Учет этого фактора может помочь не только в верификации ХТИН, но и при прогнозировании течения заболевания. В качестве примера приведем критерии диагностики ХТИН, ассоциированного с приемом нестероидных противовоспалительных препаратов (табл. 3) [4, 6, 7]. При этом учитывается продолжительность терапии этими лекарственными средствами и рассчитывается примерная суммарная доза принятого препарата за весь период его использования.

При подозрении на аутосомно-доминантную тубулоинтерстициальную болезнь почек (АДТБП) и при проведении дифференциальной диагностики с другими формами ТИБ, в частности с ХТИН, следует использовать нижеприведенные диагностические критерии АДТБП, предложенные в рамках консенсуса KDIGO [8].
А. Критерии предположительного диагноза АДТБП:
- семейный анамнез, соответствующий аутосомно-доминантному типу наследования ХБП, удовлетворяющий клиническим характеристикам (*прогрессирующее снижение функции почек, мало выраженные изменения мочевого осадка, отсутствие или слабо выраженная альбуминурия/протеинурия, отсутствие тяжелой АГ на начальных стадиях, отсутствие назначения лекарств, потенциально способных вызвать тубулоинтерстициальный нефрит, нормальные или уменьшенные размеры почек при ультразвуковом исследовании, ночная полиурия или энурез у детей вследствие снижения концентрационной способности почек);
- при отсутствии положительного семейного анамнеза ХБП, удовлетворяющего клиническим характеристикам, наличие определенных признаков при гистологическом исследовании биоптата почки (**интерстициальный фиброз, атрофия канальцев, утолщение или ламелляция базальных мембран канальцев, возможная дилатация канальцев – микроцисты, отрицательный результат иммунофлюоресценции на предмет исследования отложений комплемента или иммуноглобулинов) или внепочечных проявлений, согласующихся с мутациями HNF1B, или анамнеза ранней гиперурикемии и/или подагры.
В. Критерии установленного диагноза АДТБП:
• семейный анамнез, соответствующий аутосомно-доминантному типу наследования ХБП, удовлетворяющий ранее перечисленным клиническим характеристикам (*) и гистологическим признакам (**) по крайней мере у одного больного члена семьи (примечание: невозможно поставить окончательный диагноз только с помощью биопсии почки)
или
• выявление мутации в одном из четырех генов у больного или по крайней мере одного члена семьи.
Генетическое исследование не может использоваться широко ввиду его высокой стоимости и отсутствия соответствующих возможностей у большинства молекулярно-генетических лабораторий, однако существуют определенные показания для такого исследования, когда его выполнение является желательным:
- взрослые больные с ХБП с подозрением на АДТБП, которые желают подтвердить диагноз;
- члены семьи больного с АДТБП с нормальной функцией почек, желающие стать донорами почки;
- здоровые лица, которых интересует уточнение наличия генетической мутации;
- взрослые, заинтересованные в проведении предимплантационной генетической диагностики, чтобы избежать наследования их ребенком мутантного аллеля;
- дети с подозрением на мутацию REN гена.
Учитывая клинические проявления ХТИН, лабораторная диагностика включает оценку уровня креатинина с расчетом СКФ, мочевины и мочевой кислоты в крови, общего анализа мочи, мочевого осадка (анализ мочи по Нечипоренко) [9]. На поздних стадиях ХТИН (ХБП 3А–5 стадий) необходим контроль параметров костно-минерального обмена (уровней кальция и фосфата крови, паратгормона и 1,25(ОН)холекальциферола), эритропоэза и обмена железа (гемоглобин крови, ферритин, трансферрин). Посев мочи на стерильность и чувствительность флоры к антибиотикам выполняется в случае предположения инфекционного (бактериального) генеза ТИН. При подозрении на вирусный генез ХТИН рекомендуются исследования по верификации вируса и иммунного ответа на него с помощью полимеразной цепной реакции и иммуноферментного анализа. При подозрении на гиперурикемический (уратный) ТИН следует проводить оценку суточной экскреции мочевой кислоты с целью выявления гиперурикозурии для диагностики патогенетической формы нарушения пуринового обмена.
Таким образом, к наиболее частым проявлениям ХТИН относятся:
- мочевой синдром (эритроцитурия, протеинурия, лейкоцитурия, урикозурия, другие формы салурии);
- синдром АГ;
- синдром гипергидратации (гиперволемия, отеки, олигоанурия, положительный водный баланс);
- симптомокомплекс почечной дисфункции (острое повреждение почек в период обострения, ХБП);
- симптомы полиурии, никтурии.
Из методов инструментальной диагностики рекомендуется всем пациентам выполнять ультразвуковое исследование (УЗИ) почек, мочевого пузыря, предстательной железы (лицам мужского пола) с целью исключения других причин патологии мочевого осадка и почечной дисфункции (в частности, острого простатита, мочекаменной болезни, поликистозной болезни и т.д.). УЗИ также призвано исключить гнойные формы пиелонефрита (карбункул, абсцесс почки, апостематозный нефрит, паранефрит), которые требуют экстренного урологического лечения. Также возможно проведение дополнительных визуализирующих исследований (спиральной компьютерной томографии или магнитно-резонансной томографии).
К пункционной нефробиопсии прибегают только в сложных диагностических ситуациях, например при возникновении трудностей дифференциальной диагностики ХТИН с гломерулонефритом, неясности генеза ХТИН, быстрых темпах прогрессирования почечной дисфункции, а также при развитии ТИН в рамках аутоиммунной патологии. При этом не рекомендуется выполнять пункционную нефробиопсию с гистологическим исследованием биоптата в качестве основного метода диагностики ХТИН.
ЛЕЧЕНИЕ
Важная задачая лечения больных с ХТИН – ограничение или прекращение действия причинного повреждающего фактора, если это представляется возможным, а также замедление прогрессирования ХБП.
При ХТИН лекарственного генеза рекомендуется по возможности отмена приема препарата, вызвавшего поражение почек. При гиперурикемическом (уратном) ХТИН, в том числе в рамках подагры, показано длительное применение урикозостатиков (аллопуринол, фебуксостат), замедляющих прогрессирование ХБП [10].
Рекомендуется назначение патогенетической терапии, направленной на прекращение или ослабление воздействия эндогенных факторов, с учетом известной этиологии, например использование глюкокортикоидов и цитостатиков в комплексном лечении больных с системными васкулитами и системной красной волчанкой.
Нормотензивным пациентам с ХТИН показано применение ингибиторов АПФ или блокаторов рецепторов к ангиотензину II в субтерапевтических дозировках с целью ренопротекции, преимущественно в случаях протеинурии, а также в качестве первого класса антигипертензивной терапии при наличии АГ [11].
Рекомендуется применение блокаторов натрий-глюкозного котранспортера 2 типа (дапаглифлозина) при ХТИН, а при наличии сахарного диабета и других представителей этого класса лекарств (эмпаглифлозина, канаглифлозина и др.) [12, 13].
Рекомендуется осуществлять коррекцию модифицируемых факторов риска прогрессирования ХБП при ХТИН (АГ, ожирения, гипергликемии, анемии, дислипидемии, гиперфосфатемии, гиперурикемии и др.) [14].
В рамках терапии ХТИН возможно использование препаратов типа пентоксифиллина, сулодексида, обладающих ренопротективными свойствами, однако следует помнить о слабой доказательной базе эффективности этих лекарственных средств.
Рекомендуется проводить антибактериальную терапию при ХТИН инфекционного генеза (пиелонефрит) в период обострения в соответствии с действующими рекомендациями по лечению инфекций мочевых путей [15]. В ходе эмпирической терапии неосложненного пиелонефрита назначают, как правило, фторхинолоны (ципрофлоксацин, левофлоксацин и др.) и цефалоспорины (цефотаксим, цефподоксим, цифтибутен, цефтриаксон и др.). Другие препараты, такие как нитрофурантоин, пероральный фосфомицин и пивмециллинам, применяют реже, поскольку они не достигают адекватной концентрации в почечной ткани и используются при инфекциях нижних мочевых путей, в частности циститах. В случае гиперчувствительности к фторхинолону или резистентности к нему возможны другие варианты терапии, которые при известной этиологии включают триметоприм + сульфаметоксазол или пероральный бета-лактамный антибиотик, если известно, что уропатоген к нему чувствителен. В качестве второго выбора возможно применение аминогликозидов (гентамицина, амикацина, но следует помнить об их потенциальной нефротоксичности), цефепима и ряда других препаратов.
Обычно курс терапии ХТИН занимает от 7 до 14 дней, но продолжительность антибактериальной терапии тесно связана с лечением основной патологии, коморбидности и осложнений.
Нередко рекомендуется применение спазмолитиков вроде дротаверина, папаверина и др. с целью снятия спазмов мочевыводящих путей, на уровне которых могут формироваться зоны затрудненной уродинамики вследствие воспалительного отека. В качестве дезинтоксикационной терапии возможна пероральная регидратация и применение кристаллоидных растворов (физиологического раствора хлорида натрия, раствора декстрозы, глюкозы и др.).
ЗАКЛЮЧЕНИЕ
Высокая встречаемость ХТИН в практике врача-терапевта диктует потребность в эффективной и быстрой диагностике этого заболевания и необходимость подбора правильного комплексного лечения. Представленные материалы могут послужить в качестве алгоритмов действий при обнаружении данной патологии врачами первичного звена.



