Диагностика тромбоэмболии легочной артерии (ТЭЛА) является достаточно трудной задачей для врачей в связи с тем, что в клинической картине преобладают либо бессимптомные, либо «маскированные» ее формы. Клиническая картина заболевания часто ассоциируется с ишемической болезнью сердца, в частности с острым коронарным синдромом (ОКС). Специфические методы диагностики, такие как ангиопульмонография, сцинтиграфия, перфузионно-вентиляционные исследования с изотопами и другие, не всегда осуществимы в рутинной медицинской практике.
Особые трудности вызывает диагностика ТЭЛА на фоне острого инфаркта миокарда (ОИМ). Своевременная диагностика этого осложнения на фоне ОИМ остается актуальной проблемой в неотложной кардиологии, решение которой может способствовать снижению летальности при ОИМ. При этом существует мнение, что ОИМ часто рецидивирует на фоне повторных окклюзий легочной артерии [1]. Вероятно, в этой ситуации сложно решить вопрос о последовательности событий. Гемодинамические эффекты, развивающиеся при ТЭЛА, включают компрессию левого желудочка (ЛЖ), сдавление правой коронарной артерии (ПКА), что, в свою очередь, может провоцировать развитие коронарогенной ишемии и инфаркта миокарда.
Сложность дифференциальной диагностики ТЭЛА и ОИМ, а также их сочетаний на фоне фибрилляции предсердий, отсутствие четких специфических клинических проявлений сопутствующей патологии, значительная вариабельность клинической картины, складывающейся из различных сочетаний симптомов, побудили нас поделиться следующим клиническим наблюдением.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
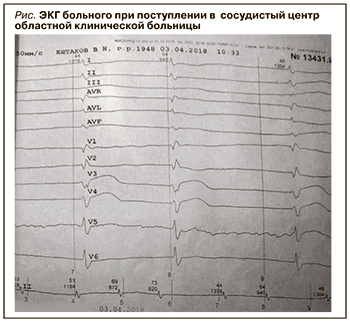 Больной Е., 69 лет, 3 апреля 2018 г. в 04:30 впервые почувствовал интенсивные давящие боли за грудиной при минимальной физической нагрузке, на короткое время купируемые спреем изосорбида динитрата, а также одышку и резкую слабость. В 10:30 был доставлен бригадой скорой помощи в районную больницу. После срочного проведения ЭКГ у больного выявили фибрилляцию предсердий брадисистолической формы, нарушение процессов реполяризации (STV2 ниже 0,6 мм, STI,AVL ниже 0,6 мм), признаки гипертрофии правого желудочка (рис. 1). Изменения на ЭКГ в сочетании с клиникой врачи расценили как острый верхушечно-боковой инфаркт миокарда. В соответствии с Европейскими клиническими рекомендациями [2] проводилось лечение дезагрегантами, гепарином. Также был выполнен тромболизис пуролазой. Однако состояние больного не улучшилось: сохранялись выраженная одышка и боли за грудиной, несмотря на введение морфина. Для «спасительного» чрескожного коронарного вмешательства пациент был отправлен в сосудистый центр областной клинической больницы (ОКБ).
Больной Е., 69 лет, 3 апреля 2018 г. в 04:30 впервые почувствовал интенсивные давящие боли за грудиной при минимальной физической нагрузке, на короткое время купируемые спреем изосорбида динитрата, а также одышку и резкую слабость. В 10:30 был доставлен бригадой скорой помощи в районную больницу. После срочного проведения ЭКГ у больного выявили фибрилляцию предсердий брадисистолической формы, нарушение процессов реполяризации (STV2 ниже 0,6 мм, STI,AVL ниже 0,6 мм), признаки гипертрофии правого желудочка (рис. 1). Изменения на ЭКГ в сочетании с клиникой врачи расценили как острый верхушечно-боковой инфаркт миокарда. В соответствии с Европейскими клиническими рекомендациями [2] проводилось лечение дезагрегантами, гепарином. Также был выполнен тромболизис пуролазой. Однако состояние больного не улучшилось: сохранялись выраженная одышка и боли за грудиной, несмотря на введение морфина. Для «спасительного» чрескожного коронарного вмешательства пациент был отправлен в сосудистый центр областной клинической больницы (ОКБ).
При поступлении в приемное отделение ОКБ 03.04.2018 в 21:10 состояние больного оставалось тяжелым: неприятные ощущения в области сердца, выраженная одышка, наклонность к гипотонии. На ЭКГ динамики не наблюдалось. На срочно проведенной селективной коронароангиографии был выявлен правый тип коронарного кровотока, атероматоз коронарных артерий. В левой коронарной артерии гемодинамически значимых сужений не определялось. В правой коронарной артерии была найдена подострая окклюзия артерии с уровня средней трети, что подтверждало наличие у больного инфаркта миокарда.
Общий анализ крови от 04.04.2018 дал следующие результаты: скорость оседания эритроцитов (СОЭ) – 3 мм/ч, лейкоциты – 12,29×109/л, эритроциты – 3,80×1012/л, гемоглобин – 110 г/л, гематокрит – 0,359 л/л, тромбоциты – 251×109/л, средний объем тромбоцита – 7,5 фл, нейтрофилы – 82,9%, эозинофилы – 0,07%, базофилы – 0,37%, моноциты – 7,65%, лимфоциты – 9%.
Общий анализ мочи соответствовал норме.
Тропонин I: 17,63нг/л.
Коагулограмма (05.04.2018): протромбиновое время – 15,5 с, протромбиновый индекс – 59%, международное нормализованное отношение (МНО) – 1,42%, активированное частичное тромбопластиновое время (АЧТВ) – 32 с, D-димер – 537 нг/мл.
Билирубин общий – 28,95мкмол/л, аспартатаминотрансфераза (АСАТ) – 97 E/L, глюкоза – 6,80 ммоль/л, креатинин – 145,5 мкмоль/л.
Тяжесть состояния больного, проявлявшаяся в первую очередь прогрессирующей дыхательной недостаточностью, гипотонией, не соответствовала левожелудочковой недостаточности, характерной для инфаркта миокарда. После проведенной эхокардиографии (ЭхоКГ) 04.04.2018 нашла подтверждение диагностическая версия о возможной ТЭЛА. Исследование выявило дилатацию правых отделов сердца, ствола легочной артерии (ЛА) и выраженную легочную гипертензию (среднее давление ЛА – 55 мм рт.ст.), а также умеренную митральную и выраженную трикуспидальную регургитацию. При этом сократительная функция левого желудочка (ЛЖ) оставалась удовлетворительной (фракция выброса – 55%), а сегментарная сократимость миокарда ЛЖ изменена: гипокинез базальных, средних, переднебоковых сегментов. Кроме этого, определялась незначительная гипертрофия стенок ЛЖ, уплотнение стенки аорты, створок аортального и митрального клапанов.
05.04.2018 было проведено дуплексное сканирование вен нижних конечностей. На момент осмотра достоверных признаков тромбофлебита обнаружено не было, но отмечался выраженный лимфостаз.
Мультиспиральная компьютерная томография (МСКТ) органов грудной клетки с внутривенным болюсным введением йопромида 370 мг/мл (06.04.2018) подтвердила диагноз ТЭЛА: на фоне гемодинамических изменений (слабой сердечной деятельности) имелись КТ-признаки ТЭЛА левой ЛА с вероятным частичным распространением на верхнюю и нижнюю ветви. Компьютерная томография выявила картину интерстициальных изменений легочной паренхимы и многочисленных двусторонних клиновидных уплотнений (инфаркт-пневмония).
Данные УЗИ органов брюшной полости от 06.04.2018: печень обычной формы, эхоструктура органа неоднородная, эхогенность повышена, имеются диффузные изменения поджелудочной железы, асцит. Нельзя исключить портальную гипертензию. Наблюдалось диффузное изменение паренхимы обеих почек.
Проводимое лечение гепарином, дезагрегантами, ингибиторами АПФ, спиронолактоном, статинами не давало эффекта. 06.04.2018 стала нарастать сердечно-легочная недостаточность, больной был переведен на искусственную вентиляцию легких (ИВЛ). С учетом наличия ТЭЛА, сопровождающейся шоком, врачами отделения отделения реанимации и интенсивной терапии (ОРИТ) было принято решение о проведении тромболизиса препаратом алтеплазы.
Показатели коагулограммы после тромболизиса (06.04.2018): нет свертывания; через 6 ч протромбиновое время – 29,6 с, протромбиновый показатель – 26,9%, МНО – 2,52, АЧТВ – 123 с.
Коагулограмма от 07.04.2018: протромбиновое время – 23,5 с, протромбиновый показатель – 35,6%, МНО – 2,0, АЧТВ – 84 с.
На ЭКГ от 08.04.2018 в 10:40 наблюдалась фибрилляция предсердий с ЧЖА 86–150 в 1 мин. Выражена перегрузка правого желудочка на фоне текущих острых коронарных нарушений.
В 14:00 того же дня состояние больного резко ухудшилось: произошла внезапная остановка сердечной и дыхательной деятельности. Реанимационные мероприятия в течение 30 мин не дали эффекта. В 14:30 была констатирована биологическая смерть.
Клинический диагноз:
- • ОЗ.1. Массивная ТЭЛА главных легочных артерий с распространением на верхние и нижние ветви с обеих сторон, инфаркт-пневмония с обеих сторон, субкомпенсированное легочное сердце.
- • ОЗ.2. ИБС: острый циркулярно-верхушечный Q-инфаркт миокарда ЛЖ, К III.
- • ООЗ. Асистолия от 08.04.2018.
- • СЗ. Гипертоническая болезнь III ст., риск 4. Постоянная форма фибрилляции предсердий, хроническая сердечная недостаточность (ХСН) III ст. (III функциональный класс), двусторонний гидроторакс, асцит, хроническая обструктивная болезнь легких (ХОБЛ).
При проведении патологоанатомического вскрытия и гистологическом исследовании материала подтверждено наличие рецидивирующей ТЭЛА, очага инфаркта миокарда в верхушечно-перегородочной области. Установлено наличие организующейся и инкапсулирующейся двусторонней инфаркт-пневмонии, ХОБЛ. Доказана гипертоническая болезнь. Установлено наличие цирроза печени на фоне жировой дистрофии, а также обнаружен микрофокус холангиоцеллюлярной карциномы печени.
ОБСУЖДЕНИЕ
При сопоставлении клинического и патологоанатомического диагнозов установлено их совпадение. На основании гистологического исследования материала ТЭЛА предшествовала развитию инфаркта миокарда. Это значит, что в описываемом клиническом наблюдении ТЭЛА не была осложнением инфаркта миокарда. Источником эмболий могли быть внутрисердечные тромбы в правых отделах сердца при постоянной форме фибрилляции предсердий, а также тромбы из венозной системы брюшной полости.
Неполный септальный цирроз печени с явлениями портальной гипертензии, выявленный на вскрытии, следует считать самостоятельной патологией, а не следствием ХСН. Скорее всего, это алкогольный цирроз печени. Косвенно подтверждают это заключение анамнестические сведения о злоупотреблении больным алкоголя, а также отсутствие выраженной атеросклеротической болезни сердца и атеросклероза аорты при патологоанатомическом исследовании. Портальная гипертензия, проявившаяся асцитом и варикозным расширением вен пищевода с участками эрозий в области сосудов, ограничивала возможности противотромботической терапии в связи с угрозой геморрагических осложнений. Тем не менее, согласно Европейским клиническим рекомендациям [2], при инфаркте миокарда и ТЭЛА, постоянной форме фибрилляции предсердий проводится терапия дезагрегантами, антикоагулянтами и в ряде случаев тромболитиками. В данном случае попытка повторного тромболизиса в связи с массивной ТЭЛА не увенчалась успехом. Наоборот, наблюдались осложнения на введение алтеплазы: полное несвертывание крови по данным коагулограммы и обнаружение при патологоанатомическом вскрытии 2 л крови в полости желудка (кровотечение из вен пищевода). Однако непосредственной причиной смерти стала рецидивирующая ТЭЛА, а не кровотечение из вен пищевода.
ЗАКЛЮЧЕНИЕ
Проблема коморбидной патологии – одна из самых трудных и обсуждаемых на сегодняшний день. Приведенный клинический случай демонстрирует сложность ранней диагностики ТЭЛА при наличии инфаркта миокарда и других заболеваний (ХСН, ХОБЛ, гипертоническая болезнь, фибрилляция предсердий, цирроз печени). Наряду с выполнением клинических рекомендаций при какой-либо патологии необходимо тщательно анализировать имеющиеся симптомы и синдромы, выделять среди них основные, проводить дифференциальную диагностику и выбирать с учетом показаний и противопоказаний рациональную терапию, принимая во внимание сопутствующую патологию.



