ВВЕДЕНИЕ
Системный подход к лечению пациентов с множеством заболеваний имеет многовековую историю. Еще светила медицины Древнего Китая обратили внимание на взаимное влияние всех процессов, протекающих в организме человека. Они применяли полную диагностику перед определением тактики лечения, целью которой являлось восстановление гармонии и баланса двух противоположных энергий (Инь и Янь) в человеческом организме.
В отечественной терапевтической школе, благодаря трудам М.Я. Мудрова, Г.А. Захарьина, Н.И. Пирогова, С.П. Боткина, по сути, было определено современное понятие коморбидности, воплощенное в императиве «лечить не болезнь, а больного» [1]. Термин «коморбидность» (лат. со – «вместе» и morbus –«болезнь») был предложен в 1970 г. Алваном Ричардом Финштейном [2]. В широком понимании он характеризует наличие у одного пациента, помимо текущего заболевания, дополнительной клинической картины, уже существующей или же появившейся самостоятельно, всегда отличающейся от основной патологии [3]. Часть авторов разделяет понятия коморбидности и мультиморбидности, определяя первую как сочетание заболеваний с общим патогенетическим механизмом, а вторую – как наличие множественных заболеваний, не имеющих единого патогенеза [4].
В 1996 г. появилось принципиальное уточнение: термин «коморбидность» было предложено использовать в случае, когда выявляется индексное заболевание, а «мультиморбидность», когда у больного присутствуют несколько хронических заболеваний, но ни одно из них не выделяется в качестве основного [5].
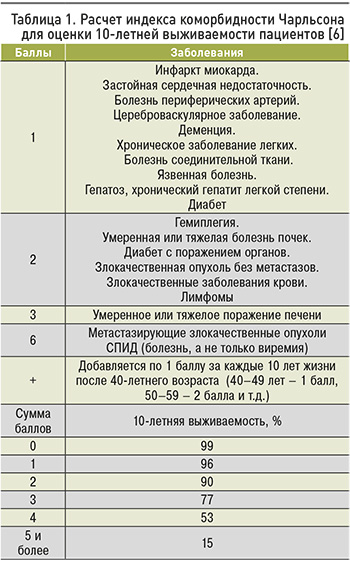
При множественной сочетанной патологии особенно важна оценка прогноза пациентов. С целью создания единой концепции лечения и прогнозирования жизни больных с сочетанными заболеваниями были разработаны методы измерения коморбидности. В систематическом обзоре Stirland L.E. et al. (2020) их представлено более тридцати [5]. В практическом здравоохранении применяется несколько калькуляторов прогноза выживаемости коморбидных пациентов. Наиболее известен индекс Чарльсона (табл. 1), который предназначен для прогнозирования смертности и представляет собой суммарную оценку сопутствующих состояний в баллах (сумма от 1 до 40) в соответствии с выявленными заболеваниями [6]. При выполнении расчетов с его помощью дополнительно прибавляют 1 балл на каждые 10 лет жизни пациента старше 40-летнего возраста. Отличительная особенность и бесспорное преимущество индекса Чарльсона – возможность оценки возраста пациента и определения уровня смертности пациента, который при отсутствии сопутствующей патологии составляет 12%, при 1–2 баллах – 26%, при 3–4 баллах – 52%, при ≥5 баллов – 85%. Таким образом, применение индекса Чарльсона – один из достоверных методов измерения коморбидности при оценке прогноза отдаленной летальности у пациентов разнообразного профиля заболеваний.
Наличие коморбидных заболеваний, наряду с прочим, увеличивает сроки и частоту повторных госпитализаций, риски осложнений, повышает угрозу инвалидизации. Кроме того, во врачебной практике коморбидность часто сопровождается полипрагмазией [7], которая увеличивает вероятность развития местных и системных побочных эффектов лекарственных средств, усложняет контроль над эффективностью терапии и зачастую снижает комплаентность пациентов [1].
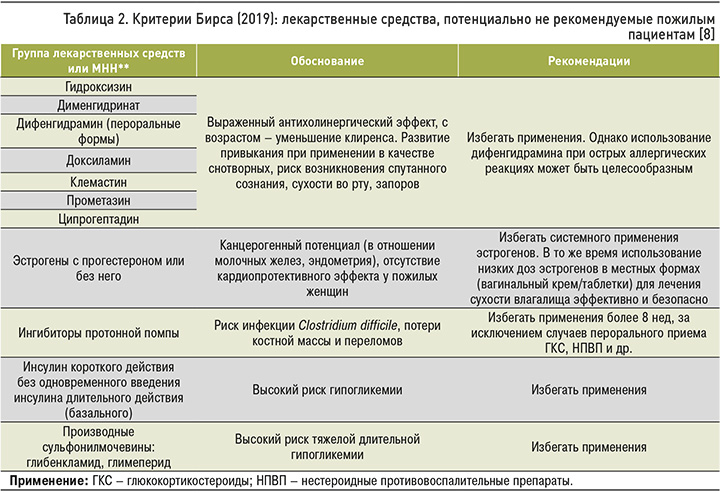
Использование критериев Американской гериатрической ассоциации (критериев Бирса – табл. 2) для пациентов старше 65 лет может способствовать рационализации фармакотерапии этой категории больных в условиях стационара и амбулаторного приема [8]. В свою очередь, применение в комплексном лечении безопасных метаболических препаратов, обладающих комплексным плейотропным воздействием, может существенно повысить эффективность проводимой терапии [9].
В 2017 г. Ассоциацией врачей общей практики (семейных врачей) Российской Федерации были разработаны клинические рекомендации по коморбидной патологии в клинической практике [10]. В нашей практике ведения коморбидных пациентов мы опираемся на опыт, рекомендации и информационные системы, разработанные Российским научным медицинским обществом терапевтов (РНМОТ) под руководством академика РАН А.И. Мартынова [9].
Все лечебные отделения «ЦКБ с поликлиникой» УДП РФ имеют возможность коллегиально, под началом А.И. Мартынова, обсуждать стратегию обследования и оптимального лечения больных с учетом возможных и прогнозируемых рисков.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Пациентка Н., 88 лет, была экстренно госпитализирована 13.03.2023 в отделение реанимации бригадой скорой медицинской помощи на лежачей каталке, минуя приемное отделение, с жалобами на тошноту, рвоту с примесью алой крови, последующий жидкий стул малинового цвета, возникшие накануне госпитализации. Клинические проявления были расценены как острое кровотечение.
Данные анамнеза: ишемическая болезнь сердца (ИБС), постинфарктный кардиосклероз (ПИКС) от 06.2022 с исходом в хроническую аневризму левого желудочка (ЛЖ) больших размеров. Хроническая сердечная недостаточность (ХСН) 2-го функционального класса (ФК) со снижением фракции выброса. Нарушения ритма сердца, пароксизмальная форма фибрилляции предсердий (ФП), вне пароксизма. Перенесенное острое нарушение мозгового кровообращения (ОНМК) в бассейне левой средней мозговой артерии (2015). Гипертоническая болезнь (ГБ) III ст., сахарный диабет 2-го типа, нарушения пуринового обмена, хроническая болезнь почек (ХБП).
Лекарственный анамнез: базовая терапия – изосорбида динитрат 20 мг утром и вечером, фуросемид 40 мг утром, бисопролол 5 мг утром, аллопуринол 100 мг/сут, апиксабан 2,5 мг утром и вечером, аторвастатин 20 мг вечером, инсулин-изофан (человеческий генно-инженерный) 24 ЕД/сут. На протяжении последнего месяца перед госпитализацией – бесконтрольный прием анальгетиков и нестероидных противовоспалительных препаратов по поводу суставно-болевого синдрома.
Данные объективного осмотра при поступлении: состояние пациентки было расценено как тяжелое, обусловленное гипотонией (снижение артериального давления до 80/50 мм рт.ст.), тахикардией (120/мин), десатурацией (87%). Частота дыхательных движений (ЧДД) 28/мин, частичная дезориентация больной во времени, месте и пространстве.
Пациентка гиперстенического телосложения. Индекс массы тела 33,2 кг/м2. Температура тела 36,7 °С. Кожные покровы выраженной бледности, повышенной влажности. Периферические симметричные отеки голеней и стоп. Трофические язвы обеих голеней (до 60 мм в диаметре) в стадии эпителизации. Аускультативно: дыхание диффузно ослабленное, везикулярное, над задненижними отделами с обеих сторон выслушивается большое количество влажных мелкопузырчатых хрипов. Тоны сердца глухие, грубый систолический шум на верхушке. Акцент II тона в аорте. Язык сухой, густо обложенный белым налетом. Живот при пальпации болезненный в эпигастральной области. Нижний край печени выступает из-под реберной дуги на 1 см. Мочеиспускание свободное, безболезненное. Симптом Пастернацкого отрицательный с обеих сторон.
Лабораторные данные при поступлении: анемия тяжелой степени (гемоглобин – 65 г/л, эритроциты – 2,2×1012/л, гематокрит – 20%); повышение маркеров воспаления (лейкоцитоз до 13,2×109/л, нейтрофилы абс. – 11,75×109/л (89%), палочкоядерные – 4%, сегментоядерные – 85%); изолированный подъем уровня тропонина при нормальном уровне креатинкиназы (тропонин – 0,053 мкг/л, креатинкиназа – 69,9 Мед/л); признаки острого почечного повреждения (повышение креатинина до 190,1 мкмоль/л, мочевины – до 32,39 ммоль/л, показатель скорости клубочковой фильтрации (СКФ по CKD-EPI) 20,00 мм/мин); гипергликемия (28 ммоль/л); в гемостазе – гипокоагуляция (протромбиновое время 13,5 с, международное нормализованное отношение 1,22, протромбин по Квику – 78%).
В общем анализе мочи: протеинурия – 312 мг/л; лейкоцитурия – 7–10 в поле зрения; глюкозурия – 4,7 ммоль/л.
По CITO пациентке была выполнена эзофагогастродуоденоскопия (ЭГДС) в течение 30 мин с момента поступления: выявлена острая язва препилорического отдела желудка размером 10×7 мм, дно которой покрыто фибрином, без признаков продолжающгося кровотечения. В теле и антральном отделе по всем стенкам визуализировались эрозии, размером до 0,2 см в диаметре, покрытые налетом гематина (рис. 1, 2).

Данные электрокардиографии (ЭКГ) при поступлении: синусовый ритм, частота сердечных сокращений (ЧСС) 86 уд/мин. Признаки перегрузки левого предсердия, гипертрофии миокарда ЛЖ, очаги кардиофиброза переднеперегородочной области ЛЖ. Недостаточность кровоснабжения миокарда передней и задней стенок ЛЖ с развитием острых очаговых изменений миокарда передневерхушечной локализации (рис. 3).
Данные эхокардиографии (ЭхоКГ) при поступлении: гипокинезия базального заднебокового, среднего переднего, среднего переднебокового, среднего заднебокового сегментов, акинезия среднего переднеперегородочного, верхушечного бокового, верхушечного заднего сегментов, дискинезия передневерхушечного, перегородочно-верхушечного сегментов. Аневризма ЛЖ больших размеров верхушечной локализации. Расширение левого предсердия до 130 мл. Снижение фракции выброса (ФВ) до 26%, свидетельствующее об осложнении ПИКС с формированием хронической аневризмы.

Данные мультиспиральной компьютерной томографии (МСКТ) органов грудной клетки при поступлении: признаки двусторонней полисегментарной нижнедолевой бронхопневмонии на фоне гипостатических изменений легких, минимальный двусторонний плевральный выпот (слева – с примерным объемом около 100 мл, справа – в следовом количестве; рис. 4, 5).
Данные цветового дуплексного сканирования (ЦДС) вен нижних конечностей при поступлении: необтурирующие тромботические массы глубоких вен голени (задних большеберцовых и малоберцовых) обеих нижних конечностей, обтурирующие тромботические массы мышечного притока правой голени. Верхний уровень распространения тромботических масс соответствует верхней трети обеих голеней.
Лечение пациентки в условиях ОРИТ проводилась с участием ведущих специалистов клиники (совместно с гастроэнтерологом, кардиологом, неврологом, эндокринологом). Учитывая риск продолжения кровотечения, с момента поступления были отменены антикоагулянты и инициирована гастропротективная терапия: ингибитор протонной помпы (омепразол 80 мг/сут внутривенно), антацид (алгелдрат + магния гидроксид), индуктор синтеза простагландинов (ребамипид 100 мг 3 раза/сут). С целью коррекции кровопотери были выполнены заместительные гемотрансфузии – суммарно 7 доз эритроцитарной взвеси, 4 дозы свежезамороженной плазмы.
Согласно клиническим рекомендациям, с учетом снижения СКФ пациентке была начата антибактериальная терапия препаратом широкого спектра действия (эртапенем 1 г/сут) с последующей оценкой ее эффективности.
Также проводились инфузионная терапия, коррекция гипергликемии, нефропротективная терапия. С учетом риска повторного развития кровотечения (сохранялась примесь крови в стуле) в первые сутки антикоагулянтная терапия не возобновлялась.
Течение заболеваний в стационаре
При контроле лабораторных показателей пациентки на 2-й день терапии на фоне заместительной гемотрансфузии показатели эритроцитарного ростка крови имели тенденцию к стабилизации: гемоглобин – 96 г/л, гематокрит – 29%, эритроциты – 3,3×1012/л. В то же время был выявлен рост маркеров повреждения миокарда: тропонина – с 0,053 до 2,171 мкг/л, креатинкиназы – до 674 Мед/л, креатинкиназы-МВ – до 66,5 Мед/л, N-концевого пропептида натриуретического гормона В-типа (NT-proBNP) – до 37876,0 пкг/мл. Уровень креатинина составлял 182,8 мкмоль/л, мочевины – 32,9 ммоль/л.
Таким образом, у больной с острой язвой желудка, постгеморрагической анемией на фоне гипоксии, гипотонии течение заболевания осложнилось вторичным повреждением миокарда, острым повреждением почек 3 ст. по KDIGO. Уровень азотемии не нарастал, диурез сохранялся адекватным водной нагрузке. Проводилась нефропротективная терапия.
При контрольном дуплексном сканировании вен нижних конечностей на 3-е сутки наблюдалось прогрессирование тромбообразования, было обнаружено появление тромботических масс в подколенной вене справа. Пациентка была осмотрена сосудистым хирургом, врачом антитромботического кабинета. С учетом характера и уровня тромбоза, отсутствия признаков флотации показаний к хирургическому лечению определено не было. На фоне сниженной функции почек (СКФ 17,75 мл/мин) с сохранением риска геморрагических осложнений больной была инициирована антикоагулянтная терапия (парнапарин натрия 4250 анти-Ха/0,4 1 раз/сут), назначена эластическая компрессия нижних конечностей.
На фоне проводимой гастропротективной, гемотрансфузионной, инфузионной терапии состояние пациентки стабилизировалось, гемоглобин повысился до 112 г/л, уровень эритроцитов составлял 3,8×1012/л, гематокрита – 34%, креатинина – 179 мкмоль/л, мочевины – 16 ммоль/л.
На 10-е сутки нахождения в стационаре у пациентки произошло развитие генерализованного судорожного синдрома с оглушением, нарушением акта глотания. По данным магнитно-резонансной томографии (МРТ), повторные ОНМК были исключены. На электроэнцефалограмме (ЭЭГ) регистрировалась межполушарная асимметрия основного ритма за счет его подавления слева, а также продолженное дельта-замедление в центрально-теменно-височных отделах левого полушария. Четкой эпилептиформной активности выявлено не было.
Кроме того, лабораторно в этот период отмечался рост азотемии, уремии (креатинин – 252,4 мкмоль/л, мочевина – 40,16 ммоль/л, мочевая кислота – 616,0 мкмоль/л, без электролитных нарушений). Инициирован острый гемодиализ (с 23.03.2023). С учетом развития генерализованного судорожного приступа пациентке была начата противоэпилептическая терапия с положительным эффектом на 2-е сутки. В этот же период было выявлено повышение температуры тела до фебрильных цифр. В лабораторных тестах наблюдались появление лейкоцитоза (10,5×109/л), подъем уровня С-реактивного белка до 130 мг/л. В моче – элементы гриба Candida. В анализах кала выявлен токсин C. difficile класса В. Мазки на SARS-CoV-2, ОРВИ отрицательные. По данным контрольной МСКТ, были исключены инфильтративные изменения. Генез гипертермии был связан с развитием клостридиального колита, микотической инфекции на фоне вторичного иммунодефицита и анемии тяжелой степени. Проводилась эффективная патогенетическая терапия (ванкомицин 1000 мг/ сут, флуконазол перорально).
За время пребывания в стационаре пациентке с ХБП С5, уремией, нарушением электролитного баланса, сопровождающегося выраженной общемозговой симптоматикой, были проведены сеансы заместительной почечной терапии с положительным клинико-лабораторным эффектом: снижение креатинина с 250 до 160 мкмоль/л, мочевины – с 42 до 11 ммоль/л, нормализация показателей воспалительных маркеров (лейкоциты – 6,3×109, С-реактивный белок – 10 мг/л). При попытках сокращения диализной терапии наблюдалось нарастание уремической энцефалопатии, гиперкалиемии (до 6,2 ммоль/л), метаболического ацидоза, гиперволемии, в связи с чем было принято решении о переводе пациентки на программный гемодиализ, обеспечен доступ перманентным манжеточным катетером, имплантированным в левую внутреннюю яремную вену.
Кроме этого, в ранние сроки госпитализации к комплексному лечению была привлечена мультидисциплинарная бригада по реабилитационно-восстановительному лечению: проводились ежедневная лечебная физкультура, механотерапия, направленная на активизацию, сохранение бытовых навыков пациентки, меры по восстановлению когнитивных способностей и способности больной к самообслуживанию в пределах догоспитального объема. Также в комплекс лечебных мероприятий было включено физиотерапевтическое лечение (магнитотерапия, лазеротерапия).
В результате комплексного лечения [11] была достигнута клиническая, лабораторно-инструментальная положительная динамика, отмечалось улучшение самочувствия и состояния пациентки. Регрессировали проявления постгипоксической энцефалопатии с улучшением интеллектуально-мнестических, когнитивных функций, уменьшением проявлений гипомимии, восстановился акт глотания. Судорожный синдром не рецидивировал. Произошло рубцевание трофических язв голеней, гемодинамика стабилизирована на целевых значениях. Уровень гликемии на фоне сахароснижающей терапии (инсулин-изофан человеческий генно-инженерный 24 ед/сут) находился в пределах допустимых значений. Наблюдались уменьшение лабораторных признаков анемии (повышение гемоглобина с 65 до 101 г/л, уровень эритроцитов – 3,7×10/12л), положительная динамика в течении ХБП (снижение креатинина с 280 до 160 мкмоль/л, мочевины – с 40 до 18 ммоль/л).
При проведении контрольной ЭГДС отмечалось рубцевание язвы желудка, исчезновение признаков эрозивных изменений слизистой оболочки (рис. 6).

По данным МСКТ органов грудной клетки, инфильтративные изменения регрессировали (рис. 7).
По данным ЭхоКГ, ФВ при динамическом контроле возросла с 26 до 30%.
При дуплексном сканировании наблюдалась реканализация тромбированных вен нижних конечностей.
Пациентка в состоянии стабильно средней тяжести была выписана домой с продолжением сеансов программного гемодиализа – 2 раза в неделю. С учетом рекомендаций по критериям Бирса (см. табл. 2) была скорректирована антигипертензивная и сахароснижающая терапия. Согласно индексу Чарльстона, риск летальности пациентки в течение следующих 10 лет составил более 85% (расчетная сумма баллов = 18).
Заключительный клинический диагноз:
K25.4. Язвенная болезнь желудка с локализацией язвы в препилорическом отделе желудка, впервые выявленная. Эрозивный гастрит. Состоявшееся желудочное кровотечение 13.03.2023. Острая постгеморрагическая анемия тяжелой степени. Гемотрансфузии: эритроцитарная взвесь 7 доз. Трансфузия свежезамороженной плазмы 4 дозы.
Фоновый: сахарный диабет 2-го типа. Целевой уровень гликированного гемоглобина менее 8%. Диабетическая дистальная полинейропатия нижних конечностей, сенсомоторная форма. Мочекаменная болезнь. Кисты почек. Хронический пиелонефрит. Нефропатия смешанного генеза (атеросклеротическая, диабетическая). ХБП С5 (СКФ 15 мл/мин). Мультифокальный атеросклероз: атеросклероз коронарных, брахиоцефальный артерий, стенозирующий атеросклероз артерий нижних конечностей.
Осложнения: I22.0 ИБС. Острый передний распространенный инфаркт миокарда (тип 2 по ЕОК) от 13.03.2023. ХСН 3 ст, IV ФК с низкой ФВ (30%). ОСН класс I по Т. Killip от 13.03.2023. Двусторонняя внебольничная пневмония в нижних долях легких смешанного генеза: бактериальная, застойная. Дыхательная недостаточность 3 ст. Белково-электролитные нарушения. Острое почечное повреждение 13.03.2023. Острый гемодиализ, 9 сеансов. 21.04.2023 операция: установка манжеточного ЦВК 28.04.2023. Тромбоз глубоких вен обеих голеней (15.03.2023) в стадии реканализации.
Сопутствующие заболевания: энцефалопатия сложного генеза 3 ст., декомпенсация. Последствия перенесенного ОНМК в 2005 г. с правосторонним гемипарезом. Доброкачественное образование левой височной доли (оперированное в 2004 г.). Стеатоз печени, поджелудочной железы. Дивертикулярная болезнь толстой кишки без признаков дивертикулита. Варикозная болезнь вен нижних конечностей. ХВН 6 по CEAP. Посттромботическая болезнь правой нижней конечности. Трофические язвы нижних конечностей Многоузловой коллоидный эутиреоидный зоб.
ЗАКЛЮЧЕНИЕ
У коморбидных пациентов при острых событиях развивается декомпенсация хронических, длительно протекающих, взаимоотягчающих патологических процессов с возможным присоединением осложнений, угрожающих жизни [12]. В нашем клиническом примере острая язва с желудочным кровотечением стала триггером, спровоцировавшим целый каскад взаимопотенциирующих патологических процессов. Постгеморрагическая анемия, гемическая гипоксия привели к декомпенсации хронических заболеваний: ИБС, сахарного диабета, энцефалопатии. Это, в свою очередь, вызвало развитие комплекса осложнений – двусторонней полисегментарной пневмонии, острой почечной недостаточности, генерализованного судорожного синдрома, нарушения в системе гемостаза (коагулопатии потребления).
Лечение пациентов с коморбидной патологией требует многофакторного воздействия на все звенья патологического процесса, что решается совместной работой мультидисциплинарной бригады специалистов (в нашем случае это были терапевт, гастроэнтеролог, гематолог, пульмонолог, невролог, эпилептолог, эндокринолог, нефролог, уролог, гнойный хирург). Важным звеном ведения больного являются реабилитационно-восстановительные мероприятия, направленные на активизацию, расширение двигательных функций, восстановление бытовых навыков, поддержание когнитивного статуса, т.е. показателей, влияющих на качество жизни пациента. Реабилитация может включать диетотерапию, лечебную физкультуру, физиотерапевтическое лечение, массаж и другие методы. Только слаженная работа специалистов может привести к успеху, компенсации множественных патологических процессов и выписке пациентов на амбулаторный этап.
Лечение коморбидных пациентов пожилого возраста сопровождается значительными финансовыми затратами и эффективнее всего проводятся в условиях крупных многопрофильных стационаров, обладающих как кадровым составом, так и необходимой материально-технической базой для оказания медицинской помощи таким больным.



