ВВЕДЕНИЕ
Несмотря на очевидный прогресс в диагностике и лечении сердечно-сосудистых заболеваний, на сегодняшний день они остаются одной из основных причин смертности и инвалидизации во всем мире. Более того, в перспективе ожидается дальнейшее увеличение распространенности сердечно-сосудистой патологии, ожирения и сахарного диабета (СД) 2-го типа [1, 2].
Согласно данным литературы, около 200 млн человек во всем мире имеют заболевания периферических артерий, при этом более чем у половины из них диагностируются ишемическая болезнь сердца (ИБС) и(или) цереброваскулярные заболевания [3, 4]. В многочисленных эпидемиологических исследованиях выявлена связь между атеросклеротическим процессом сонных артерий с наличием и степенью выраженности атеросклероза коронарных сосудов [5, 6]. Накоплены данные о высокой прогностической значимости периферического атеросклероза в отношении оценки наличия и выраженности патологического процесса коронарных артерий [7, 8]. Частота обнаружения сочетанного поражения коронарных, брахиоцефальных и артерий нижних конечностей колеблется от 10 до 65%, а по данным некоторым авторов, доходит до 90% [9, 10]. Акцентируется внимание на определенных количественных и качественных характеристиках атеросклеротических бляшек, позволяющих верифицировать не только наличие, но и выраженность поражения коронарного русла.
Стратегия высокого риска – основное направление первичной профилактики хронических неинфекционных заболеваний, цель которой заключается в выявлении пациентов с вероятностью развития сердечно-сосудистой патологии, обусловленной атеросклеротическим процессом [11–13].
В реальной клинической практике используется немалое количество инструментов прогнозирования кардиоваскулярных событий. Вместе с тем большое количество проведенных ранее исследований, направленных на определение эффективности уже существующих шкал оценки риска, несомненно, требует дополнения и уточнения. Анализируя результаты этих работ, можно утверждать, что проблема определения сердечно-сосудистого риска сохраняет свою актуальность. Разработка новых шкал, отвечающих этой цели, согласно парадоксу Роуза, будет иметь огромное социально-экономическое значение [14].
Цель исследования – разработать калькулятор оценки риска сердечно-сосудистых событий и неблагоприятных исходов у больных с периферическим атеросклерозом в ходе трехлетнего проспективного наблюдения, в том числе на основании данных клинико-инструментальных характеристик эндотелиальной функции.
МАТЕРИАЛ И МЕТОДЫ
В исследование были включены 519 пациентов с атеросклеротическим поражением различных сосудистых бассейнов, находившихся на лечении в профильных отделениях ГБУ Ростовской области «Ростовская областная клиническая больница», в том числе 360 (69,4%) мужчин и 159 (30,6%) женщин. Средний возраст обследованных больных составил 60,0 ± 8,7 года.
У пациентов были собраны жалобы, также были проанализированы данные анамнеза и объективного статуса. Проведены стандартные лабораторные исследования с оценкой показателей липидного профиля. Комплекс инструментальных исследований включал выполнение ЭКГ в покое, холтер-ЭКГ, эхокардиографии, ультразвукового исследования органов брюшной полости, почек, ультразвукового триплексного сканирования (УЗТС) брахиоцефальных артерий (БЦА), УЗТС артерий нижних конечностей, вен нижних конечностей, компьютерную томографию артерий нижних конечностей, исследование сердечно-сосудистой системы с использованием аппарата «Ангиоскан». Оценке подвергались такие параметры, как частота пульса (ЧП, уд./мин.), индекс жесткости сосудов (SI, м/с), индекс отражения, используемый для оценки вклада отраженного компонента в пульсовую волну (RI, %), индекс аугментации (AIр, %), индекс аугментации при частоте пульса 75 уд./мин. (AI75, %), возрастной индекс (AGI), возраст сосудистой системы (VA, лет), длительность пульсовой волны (РD, мс), продолжительность систолы (ЕD, %), центральное систолическое давление – прогноз (Sрa, мм рт. ст.), индекс наполнения пульса (ИНП). При наличии клинической симптоматики, указывающей на присутствие патологического процесса, выполнялись коронароангиография, ангиография почечных, сонных и артерий нижних конечностей.
При разработке калькулятора оценивали результаты 195 пациентов с периферическим атеросклерозом.
Протокол исследования был одобрен локальным независимым этическим комитетом ФГБОУ ВО «Ростовский государственный медицинский университет» Минздрава России.
Артериальная гипертензия наблюдалась у 500 (96,3%), отягощенная наследственность – у 239 (46,0%), курение – у 209 (40,2%) обследованных пациентов (табл. 1) [15].
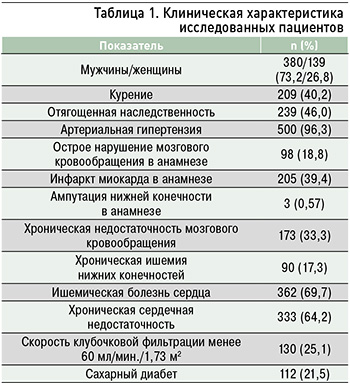
По результатам анализа проведенного ангиографического исследования атеросклеротический стеноз коронарных артерий был верифицирован у 472 (90,9%), поражение БЦА – у 199 (38,3%), стеноз почечных артерий – у 103 (19,8%), стеноз артерий нижних конечностей – у 105 (20,2%) участников, с учетом как моно-, так и комбинированного сосудистого поражения. Наличие атеросклеротического стеноза одного сосудистого региона наблюдалось у 258 (49,7%), патологический процесс в области двух бассейнов – у 170 (32,8%), трех – у 85 (16,4%), четырех – у 6 (1,1%) человек (табл. 2).
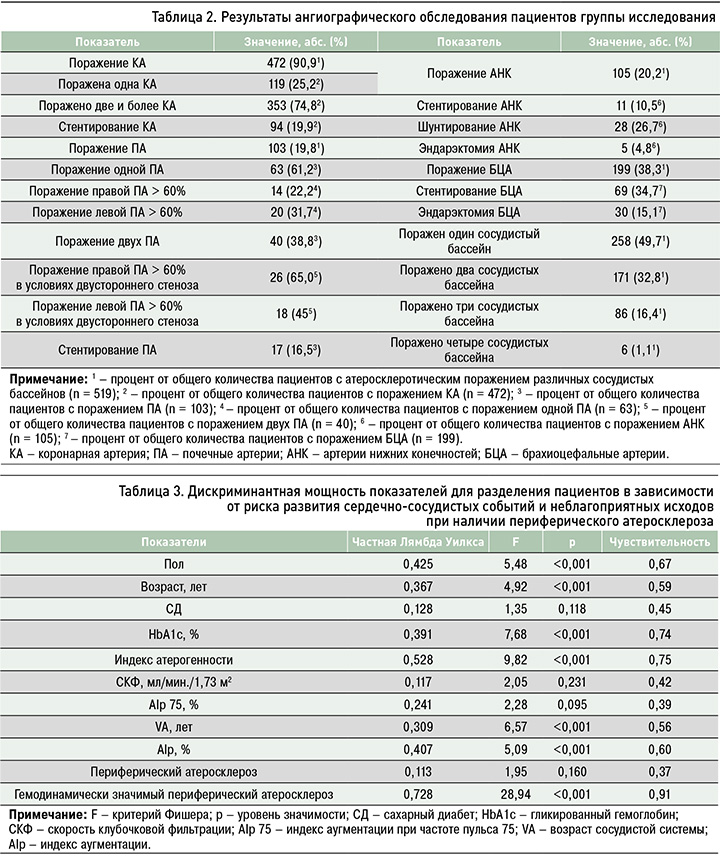
В ходе проспективного этапа исследования данных установлено, что у 126 (28,9%) пациентов в течение трех лет отмечались сердечно-сосудистые или иные события, причем у 44 (10,1%) больных представленные эпизоды носили фатальный характер.
Сосудистое событие в течение первого года после госпитализации отмечалось у 12 (9,6%), в течение 2 лет – у 61 (48,4%), в течение 3 лет – у 53 (42,1%) человек.
Конечные точки, встречавшиеся у больных группы исследования:
- инсульт – у 27 (6,1%) пациентов, в том числе нефатальный у 17 (4,1%) и фатальный у 10 (2,0%) человек;
- транзиторная ишемическая атака – у 15 (3,4%) лиц;
- инфаркт миокарда – у 47 пациентов (10,9%), в том числе нефатальный у 19 (4,8%) и фатальный у 28 (6,1%) больных;
- госпитализация по причине стенокардии – у 13 участников (2,9%);
- развитие сердечной недостаточности – 14 (3,2%) пациентов, в том числе нефатальной у 11 (2,5%) и фатальной у 3 (0,7%) человек;
- хроническая болезнь почек – у 11 (2,1%) больных, в том числе нефатальная у 8 (1,5%) и фатальной у 3 (0,6%) лиц.
Статистический анализ полученных результатов проводился с помощью пакетов прикладных статистических программ Microsoft Office Excel 2010 (Microsoft Corp., США) и Statistica 10.0 (StatSoft Inc., США). Использовался метод построения обобщенных линейных моделей GLM (Generalized Linear Models) с пошаговым включением предикторов.
При построении модели методом «Пошаговый с включением» на каждом этапе в модель добавлялись переменные. При анализе полученных статистических отчетов принималось решение об упрощении/усложнении модели. Значимость предикторов оценивалась посредством статистики Вальда и по р-уровню значимости проверки соответствующей гипотезы (менее 5%). Коэффициент множественной детерминации отражал меру зависимости риска развития фатальных сердечно-сосудистых событий и неблагоприятных исходов от предиктора при учете множества других. Скорректированный коэффициент детерминации рассчитывался с учетом числа факторов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
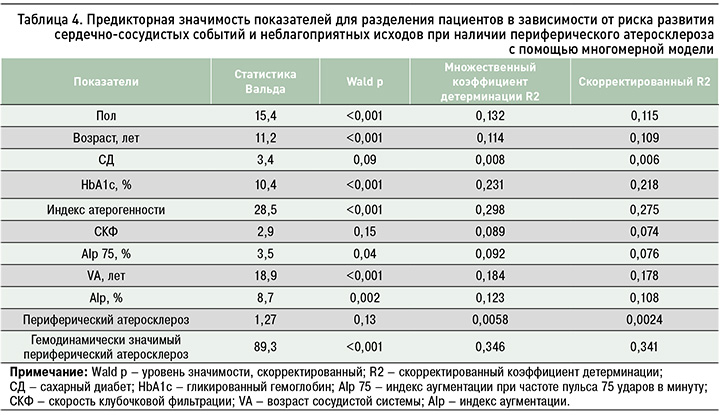
При разработке калькулятора на основании клинико-инструментальных данных 195 пациентов группы исследования анализировалось влияние 11 факторов для разделения участников по риску фатальных сердечно-сосудистых событий: пола, возраста, наличия СД, значений гликированного гемоглобина, индекса атерогенности, скорости клубочковой фильтрации, AIр, AIp 75, VA, наличия периферического атеросклероза, гемодинамически значимого периферического атеросклероза (табл. 3) [15].
Наиболее выраженной прогностической значимостью для оценки определяемого в работе сердечно-сосудистого риска обладали такие факторы, как наличие гемодинамически значимого периферического атеросклероза, величина индекса атерогенности, гликированного гемоглобина, пол больных и возраст, биологический сосудистый возраст и индекс аугментации. Коэффициент множественной детерминации при таком комплексировании факторов был наибольшим. Представленные факторы были включены далее и в многомерную регрессионную модель (табл. 4) [15].
Калькулятор оценки риска сердечно-сосудистых событий и неблагоприятных исходов был разработан с помощью метода бинарной логистической регрессии. Учитывались результаты обследования 195 пациентов с периферическим атеросклерозом, из них фатальные и нефатальные сердечно-сосудистые события и неблагоприятные исходы в течение трех лет развились у 45 человек (ранжировано как «1»), а у 150 они отсутствовали (ранжировано как «0»).
Полученное математическое выражение для расчета величины вероятности развития сердечно-сосудистых событий и неблагоприятных исходов (Z) имело следующий вид:
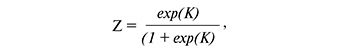
где К – линейная комбинация предикторов и коэффициентов.
Значение K, в свою очередь, рассчитывалось по формуле:
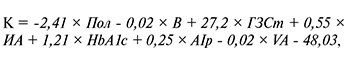
где Пол – ранг пола (1 – мужской, 0 – женский); В – возраст пациента в годах; ГЗСт – наличие гемодинамически значимого стеноза (1/0); ИА – индекс атерогенности; HbA1с – гликированный гемоглобин (%); Alp – индекс аугментации (%); VA – биологический сосудистый возраст (годы).
Коэффициенты и постоянная были получены методом логистической регрессии при анализе результатов обследования опытной выборки из 195 пациентов.
По результатам ROС-анализа при превышении значения Z > 0,29 с диагностической чувствительностью 93,75% и диагностической специфичностью 93,41% делался вывод о высоком риске развития сердечно-сосудистых событий и неблагоприятных исходов (рис.).
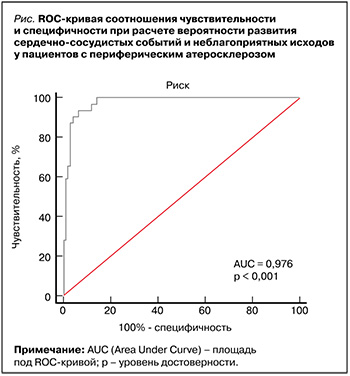
Разделительная точка для переменной Z, равная 0,29, соответствовала максимальной диагностической чувствительности и специфичности.
Площадь под кривой ROС (AUС) соответствовала 0,976 ± 0,0155 (доверительный интервал: 0,931–0,995) и свидетельствовала об отличном качестве разделения пациентов на два класса по включенным переменным в модели. ROС-кривая статистически значимо отличалась от опорной диагональной линии (z = 41,539 при р < 0,001).
Для автоматизированного расчета индивидуального значения величины Z у пациентов и формирования заключения о выраженности сердечно-сосудистого риска на базе табличного процессора Еxсеl было создано окно расчета (табл. 5).
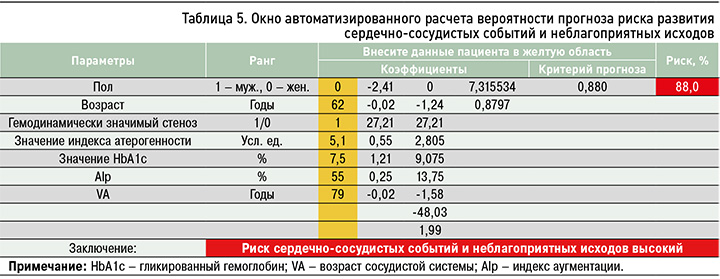
Индивидуальные значения больного вносили в область желтого цвета и по разработанной нами формуле автоматически рассчитывали риск развития сердечно-сосудистых событий и неблагоприятных исходов, а также знакомились с качественной оценкой риска.
В разработанном калькуляторе такие факторы, как пол, паспортный возраст, биологический сосудистый возраст, индекс аугментации как критерий жесткости стенки аорты, являются немодифицируемыми и определяют фоновое значение риска. Индекс атерогенности и величина HbA1c относятся к модифицируемым факторам. Пациенты при высоком риске развития сердечно-сосудистых событий и неблагоприятных исходов должны быть мотивированы на активную гиполипидемическую и сахароснижающую терапию с обязательным мониторингом лабораторных показателей.
Если же у пациента при высокой вероятности развития кардиоваскулярных событий и неблагоприятных исходов в процессе лечения не происходит необходимой модификации факторов риска с помощью выбранной терапевтической стратегии, то в качестве практической рекомендации формируется относительное показание к проведению хирургической реваскуляризации в области гемодинамически значимого стеноза периферических артерий.
Разработанная регрессионная модель определения риска развития сердечно-сосудистых событий и неблагоприятных исходов относится к нелинейным. Отрицательный знак коэффициентов перед рангом пола, возраста и биологическим сосудистым возрастом указывает на то, что чаще гемодинамически значимые стенозы артерий в выборке пациентов наблюдались у мужчин среднего возраста, когда биологический сосудистый возраст не имел высоких значений. Однако наличие корректирующей постоянной (-48,03) при расчете величины К (уравнение линейной комбинации предикторов), нелинейной логарифмической связи между переменными Z и К корректировалось тем, что при анализе одномерного влияния пола, возраста и биологического сосудистого возраста были получены иные закономерности.
Методом ROС-анализа для каждого предиктора в модели были установлены критические точки разделения, при превышении которых риск развития сердечно-сосудистых событий и неблагоприятных исходов резко возрастал. Это женский пол, возраст старше 62 лет, наличие гемодинамически значимого периферического атеросклероза, величина индекса атерогенности > 5,1, гликированного гемоглобина > 7,5%, биологический сосудистый возраст > 70 лет, индекс аугментации > 51,3% (табл. 6) [15].
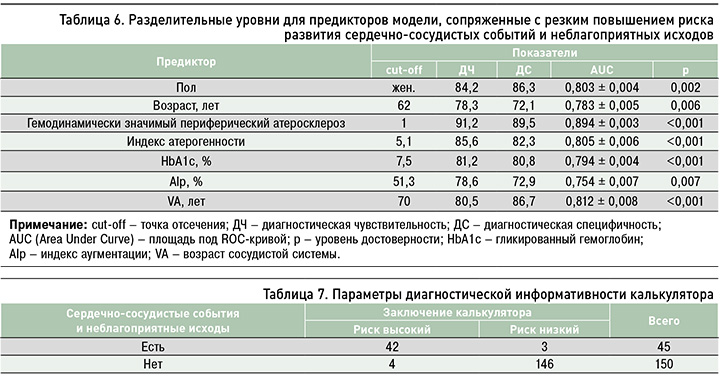
С точки зрения возможности модификации риска развития сердечно-сосудистых событий и неблагоприятных исходов наиболее значимым оказались такие факторы, как наличие гемодинамически значимого периферического атеросклероза, повышение величины индекса атерогенности и HbA1с.
Следовательно, калькулятор имел наибольший прогностический потенциал у мужчин младше 62 лет при значениях биологического сосудистого возраста ниже 70 лет.
Апробация калькулятора на изучаемой выборке пациентов при их долгосрочном проспективном наблюдении показала, что среди 45 пациентов с подтвержденными сердечно-сосудистыми событиями и неблагоприятными исходами в отдаленном периоде у 42 больных кардиоваскулярный риск был высоким, а среди пациентов с отсутствием сосудистых событий низкий риск подтвердился у 146 из 150 человек (табл. 7).
Такое распределение показателей определило следующие фактические характеристики модели: диагностическая чувствительность – 85,5%, диагностическая специфичность – 96,7%, диагностическая точность – 94,3%, прогностическая ценность положительного результата – 90,32%, прогностическая ценность отрицательного результата – 95,65%.
Полученные результаты наглядно демонстрируют возможность применения разработанного калькулятора в реальной клинической практике для оценки риска развития сердечно-сосудистых событий и неблагоприятных исходов у пациентов с периферическим атеросклерозом.
ЗАКЛЮЧЕНИЕ
Клинические руководства традиционно рекомендуют относить всех пациентов с установленным сосудистым заболеванием к группе очень высокого риска. Однако игнорируется тот факт, что индивидуальный уровень риска сердечно-сосудистых событий у таких пациентов может различаться, что исключает возможность более персонализированного подхода к управлению факторами риска при вторичной профилактике [16].
Большинство пациентов с установленными атеросклеротическими сердечно-сосудистыми заболеваниями подвержено очень высокому риску рецидивирующих событий. Поскольку обсуждаемый риск значительно варьирует, необходимо определить ту группу лиц, у которой следует рассмотреть более интенсивную стратегию вторичной профилактики.
В ходе исследования нами был разработан калькулятор оценки риска сердечно-сосудистых событий и неблагоприятных исходов в отдаленном периоде у пациентов с периферическим атеросклерозом, учитывающий модифицируемые и немодифицируемые факторы риска и позволяющий с высокой точностью прогнозировать вероятность развития неблагоприятного сердечно-сосудистого эпизода. В алгоритм оценки отдаленного прогноза включены факторы с наибольшей прогностической значимостью: наличие гемодинамически значимого периферического атеросклероза, величина индекса атерогенности, HbA1с, пол, возраст, биологический сосудистый возраст пациента и AIр.
Выделим ряд аспектов, подчеркивающих потенциальную ценность разработанного калькулятора прогнозирования риска сердечно-сосудистых событий и неблагоприятных исходов. Несмотря на то что всех включенных в наше исследование пациентов следует расценивать как лиц с высоким уровнем сердечно-сосудистого риска, в то же время оправдан персонализированный подход к таким больным с целью снижения вероятности неблагоприятного отдаленного прогноза. Например, лицам с наименьшим риском может быть предложена программа вторичной профилактики и реабилитации на дому, тогда как как больные с высоким риском могут быть кандидатами на получение более специализированных услуг по профилактике и реабилитации в медицинских учреждениях. Калькулятор, информирующий пациентов о вероятности развития неблагоприятного сердечно-сосудистого события, также акцентирует их внимание на необходимости придерживаться адекватной терапевтической стратегии. В рамках дальнейшей разработки темы предлагается проведение многоцентрового исследования для апробации алгоритма прогнозирования кардиоваскулярных событий у пациентов с периферическим атеросклерозом. Представляется целесообразным расширение рассмотренного прогностического алгоритма путем углубленного изучения и последующего включения в него дополнительных факторов, которые могли бы быть использованы в новых системах оценки сердечно-сосудистого риска.



