Подагра – системное заболевание, при котором в различных тканях откладываются кристаллы моноурата натрия, и на фоне гиперурикемии развивается воспаление, обусловленное экзогенными и/или генетическими факторами. Основным органом-мишенью являются почки [1, 2]. Недостаточно изучен вопрос дисфункции мочевыделительной системы при подагре. Актуален поиск методов ранней диагностики нарушений функции почек и мочевых путей у больных со сложным преморбидным фоном. Ниже представлены возможности радионуклидной функциональной диагностики – технологии системной экспертизы нефроурологического состояния на базе комплексной реносцинтиграфии (СЭНС-КР) [3, 4].
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Больная П., 71 год, 05.02.2018 поступила в терапевтический стационар с жалобами на боль и припухлость I плюснефалангового сустава (ПФС) правой стопы, периодически возникающие головокружения, повышение артериального давления (АД) до 160/90 мм рт.ст.
Данные анамнеза: диагноз подагры установлен в июле 2016 г., когда у больной развился острый артрит 1 правого ПФС, разрешившийся самостоятельно. В декабре 2016 г. острый артрит возник повторно и держался 2 нед, в январе 2018 г. произошел еще один 2-недельный рецидив. Пациентка принимала нимесулид (по 200 мг) во время приступа, аллопуринол (по 50 мг), придерживалась назначенной диеты. У ревматолога наблюдалась периодически.
В течение многих лет больная страдает хроническим гломерулонефритом (инвалидность присвоена в 32 года) и артериальной гипертензией (частые подъемы АД до 160/90 мм рт.ст., головная боль, головокружение, тошнота); адаптирована к АД 130/80 мм рт.ст. Последние 15 лет постоянно пользуется гипотезивными препаратами с мочегонными свойствами (гидрохлоротиазид, эпизодически фуросемид). У нефролога наблюдалась нерегулярно. Наследственность не отягощена. Лекарственной аллергии и вредных привычек не отмечено.
При осмотре отмечено удовлетворительное состояние пациентки, нормостеническая конституция, повышенная упитанность. Рост 164 см, вес 82 кг. В легких дыхание везикулярное, хрипов нет, частота дыхания 18 в минуту. Тоны сердца приглушены, ритм правильный, пульс 84 в минуту, АД 155/90 мм рт.ст. Живот увеличен в объеме за счет избыточного развития подкожной жировой клетчатки, при пальпации мягкий, безболезненный. Край печени не выступает из-под реберной дуги. Размеры печени по Курлову: 10 × 8 × 7 см. Селезенка не увеличена. Стул в норме. Область почек визуально не изменена. Симптом поколачивания отрицательный с обеих сторон. Мочеиспускание учащено до 10–15 раз/сут, никтурия (3–4 раза за ночь). Выявлена пастозность нижней трети голеней и стоп. Щитовидная железа не увеличена. Неврологический статус без особенностей. Отмечена болезненность I ПФС правой стопы, небольшое ограничение движений.
Лабораторно-инструментальное обследование: в анализах крови гемоглобин снижен до 101 г/л, эритроциты до 3 × 1012/л. Повышены следующие показатели: скорость оседания эритроцитов (СОЭ) – до 35 мм/ч, мочевая кислота – до 466 мкмоль/л, креатинин – до 138 мкмоль/л, мочевина – до 7,5 ммоль/л. Данные общего анализа мочи: удельный вес – 1010, глюкоза – нет, белок – 0,344 г/л, лейкоциты – 1–2 в поле зрения. В анализе мочи по Зимницкому выявлено снижение плотности мочи от 1005 до 1012 мл. Результаты пробы Реберга: клубочковая фильтрация снижена до 35 мл/мин, канальцевая реабсорбция – 98%; скорость клубочковой фильтрации (СКФ) по CKD-EPI – 33 мл/мин/1,73м2; IIIb стадия хронической болезни почек (ХБП). Данные сонографии почек: левая почка – паренхима 12 мм, правая – 13 мм; в чашечно-лоханочной системе (ЧЛС) обеих почек – депозиты мочевой кислоты (до 4–10 мм), кисты до 10–14 мм. Консультация уролога: данных в пользу острой урологической патологии нет, рекомендовано наблюдение нефролога.
Проведено исследование функции почек с 99mTc-технефором в рамках технологии СЭНС-КР на 2-детекторной γ-камере (рис. 1).
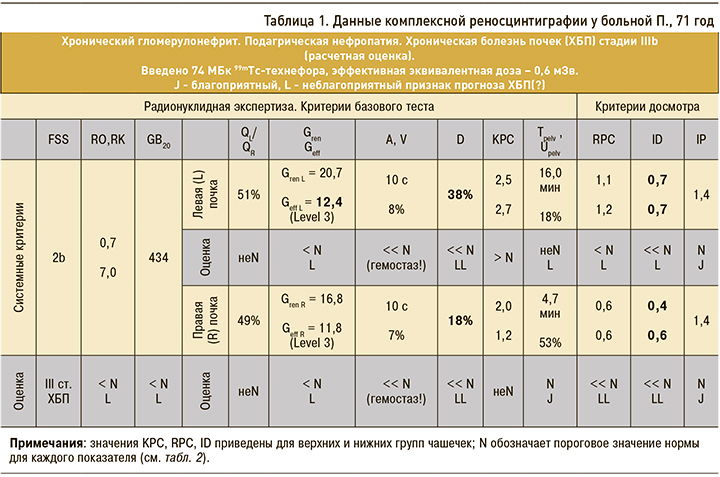
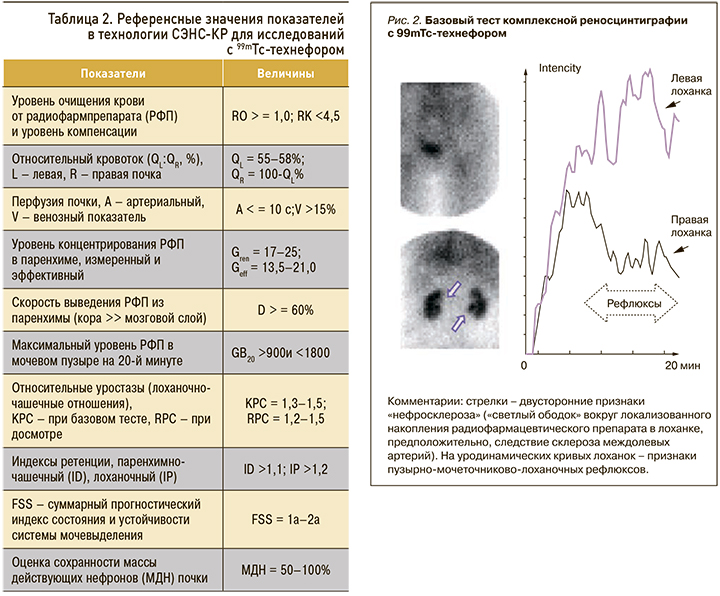
Относительный почечный кровоток дисфункционально симметричен: в левую почку поступает 51%, в правую – 49%. Выраженные двусторонние относительные гемостазы (A–V) – признаки возможного отека паренхимы почек. Умеренно сниженная концентрационная функция почек (Gren, Geff), выраженные застойные явления в паренхиме и чашечках (D, ID) указывают на существенно сниженный ренальный резерв (табл. 1, 2).
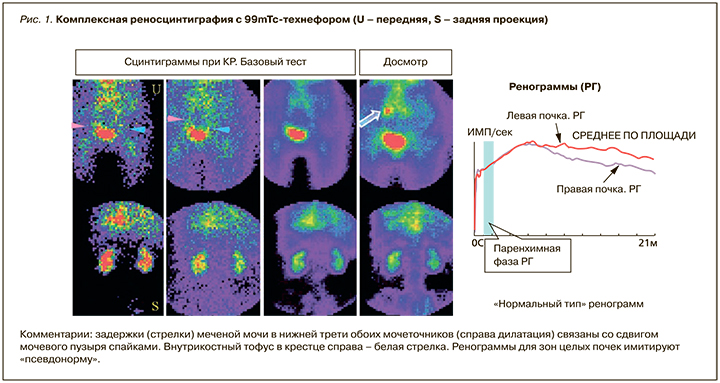
В то же время у больной сохранен уродинамический резерв выведения из лоханок (IP) на фоне рефлюкс-аритмии (рис. 2). Выявленная функциональная пиелоэктазия (КРС >2) и признаки гемостазов в почках складываются в картину вероятного обострения латентной инфекции мочевых путей, протекающей на фоне полиурии клинически бессимптомно, что характерно для пожилых людей. Суммарная функция почечного очищения крови (FSS, RO-RK, GB20) у больной П. снижена умеренно со сдвигом к значительной степени, имеется неустойчивая компенсация (см. табл. 1, 2). В этих условиях важен контроль и своевременное лечение нарушений оттока в мочевыводящей системе с назначением противовоспалительной терапии и спазмолитических препаратов.
По результатам обследования у больной П. сформулирован заключительный диагноз «подагра, хроническое течение, тофусная форма. Подагрическая нефропатия. ХБП IIIb стадии. Хронический гломерулонефрит. Вторичная артериальная гипертензия 2 степени. Риск 3 (высокий). Ожирение I степени».
Проведено лечение: диклофенак (при болях), аллопуринол, эналаприл, дротаверин. Рекомендована диета, ежедневный прием эналаприла по 20 мг, гидрохлоротиазида по 12,5 мг, аллопуринола по 100 мг. Рекомендовано дальнейшее наблюдение у специалистов по месту жительства: нефролога, уролога, ревматолога.
ОБСУЖДЕНИЕ
Как только установлен диагноз подагры, пациентам необходим скрининг ХБП; при ее подтверждении важно контролировать факторы риска, связанные с вероятностью ее прогрессирования. Отсутствие в клинике эффективных средств слежения за состоянием мочевыводящей системы приводит, на наш взгляд, к недооценке функциональных нарушений ренальной паренхимы и оттока из чашечно-лоханочной системы при ведении пациентов с риском развития ХБП. Развернутый дифференцированный анализ по данным комплексной реносцинтиграфии позволил выявить существенные потери ренального резерва, спектр устойчивых (даже на фоне лекарственной полиурии) уродинамических нарушений у больной П., признаки развития нефросклероза. Почечные резервы снижены при наличии ХБП стадии IIIb, повышен риск дальнейшего развития заболевания. Неучтенные вовремя или недолеченные нарушения со стороны мочевых путей могут значительно осложнять работу паренхимы и ускорять развитие более тяжелой стадии ХБП [5, 6].
ЗАКЛЮЧЕНИЕ
Представленный пример показывает, насколько важен системный подход при диагностике нарушений суммарной функции почечного очищения крови, концентрационной функции паренхимы почек, развития нефросклероза, устойчивых задержек оттока в мочевыводящей системе и обострения инфекции мочевых путей у больных хронической тофусной подагрой. Технология СЭНС-КР позволяет своевременно выявлять обострение инфекции мочевых путей или высокую предрасположенность к ней, способствуя предупреждению или замедлению развития ХБП. Эта радионуклидная технология восполнила недостаток в клинике средств углубленного контроля над функцией мочевыводящей системы, обеспечила для пациента, регулярно получавшего лечение по поводу подагры, объективные показания к лечению и динамическому наблюдению не только у ревматологов, но и у нефрологов, урологов.



