ВВЕДЕНИЕ
Аллергический ринит (АР) – заболевание, характеризующееся IgE-опосредованным воспалением слизистой оболочки полости носа (которое развивается под действием аллергенов) и наличием ежедневно проявляющихся в течение часа и более хотя бы двух из следующих симптомов: заложенности (обструкция) носа, выделений из носа (ринорея), чихания, зуда в полости носа. АР часто сочетается с другими аллергическими заболеваниями, такими как аллергический конъюнктивит, атопический дерматит, бронхиальная астма (БА) [1, 2]. Распространенность АР в разных странах мира составляет 4–32%, в России – 10–24%. У 15–38% пациентов с этим заболеванием одновременно выявляется БА. В то же время 55–85% больных БА отмечают симптомы АР [1–11].
Несмотря на то что АР не относится к числу тяжелых, жизнеугрожающих заболеваний, его медико-социальное значение достаточно значимо и связано с высокой распространенностью, снижением качества жизни пациентов, частым сочетанием с синуситом, отитом, БА. Это определяет необходимость своевременной диагностики АР и проведения адекватной терапии, соответствующей степени тяжести заболевания.
К основным целям терапии АР относятся устранение симптомов, достижение и поддержание контроля заболевания, снижение риска развития осложнений, повышение качества жизни. Для лечения АР, согласно клиническим рекомендациям, могут применяться глюкокортикостероиды (ГКС) (интраназальные и системные), блокаторы Н1-гистаминовых рецепторов 2-го поколения и их активные метаболиты (интраназальные и системные), антагонисты лейкотриеновых рецепторов, назальные деконгестанты, интраназальные кромоны, омализумаб [1, 2]
Лечение АР подразумевает комплексный ступенчатый подход, при выборе терапии учитывается степень тяжести заболевания, преобладающие симптомы и их выраженность, индивидуальные социальные, психологические особенности и предпочтения пациента, сопутствующая патология. Также необходимо помнить, что, кроме рациональной фармакотерапии, важную роль в лечении АР, как и других аллергических заболеваний, играют элиминационные мероприятия, аллерген-специфическая иммунотерапия, образовательные программы (табл. 1) [1, 2].
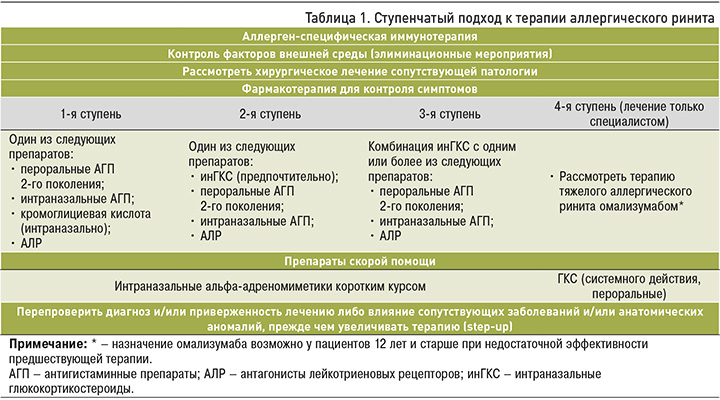
Антагонисты Н1-гистаминовых рецепторов 2-го поколения, или неседативные антигистаминные препараты (АГП) и антагонисты лейкотриеновых рецепторов (АЛР) являются одними из базисных средств для лечения АР. В данной статье обобщены имеющиеся к настоящему времени данные о перспективной терапевтической стратегии при сезонном и круглогодичном АР – применении фиксированной комбинации, включающей АГП 2-го поколения левоцетириин и АЛР монтелукаст.
ГИСТАМИН И ЛЕЙКОТРИЕНЫ КАК МЕДИАТОРЫ АЛЛЕРГИЧЕСКОГО ВОСПАЛЕНИЯ ПРИ АЛЛЕРГИЧЕСКОМ РИНИТЕ
Гистамин играет центральную роль как в ранней, так и поздней фазе аллергического воспаления. Высвобождение его происходит в результате дегрануляции тучных клеток и базофилов, а эффекты при АР реализуются через взаимодействие с Н1-гистаминовыми рецепторами, широко представленными в разных органах и тканях. Результатом этого взаимодействия становится повышение проницаемости сосудов и отек ткани, сокращение гладкой мускулатуры, гиперсекреция слизистых желез, раздражение периферических нервных окончаний, усиление секреции провоспалительных цитокинов, таких как интерлейкин 1-альфа (ИЛ-1-альфа), ИЛ-1-бета, ИЛ-6, фактор некроза опухоли-альфа, простагландины, лейкотриены, хемокины. Гистамин также регулирует функции моноцитов, Т- и В-лимфоцитов, макрофагов, нейтрофилов, эозинофилов и дендритных клеток, усиливает секрецию ИЛ-5, ИЛ-4, ИЛ-13 Th-2 лимфоцитами [12, 13].
Лейкотриены (ЛТ) – липидные медиаторы воспаления, которые являются продуктами метаболизма арахидоновой кислоты через 5-липооксигеназный путь. Бóльшая часть биологических эффектов ЛТ, участвующих в патогенезе АР, осуществляется через активацию специфических цис-ЛТ1-рецепторов, расположенных на тучных клетках, моноцитах и макрофагах, эозинофилах, базофилах, нейтрофилах, Т- и В-лимфоцитах, гладкомышечных клетках, бронхиальных фибробластах и эндотелиальных клетках. Активация этих рецепторов при АР стимулирует продукцию ИЛ-4 и ИЛ-13, вызывает гиперсекрецию слизи, повышение проницаемости сосудов и отек слизистой оболочки полости носа, миграцию эозинофилов [14–18]. Важно, что провоспалительные эффекты ЛТ недостаточно контролируются ГКС, в связи с чем для их подавления необходимо использовать АЛР [19].
ЛЕВОЦЕТИРИЗИН И МОНТЕЛУКАСТ В ЛЕЧЕНИИ АЛЛЕРГИЧЕСКОГО РИНИТА
Левоцетиризин – активный энантиомер цетиризина, селективный антагонист Н1-гистаминовых рецепторов. Это лекарственное средство характеризуется высоким сродством и избирательностью к данному типу рецепторов, быстрым началом действия и достаточной длительностью основного эффекта. В большом числе клинических исследований доказаны эффективность и хорошая переносимость левоцетиризина при АР, положительная динамика на фоне его приема таких проявлений заболевания, как назальная обструкция, ринорея, зуд в носу, пароксизмы чихания. На основании этого левоцетиризин рекомендован для лечения сезонного и круглогодичного АР. Есть данные о преимуществе левоцетиризина в сравнении с другими АГП 2-го поколения с точки зрения более быстрого купирования основных симптомов АР и большей длительности действия [20–25].
Монтелукаст – наиболее изученный и наиболее часто применяемый препарат группы АЛР с оптимальным профилем эффективности и безопасности. Он эффективно воздействует на эозинофильное воспаление, способствует уменьшению эозинофилии крови и слизистой оболочки дыхательных путей, снижает выраженность симптомов АР [26, 27]. Показано, что применение монтелукаста у пациентов с АР и БА приводит к значимому улучшению течения обоих заболеваний по сравнению с плацебо [28]. Имеются основания полагать, что это лекарственное средство обладает расширенным спектром противовоспалительной активности ввиду задействования дополнительных механизмов, не связанных с блоком ЛТ-рецепторов [29].
Лечение АР среднетяжелого и тяжелого течения предполагает использование различных комбинаций лекарственных препаратов. В целях совершенствования фармакотерапии АР представляется рациональным применение фиксированной комбинации двух эффективных противоаллергических препаратов с разным механизмом действия – левоцетиризина и монтелукаста. При этом необходимо иметь в виду, что к фиксированной комбинации лекарственных средств предъявляется ряд требований: синергизм фармакодинамики и взаимодополняющее действие активных веществ, усиление основного эффекта, фармакокинетическая совместимость компонентов, сохранение благоприятного профиля безопасности.
ЭФФЕКТИВНОСТЬ И БЕЗОПАСНОСТЬ ФИКСИРОВАННОЙ КОМБИНАЦИИ ЛЕВОЦЕТИРИЗИН/МОНТЕЛУКАСТ ПРИ АЛЛЕРГИЧЕСКОМ РИНИТЕ
Высокая эффективность комбинации монтелукаста с различными АГП 2-го поколения у пациентов с АР продемонстрирована в ряде исследований [30–32]. В нескольких клинических испытаниях изучена и фиксированная комбинация левоцетиризина с монтелукастом. Так, в исследовании Bylappa K.В. et al. (2018) положительная динамика субъективных ощущений на фоне ее применения (монтелукаста 10 мг/левоцетризин 5 мг) была зарегистрирована у 95,1% пациентов с сезонным АР, тогда как в группе монотерапии монтелукастом (10 мг) этот показатель составил лишь 86,5%, а в группе монотерапии левоцетризином (5 мг) – 88% [33]. Еще в одном рандомизированном двойном слепом плацебо-контролируемом перекрестном исследовании были продемонстрированы преимущества применения монтелукаста с дезлоратадином или левоцетиризином для лечения персистирующего АР. Комбинированное лечение (монтелукаст/АГП) сопровождалось более выраженным улучшением назальных симптомов АР, более значительным снижением уровня эозинофильного катионного белка, чем монотерапия этими препаратами. При этом эффективность комбинации монтелукаста с левоцетиризином была выше по сравнению с комбинацией монтелукаста с дезлоратадином [31].
Gupta V. et al. (2010) провели 6-недельное клиническое исследование эффективности фиксированной комбинации левоцетиризин/монтелукаст (основная группа) в сравнении с монотерапией левоцетиризином (контрольная группа) у больных АР. В нем были получены данные о значимом уменьшении выраженности дневных и ночных назальных симптомов в основной группе по сравнению с контролем. В обеих группах отмечались такие побочные эффекты, как тошнота, головокружение, головная боль, сонливость, сухость во рту, лихорадка и слабость, но все они были нетяжелыми и не послужили причиной отмены терапии [34].
Одной из целевых категорий пациентов для проведения комбинированной терапии АГП и АЛР являются пациенты с АР и БА. Фиксированная комбинация монтелукаста и левоцетиризина оказалась более эффективной и безопасной при лечении круглогодичного АР у пациентов с БА по сравнению с одним монтелукастом. Было установлено положительное влияние комбинации левоцетиризина и монтелукаста на ингибирование как ранней, так и поздней фазы реакций при АР. При этом статистически значимое улучшение, по сравнению с исходным уровнем, средней дневной оценки носовых симптомов в течение 2-недельного периода лечения в группе, применявшей фиксированную комбинацию, отмечалось быстрее, чем в группе, получавшей только монтелукаст. Авторы констатировали хорошую переносимость монтелукаста/левоцетиризина и высокий профиль безопасности терапии, который был аналогичен таковому в группе, получавшей только монтелукаст [35].
СРАВНИТЕЛЬНАЯ ФАРМАКОКИНЕТИКА ЛЕВОЦЕТИРИЗИНА И МОНТЕЛУКАСТА
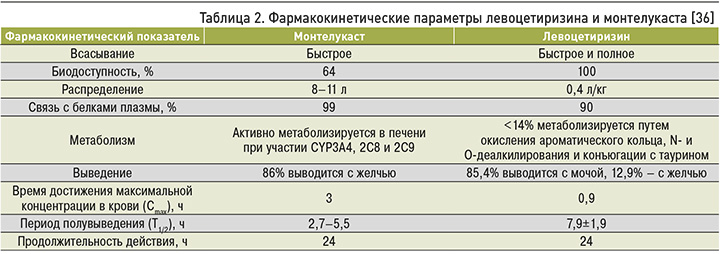
Основные фармакокинетические параметры левоцетиризина и монтелукаста сопоставимы и позволяют объединить эти лекарственные средства в одной лекарственной форме. Сравнительная фармакокинетика левоцетиризина и монтелукаста у взрослых пациентов представлена в таблице 2.
ПРЕПАРАТ МОНТРАЛ МЛ – ФИКСИРОВАННАЯ КОМБИНАЦИЯ ЛЕВОЦЕТИРИЗИНА И МОНТЕЛУКАСТА В ЛЕЧЕНИИ АЛЛЕРГИЧЕСКОГО РИНИТА
Препарат Монтрал МЛ представляет собой фиксированную комбинацию, содержащую левоцетиризин 5 мг и монтелукаст 10 мг. Показанием к применению препарата Монтлар МЛ (левоцетиризин 5 мг + монтелукаст 10 мг) является лечение сезонного (интермиттирующего) и круглогодичного (персистирующего) АР у взрослых и детей старше 15 лет.
В 2021 г. были опубликованы результаты сравнительного клинического исследования эффективности и безопасности препарата Монтрал МЛ и монотерапии левоцетиризином 5 мг у пациентов с АР и конъюнктивитом, вызванным сенсибилизацией к аллергенам пыльцы сложноцветных трав. При применении препарата Монтрал МЛ было зарегистрировано статистически достоверное среднее улучшение назальных и конъюнктивальных симптомов, а также более высокая эффективность контроля течения заболевания в сравнении с монотерапией левоцетиризином 5 мг (p <0,05). Наряду с этим была показана способность препарата Монтрал МЛ достоверно (p <0,05) снижать число эозинофилов в периферической крови и в мазке из полости носа, уменьшать миграцию эозинофилов, ограничивать высвобождение медиаторов воспаления, снижать концентрацию эозинофильного катионного белка в сыворотке крови в сравнении с левоцетиризином 5 мг [37].
ЗАКЛЮЧЕНИЕ
Рациональная терапия больных АР остается актуальной проблемой ввиду широкой распространенности и медико-социальной значимости этого заболевания. Одним из возможных путей совершенствования фармакотерапии АР можно считать применение фиксированной комбинации левоцитиризин/монтелукаст 5 мг/10 мг (препарат Монтлар МЛ). Препарат применяется по 1 таблетке 1 раз/сут, что является важным фактором повышения приверженности пациентов терапии. Результаты клинических исследований свидетельствуют о более значимом контроле симптомов АР у пациентов, получавших фиксированную комбинацию левоцетиризин/монтелукаст 5 мг/10 мг, по сравнению с пациентами, получавшими монотерапию монтелукастом 10 мг или левоцетиризином 5 мг. Это позволяет рассматривать препарат Монтрал МЛ в качестве компонента перспективной стратегии лечения АР, в том числе у коморбидных пациентов, имеющих сочетание этого заболевания с БА.



