ВВЕДЕНИЕ
Баланс между потоками ионов калия и натрия является принципиальным условием выживания и нормального функционирования клеток всех типов. Ионы калия принципиально необходимы для функционирования миоцитов и, в частности, гладкой мускулатуры сосудов и миокарда и для поддержания баланса вегетативной нервной системы [1]. Поэтому адекватная обеспеченность организма калием чрезвычайно важна для нормофизиологического функционирования организма.
Наиболее точным способом оценки состояния калиевого гомеостаза и установления у пациента недостаточности калия является измерение уровней калия в таких биосубстратах пациента, как цельная кровь, плазма крови (ПК), эритроциты (ЭР), моча и др. Однако клинико-лабораторная диагностика недостаточности калия является достаточно инвазивной процедурой, требует определенных затрат времени и средств.
Для более грубых оценок обеспеченности калием используются опросники диеты и/или балльные клинические шкалы. Использование балльных клинических шкал обосновано тем, что с недостаточностью калия ассоциированы различные клинические симптомы и прежде всего астения [3].
Астени́я (от др.-греч. ασθένεια — бессилие) — болезненное состояние, известное также как синдром хронической усталости. Астения (диагноз R53 по МКБ-10) проявляется повышенной утомляемостью и истощаемостью с крайней неустойчивостью настроения, ослаблением самообладания, нарушениями сна, утратой способности к длительному умственному и физическому напряжению, непереносимостью громких звуков, яркого света, резких запахов. Астения провоцируется в любом возрасте, в том числе и в молодом, в ответ на чрезмерную нагрузку на фоне неадекватного питания и нарушенного режима отдыха [4]. Отличительной чертой астении являются жалобы пациента именно на утомляемость, мышечную слабость, низкую умственную и физическую работоспособность. Ее дифференцируют от соматоформных расстройств, где в клинической картине преобладают жалобы на то или иное заболевание (гастрит, синдром раздраженной кишки, головная боль и т.д.).
Астения связана со снижением адаптационных резервов организма в любом возрасте. Казалось бы, в молодом возрасте адаптационные резервы должны быть максимальны. Однако это происходит, как правило, только в идеале [5, 6]. Действительно, при правильном планировании рабочего времени, регулярных физических нагрузках и рациональном питании (содержащем нутриенты в количествах, соответствующих хотя бы нижним границам установленных норм [7]) молодые люди способны переносить значительные стрессовые нагрузки (жизнь в общежитии, для студентов период сессии, большая учебная нагрузка) без ущерба для здоровья.
В противном случае у студентов часто развивается так называемый синдром информационной усталости, вегетоневрозы, психоэмоциональное состояние становится неустойчивым, развивается зрительное перенапряжение и т.д. Студенты жалуются на «полное бессилие», причем часто оно сопровождается абнормально низким артериальным давлением. Отметим, что путевки в санаторий/профилакторий наиболее активно востребованы студентами, предъявляющими жалобы на присущие астении выраженную усталость, быструю утомляемость, бессилие, апатию и обморочные состояния. Эти симптомы встречаются чаще у девушек, чем у юношей.

Следует отметить, что астения часто сочетается с хроническим дефицитом калия (диагноз E87.6 «гипокалиемия» по МКБ-10) и магния (диагноз Е61.2 «гипомагнеземия»); низкое артериальное давление связано также с гипонатриемией (диагноз E87.1). Часто роль дефицитов калия и магния недооценивается в терапии и профилактике астении, что значительно затрудняет лечение таких пациентов. Тем не менее дефициты калия и магния не только характеризуются клинической симптоматикой, сходной с астенией (чувство усталости, сохраняющееся даже после сна и отдыха, быстрая утомляемость, нарушения сна, чувство тревоги, подавленность), но и имеют фундаментальное значение для развития гипотонии и астенизации нервной системы [6]. Поэтому анализ клинической симптоматики может позволить в принципе оценивать состояние калий-магниевого гомеостаза пациента.
Основной проблемой с разработкой и применением балльных клинических шкал является, как правило, отсутствие достоверных корреляций между получаемыми балльными оценками и реально измеренными уровнями калия в крови и в других биосубстратах. В настоящей работе представлены результаты построения и верификации клинической балльной шкалы, которую мы назвали «Калий: плазма, эритроциты, моча» (КПЭМ). Использование предлагаемой шкалы позволяет прогнозировать уровни калия в биосубстратах на основе клинической картины состояния пациента. Данная шкала построена с использованием современных методов машинного обучения и анализа биомедицинских данных: комбинаторной теории разрешимости и теории классификации значений признаков [8–13], которые позволяют достигнуть достаточно высокой аккуратности получаемых прогнозов.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование соответствовало этическим стандартам комитетов по биомедицинской этике, разработанным в соответствии с Хельсинской декларацией с поправками от 2000 г. и Правилами клинической практики в РФ от 1993 г. Все наблюдаемые были подробно информированы о проводимом исследовании, его целях, безопасности применения препарата, исходя из данных о его составе. Все добровольцы дали письменное информированное согласие на участие в исследовании.
Выборка пациентов. В исследование вошли 345 пациентов старше 18 лет (50% мужчин). Для каждого из пациентов в базу данных заносились данные антропометрии, динамометрии, фоновая и ортостатическая вариабельность ритма сердца (ВРС), все разделы шкалы стресса ИДИКС (условия и организация труда, субъективная оценка профессиональной ситуации, переживание острого стресса и др.), шкалы оценки вегетососудистой дистонии (шкала астении, тест САН), артериальное давление, общий анализ крови, биохимический анализ крови, общий анализ мочи, анамнез (110 диагнозов по МКБ-10), данные краткого опросника диеты, результаты осмотра состояния кожи и ее придатков, опросник по дефициту магния, опросники дефицитов витаминов, уровни витаминов в плазме крови, данные электроокулометрии и др. Всего для каждого пациента было измерено значение 521 параметра. Пациенты (345 человек) были рандомизированы на 2 группы: «выборку обучения» (на основе которой настраивались веса признаков шкалы КПЭМ, n=170) и «контрольную выборку» (на основе которой верифицировалась шкала КПЭМ, n=175).
Кистевая динамометрия. Измерения проводились с помощью динамометра кистевого ДК-140. Динамометр берут в руку циферблатом внутрь. Руку вытягивают в сторону на уровне плеча и максимально сжимают динамометр. Проводятся по два измерения на каждой руке, фиксируется лучший результат. В норме средние показатели силы правой кисти (если человек правша) у мужчин 35–50 кг, у женщин 25–33 кг, средние показатели силы левой кисти обычно на 5–10 кг меньше. Любой показатель силы обычно тесно связан с объемом мышечной массы, поэтому при оценке результатов динамометрии важно учитывать и «абсолютную» силу (т.е. ту величину, которую показал динамометр), и «относительную», (т.е. отнесенную к массе тела). Относительная сила вычисляется по формуле сила (%) = (сила кисти, кг/масса тела, кг) х 100%. Относительная сила правой руки (у правшей) составляет 65–80% у мужчин и 48–50% у женщин.
 Кардиоинтервалография для определения параметров вегетативной нервной системы. У обследуемых анализировались параметры вегетативной нервной системы на основе анализа ВРС с использованием 12-канального электрокардиографа «Поли-Спектр» («Нейрософт», Иваново) с пакетом специальных программ (версии 2011 г.). Использовались 2 методики: анализ ВРС в покое (в соответствии с Международным Стандартом 1996 г.) и анализ ВРС при проведении ортостатической пробы. Для стандартизации исследований выбрана предпочтительная длительность 5 минут. К регистрации кардиоритмограммы приступали не ранее чем 1,5–2 часа после еды в тихой, затененной комнате с температурой 20–22°С. Перед регистрацией кардиоритмограммы студенты адаптировались в течение 5 минут. Запись осуществлялась в покое (5 минут) и в положении стоя (5 минут). Оценивались общая мощность спектра нейрогуморальной модуляции, уровни вагальных, гуморально-метаболических и симпатических влияний на сердечный ритм, баланс между симпатической и парасимпатической реактивностями вегетативной нервной системы.
Кардиоинтервалография для определения параметров вегетативной нервной системы. У обследуемых анализировались параметры вегетативной нервной системы на основе анализа ВРС с использованием 12-канального электрокардиографа «Поли-Спектр» («Нейрософт», Иваново) с пакетом специальных программ (версии 2011 г.). Использовались 2 методики: анализ ВРС в покое (в соответствии с Международным Стандартом 1996 г.) и анализ ВРС при проведении ортостатической пробы. Для стандартизации исследований выбрана предпочтительная длительность 5 минут. К регистрации кардиоритмограммы приступали не ранее чем 1,5–2 часа после еды в тихой, затененной комнате с температурой 20–22°С. Перед регистрацией кардиоритмограммы студенты адаптировались в течение 5 минут. Запись осуществлялась в покое (5 минут) и в положении стоя (5 минут). Оценивались общая мощность спектра нейрогуморальной модуляции, уровни вагальных, гуморально-метаболических и симпатических влияний на сердечный ритм, баланс между симпатической и парасимпатической реактивностями вегетативной нервной системы.
Определение уровня калия и магния в плазме и в эритроцитах. Лабораторная диагностика уровня магния в эритроцитах проводилась методом абсорбционной спектрофотометрии на полуавтоматическом фотометре «StatFax 1904+» (США). Забор крови осуществлялся из локтевой вены в количестве 3 мл (жгут на руку желательно не накладывать, так как при сильном сдавливании уровень электролитов может быть завышенным вследствие микротравматизации нестойких элементов тканей крови). Кровь на анализ бралась строго натощак с 8:00 до 10:00. Кровь для исследования отбирали в пробирку с гепарином из расчета 5 мг (650 ЕД) на 1 мл крови или 1 капля (0,02 мг) на 5—10 мл крови. Концентрации калия и магния устанавливали по методу внутреннего стандарта (реагенты фирмы «HUMAN», Германия).
Интеллектуальный анализ данных. Был разработан уникальный формализм для нахождения метрических сгущений заданной размерности и выраженности, и создан проблемно-ориентированный формализм, включающий два комплементарных подхода: бинарно-комбинаторный и метрический. Использование метрических карт не только позволило наглядно доказать фундаментальный факт «дефицит магния является патофизиологическим ядром коморбидных патологий», но и систематически рассмотреть весь массив взаимодействий между биомедицинскими параметрами на основе анализа метрических сгущений [8].
 В настоящей работе прогноз уровней калия в плазме крови, эритроцитах и моче производился посредством построения регрессионных моделей с использованием специального пакета программ для комбинаторного анализа разрешимости/регулярности и упомянутого выше анализа метрических сгущений. В результате для уровней калия в каждом из исследованных биосубстратов были получены веса признаков, практическая применимость которых была протестирована на независимой контрольной выборке пациентов (n=175). Подробные описания полученных наборов признаков представлены далее.
В настоящей работе прогноз уровней калия в плазме крови, эритроцитах и моче производился посредством построения регрессионных моделей с использованием специального пакета программ для комбинаторного анализа разрешимости/регулярности и упомянутого выше анализа метрических сгущений. В результате для уровней калия в каждом из исследованных биосубстратов были получены веса признаков, практическая применимость которых была протестирована на независимой контрольной выборке пациентов (n=175). Подробные описания полученных наборов признаков представлены далее.
РЕЗУЛЬТАТЫ
В результате проведенного исследования была получена верифицированная комплексная шкала «Калий: плазма, эритроциты, моча» (КПЭМ) для прогнозирования уровней калия у пациентов. Данная шкала состоит из трех частей для оценки обеспеченности калием: прогнозирование уровней калия в плазме крови (К+(ПК)), прогнозирование уровней калия в эритроцитах (К+(ЭР)), прогнозирование уровней калия в моче (К+(М)).
В табл. 1 представлена первая часть оценки обеспеченности калием по шкале КПЭМ - прогнозирование уровней К+(ПК); в примечании к таблице описан способ применения этой части КПЭМ. Наличие у пациента признаков с положительными значениями весов (артериальное давление в диапазоне нормы, регулярные занятия физкультурой и др.) соответствует лучшей обеспеченности калием организма и более высокому уровню калия в плазме крови. Признаки с отрицательными значениями весов соответствуют преимущественно наличию у пациента состояний, коморбидных с недостаточной обеспеченностью калием (например, наличие у пациента флебита и/или тромбофлебита, ларингита, частых головных болей, судорог и др.), отдельным симптомам дефицита калия (темные круги вокруг глаз, гиперакузия и др.), нарушениям диеты (рафинированные продукты питания), вредным привычкам (ежедневное употребление алкогольных напитков), данным анамнеза (внутриутробная гипоксия, стигмы дизэмбриогенеза и др.).
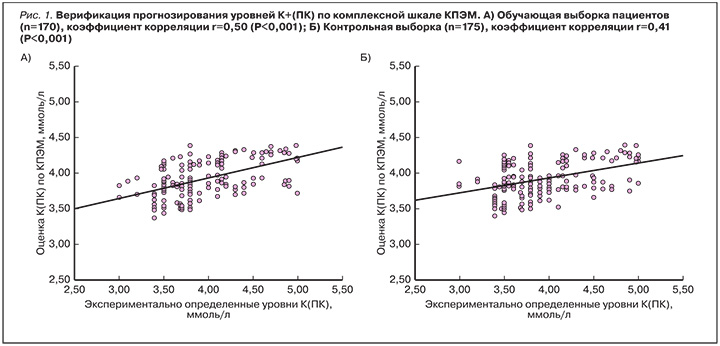
Верификация первой части шкалы КПЭМ с использованием независимой выборки пациентов (pис. 1) показала, что прогнозируемые значения уровней калия в плазме крови находятся в статистически достоверной корреляции с экспериментально определенными уровнями К+(ПК). При этом значения коэффициента корреляции между прогнозируемыми и экспериментальными уровнями К+(ПК) достаточно близки для обучающей (r=0.50) и контрольной (r=0,41) выборок пациентов.
В табл. 2 представлена вторая часть оценки обеспеченности калием по шкале КПЭМ – прогнозирование уровней К+(ЭР); в примечании к таблице описан способ применения этой части шкалы КПЭМ. Наличие у пациента нормотонии, хорошего самочувствия, более высокого результата динамометрии правой руки соответствовало более высоким уровням калия в эритроцитах. Наоборот, наличие у пациента гиперакузии, темных кругов под глазами, судорог икроножных мышц, «симптома прикладывания», иммунодефицита, более старший возраст пациента и другое соответствовали более низким уровням К+(ЭР).
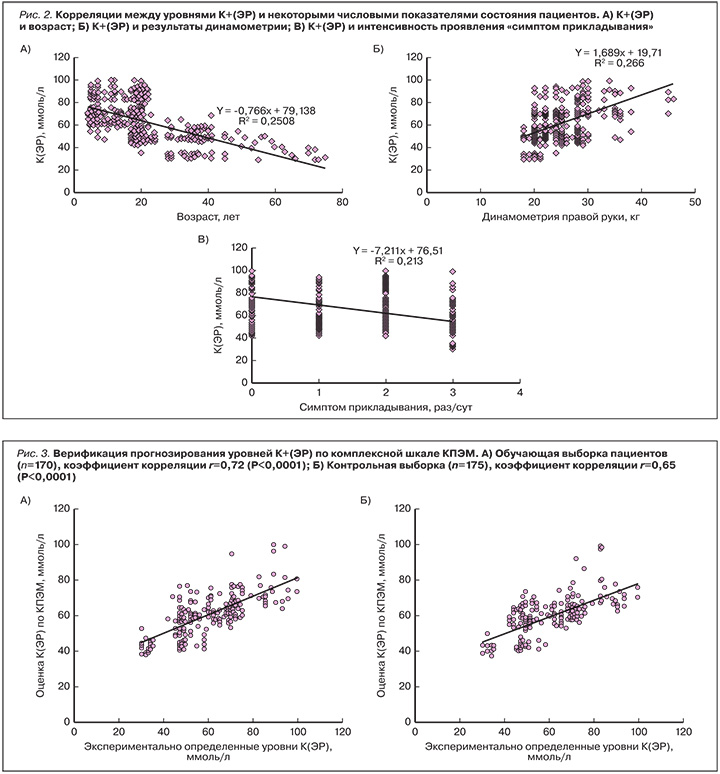
В частности, установлена обратная корреляция между уровнями К+(ЭР) и возрастом: уровни калия были достоверно ниже у более старших пациентов, так что повышение возраста на 1 год соответствовало снижению уровней К+(ЭР) в среднем на 0,77 ммоль/л (pис. 2А). Более высокие результаты динамометрии соответствовали более высоким уровням К+(ЭР): повышение результата динамометрии правой руки на 1 кг соответствовало повышению К+(ЭР) на 1,69 ммоль/л (pис. 2В).
 Достаточно информативным клиническим признаком снижения уровней К+(ЭР) у взрослых явился так называемый симптом прикладывания (поддержка рукой головы из-за усталости шеи) [VRS-STATIA]. Из физиологии хорошо известно, что калий участвует в процессах сокращения поперечнополосатой и гладкой мускулатуры. Поэтому низкая обеспеченность калием снижает силу скелетной мускулатуры и уменьшает тонус мышц спины и шеи.Число случаев «прикладывания» в течение рабочего/учебного дня отражает степень утомляемости мышц и, соответственно, зависит от обеспеченности калием. Настоящий анализ показал, что каждое дополнительное «прикладывание», отмеченное у пациента, соответствовало снижению уровней К+(ЭР) в среднем на 7,2 ммоль/л (pис. 2В, вес признака: -8,27).
Достаточно информативным клиническим признаком снижения уровней К+(ЭР) у взрослых явился так называемый симптом прикладывания (поддержка рукой головы из-за усталости шеи) [VRS-STATIA]. Из физиологии хорошо известно, что калий участвует в процессах сокращения поперечнополосатой и гладкой мускулатуры. Поэтому низкая обеспеченность калием снижает силу скелетной мускулатуры и уменьшает тонус мышц спины и шеи.Число случаев «прикладывания» в течение рабочего/учебного дня отражает степень утомляемости мышц и, соответственно, зависит от обеспеченности калием. Настоящий анализ показал, что каждое дополнительное «прикладывание», отмеченное у пациента, соответствовало снижению уровней К+(ЭР) в среднем на 7,2 ммоль/л (pис. 2В, вес признака: -8,27).
Интересно отметить, что в процессе построения второй части шкалы КПЭМ было установлено, что уровни К+(ЭР) зависят и от обеспеченности другими микронутриентами. В частности, прием витаминных комплексов (курсами по 1–2 мес не менее 1–2 раз/год) способствовал повышению уровней К+(ЭР) (в среднем на 4,9 ммоль/л, вес признака: +5,84), а наличие железодефицитной анемии, наоборот, способствовало достоверному снижению уровней К+(ЭР) (в среднем на 8,5 ммоль/л, вес признака: -18,0).
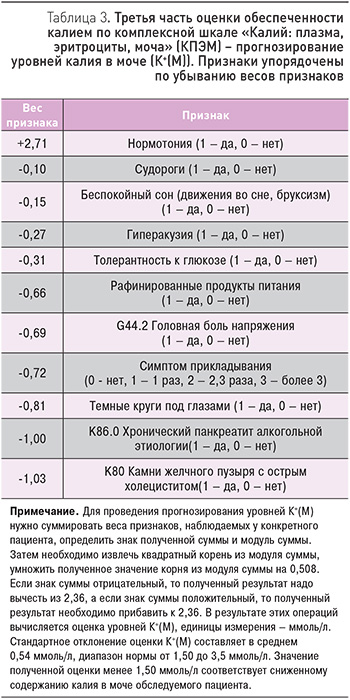
Верификация второй части шкалы КПЭМ с использованием независимой выборки пациентов (pис. 3) показала, что прогнозируемые значения уровней калия в эритроцитах по шкале КПЭМ находятся в статистически достоверной корреляции с экспериментально определенными уровнями К+(ЭР). При этом значения коэффициента корреляции между прогнозируемыми и экспериментальными уровнями К+(ЭР) достаточно высоки как для обучающей (r=0,72), так и для контрольной (r=0,65) выборок пациентов.
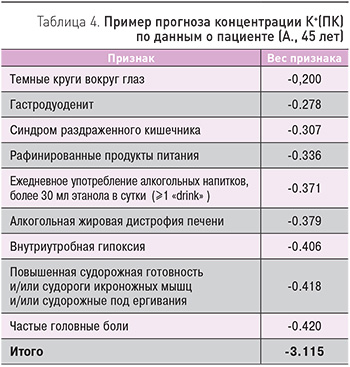
В табл. 3 представлена третья часть оценки обеспеченности калием по шкале КПЭМ – прогнозирование уровней калия в моче, К+(М). Из перечисленных в табл. 3 признаков только нормотония (вес признака: +1,512) была ассоциирована с положительным вкладом в уровни К+(М). Остальные признаки характеризовались отрицательными значениями весов и соответствовали клинической симптоматике дефицита калия (темные круги под глазами, гиперакузия, головная боль напряжения, симптом прикладывания, нарушения сна, судороги) и также наличию у пациента состояний, коморбидных недостаточной обеспеченности калием (хронический панкреатит алкогольной этиологии, камни желчного пузыря с острым холециститом, толерантность к глюкозе).
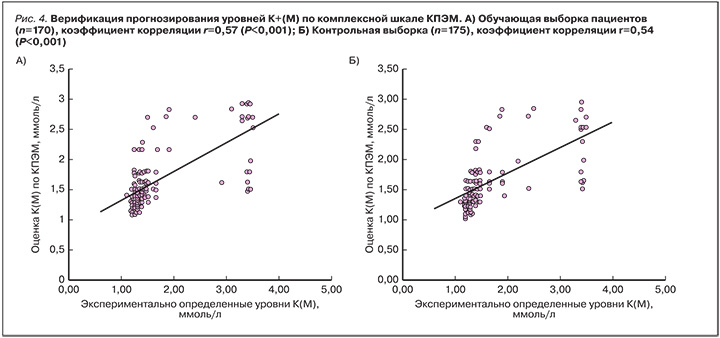
Верификация третьей части шкалы КПЭМ с использованием независимой выборки пациентов (pис. 4) показала, что прогнозируемые по шкале КПЭМ значения уровней калия в моче находятся в статистически достоверной корреляции с экспериментально определенными уровнями К+(М). При этом значения коэффициента корреляции между прогнозируемыми и экспериментальными уровнями К+(М) достаточно близки для обучающей (r=0,57) и контрольной (r=0,54) выборок пациентов.
 Таким образом, три части шкалы КПЭМ позволяют прогнозировать концентрации калия в плазме крови (1), эритроцитах (2) и моче (3) пациента на основании данных опроса, осмотра, анамнеза и динамометрии пациента. При этом с большей обеспеченностью калием ассоциированы артериальное давление в диапазоне нормы, хорошее самочувствие пациента, регулярные занятия физкультурой, прием витаминных комплексов. Различные заболевания в анамнезе, регулярное употребление алкоголя, прием рафинированных продуктов и глюкозотолерантность отрицательно сказываются на уровнях калия в исследуемых биосубстратах.
Таким образом, три части шкалы КПЭМ позволяют прогнозировать концентрации калия в плазме крови (1), эритроцитах (2) и моче (3) пациента на основании данных опроса, осмотра, анамнеза и динамометрии пациента. При этом с большей обеспеченностью калием ассоциированы артериальное давление в диапазоне нормы, хорошее самочувствие пациента, регулярные занятия физкультурой, прием витаминных комплексов. Различные заболевания в анамнезе, регулярное употребление алкоголя, прием рафинированных продуктов и глюкозотолерантность отрицательно сказываются на уровнях калия в исследуемых биосубстратах.
Клинический пример
Приведем краткий пример применения шкалы КПЭМ. Пациентка А. из «контрольной группы», 45 лет, 6 ОРВИ/год, характеризовалась нерациональным питанием (так называемый фастфуд), регулярным употреблением рафинированных продуктов питания, гиподинамией, низкими показателями динамометрии правой руки (18 кг), выраженным симптомом прикладывания (более 3 «прикладываний» в сутки), темными кругами под глазами, сниженным артериальным давлением, нарушенным режимом сна/бодрствования.
У пациентки отмечалось выпадение волос, спазмы (3 балла), беспокойный сон. Пациентке были поставлены следующие диагнозы: Психические и поведенческие расстройства, вызванные употреблением алкоголя, K70.0 Алкогольная жировая дистрофия печени, K70.1 Алкогольный гепатит, K86.0 Хронический панкреатит алкогольной этиологии, K29.9 Гастродуоденит неуточненный, K58 Синдром раздраженного кишечника, G44.2 Головная боль напряжения, G47.9 Нарушение сна неуточненное, H52 Миопия, I84 Геморрой, J15 Бактериальная пневмония анамнез, N20.2 Камни почек с камнями мочеточника (оксалаты). Из анамнеза известно, что пациентка родилась с признаками внутриутробной гипоксии (P20.9 Внутриутробная гипоксия неуточненная).
При суммировании данных пациентки по первой части шкалы КПЭМ (см. табл. 1) получается значение -3.115 (табл. 4), квадратный корень из модуля суммы 1,76, умножаем на 0,258, получаем 0,46. Вычитая полученный результат из 3,93, получаем прогноз уровней К+(ПК)=3,47±0,42 ммоль/л, что соответствует гипокалиемии в плазме крови (диапазон нормы от 3,50 до 5,00 ммоль/л). Экспериментально определенное значение К+(ПК) составило 3,40 ммоль/л.
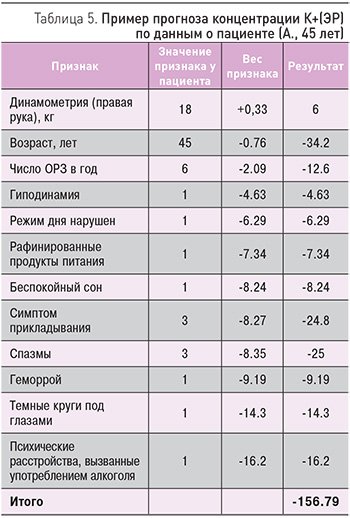
При суммировании данных пациентки по второй части шкалы КПЭМ (см. табл. 2) получается значение суммы, равное -156,79 (табл. 5). Квадратный корень из модуля суммы равен 12,52; умножая на 1,95, получаем 24,4. Так как знак суммы отрицательный, то из 72 вычитаем 24,4 и получаем оценку концентрации К+(ЭР), равную 47,6±11 ммоль/л (стандартное отклонение оценки К+(ЭР) составляет в среднем 11 ммоль/л). Таким образом, у пациентки отмечается выраженный дефицит калия в эритроцитах (нижняя граница нормы - 70 ммоль/л). При экспериментальном определении уровней калия в эритроцитах полученное значение оказалось еще ниже (34 ммоль/л).
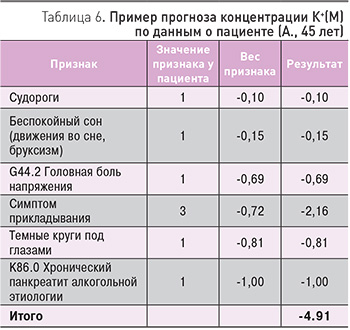
При суммировании данных пациентки по третьей части шкалы КПЭМ (см. табл. 3) получается значение суммы, равное -4.91 (табл. 6). Квадратный корень из модуля суммы равен 2,22; умножая на 0,508, получаем 1,13. Так как знак суммы отрицательный, то из 2,36 вычитаем 1,13 и получаем оценку концентрации К+(М)=1,23±0,54 ммоль/л, что соответствует сниженной обеспеченности калием. При экспериментальном определении уровней калия в эритроцитах полученное значение было несколько выше (1,33 ммоль/л).
Таким образом, оценка обеспеченности калием пациентки А. 45 лет по шкале КПЭМ указывает на выраженное снижение уровней калия в плазме крови, эритроцитах и моче. Данный прогноз по шкале КПЭМ полностью подтверждается результатами экспериментального исследования биосубстратов пациентки.
ЗАКЛЮЧЕНИЕ
На основе анализа выборки пациентов (n=345, возраст 18–75 лет) получена и верифицирована комплексная шкала «Калий: плазма, эритроциты, моча» (КПЭМ) для оценки обеспеченности калием. Для каждого пациента было измерено значение 521 параметра, на основе которых были выбраны наиболее информативные признаки, статистически достоверно коррелирующие с уровнями калия в исследуемых биосубстратах. Полученная в результате проведенного анализа данных шкала КПЭМ позволяет проводить неинвазивную оценку уровней калия в плазме крови, эритроцитах и моче пациентов на основе наблюдаемой симптоматики, данных анамнеза и опроса пациентов. На независимой контрольной выборке (n=175) установлено существование достоверных корреляций между экспериментально определенными уровнями калия и оценками, полученными по шкале КПЭМ. Использование предлагаемой шкалы позволяет существенно оценить состояние калиевого гомеостаза пациента еще до проведения клинико-лабораторных анализов соответствующих биосубстратов.



