ВВЕДЕНИЕ
В настоящее время имеется достаточный арсенал средств лечения кардиоваскулярной патологии. Один из таких методов лечения – имплантация внутрисердечных устройств (ВСУ), в частности постоянных искусственных водителей ритма (ИВР) и кардиовертеров-дефибрилляторов (КДФ) [1–4]. В последнее время отмечается рост количества имплантаций ИВР и КДФ, что объясняется расширением показаний к их установке [5–7]. Имплантацию ИВР и КДФ в литературе обозначают как кардиоимплантацию электронных устройств (КИЭУ) [8, 9]. Обладая доказанной эффективностью, КИЭУ в то же время может сопровождаться развитием ряда осложнений [5, 9]. К ранним осложнениям относят гематомы и пневмоторакс [5]. Одним из серьезных поздних осложнений КИЭУ являются инфекции [10–14].
Инфекция имплантированных ВСУ – тяжелая патология, связанная с высокой смертностью [15– 18]. Увеличение частоты установки ВСУ сопряжено с возрастанием доли пациентов старшего возраста, имеющих большое количество сопутствующих болезней [15]. Это приводит к риску инфицирования ВСУ, в том числе развитию инфекционного эндокардита (ИЭ). У пациентов с инфекцией ВСУ рекомендовано различать следующие сценарии развития ИЭ: локальную инфекцию устройства и ИЭ ВСУ [19, 20–22].
Наиболее частыми возбудителями ИЭ, ассоциированного с ВСУ, выступают стафилококки (60–80%), преимущественно «коагулазо-отрицательные стафилококки» [15, 23]. ИЭ ВСУ следует подозревать при наличии у пациента с ВСУ лихорадки неясного генеза [24, 25]. Как и при других формах ИЭ, в этом случае микробиологическое исследование крови на стерильность и эхокардиография (ЭхоКГ) — краеугольные камни диагностики [5, 11, 15].
Алгоритм диагностики инфекции ложа ВСУ или системной инфекции, ассоциированной с ВСУ, приведен на рисунке.
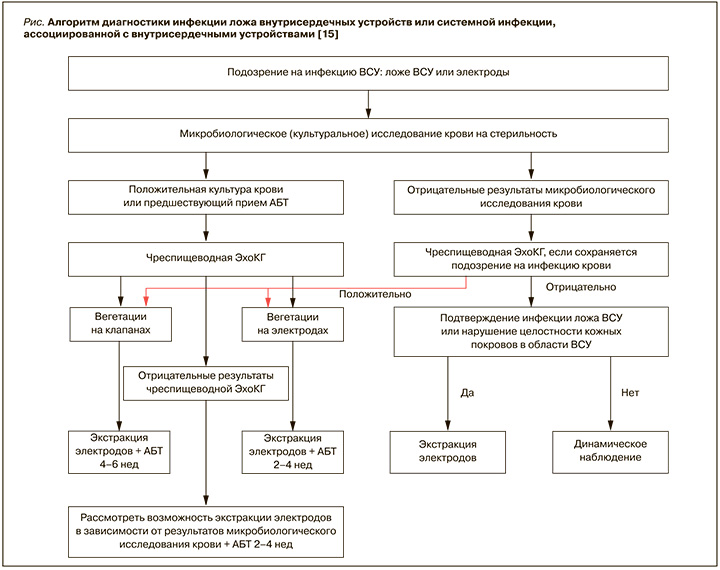
Ниже нами представлено клиническое наблюдение вторичного подострого ИЭ, ассоциированного с электродами имплантированного КДФ.
ОПИСАНИЕ КЛИНИЧЕСКОГО СЛУЧАЯ
Пациентка К., 50 лет, поступила в Лечебно-реабилитационный центр (ЛРЦ) Минздрава России 19.06.2023.
Жалобы при поступлении: общая слабость, периодические ознобы, эпизоды повышения температуры тела до 39 °С, боли и ограничение объема движений в правом коленном суставе.
Анамнез заболевания: в раннем детстве диагностирован врожденный порок сердца – дефект межпредсердной перегородки, открытый артериальный проток. В 1978 г. пациентке была выполнена перевязка открытого артериального протока, ушивание дефекта межпредсердной перегородки. В 2000 г. появились эпизоды желудочковой тахикардии, частая желудочковая и наджелудочковая экстрасистолии, выявлена асимметричная гипертрофия миокарда левого желудочка (ЛЖ) без обструкции выносящего тракта. В течение многих лет пациентка принимала амиодарон. 10.11.2020. в Федеральном научном центре трансплантологии и искусственных органов им. академика В.И. Шумакова ей была проведена имплантация трехкамерного КДФ Medtronic Brava CRT-D DTBC2D4. В дальнейшем больная наблюдалась кардиологом, применяла амиодарон, метопролол, спиронолактон, ацетилсалициловую кислоту.
В октябре 2021 г. пациентка в дорожно-транспортном происшествии в качестве пассажира получила множественные травмы, по поводу которых ей было выполнено оперативное лечение (открытая репозиция, остеосинтез правой бедренной кости спицестержневым аппаратом; открытая репозиция, остеосинтез левой лучевой кости титановой пластиной; открытая репозиция, остеосинтез средней трети – нижней трети левой локтевой кости титановой пластиной и винтами; открытая репозиция и остеосинтез левого надколенника). В марте 2023 г. при проведении реабилитационных мероприятий пациентка отметила гиперемию в области правого коленного сустава, повышение температуры тела до 37,8 °С. Была госпитализирована в ортопедический стационар, состояние расценили как спицевой остеомиелит мыщелков правой бедренной кости, было выполнено удаление металлофиксаторов из обоих надколенников в сочетании с остеонекрэктомией наружного мыщелка правой бедренной кости.
В течение года пациентка отмечала эпизоды повышения температуры тела до 38–39 °С. На ЭхоКГ от 23.12.2022 были выявлены умеренное расширение полости левого предсердия, гипертрофия ЛЖ, умеренная легочная гипертензия, небольшой гидроперикард, фибриновые нити вокруг электрода, убедительных данных в пользу вегетаций не было.
Пациентку госпитализировали в отделение медицинской реабилитации взрослых ЛРЦ Минздрава России. В первые сутки нахождения в стационаре у больной отмечались озноб, повышение температуры тела до 39,5 °С, снижение артериального давления (АД) до 80/60 мм рт.ст.; при лабораторном скрининге были обнаружен лейкоцитоз, повышение прокальцитонина (ПКТ). С подозрением на вторичный ИЭ (ассоциированный с КДФ) пациентка была переведена в отделение реанимации и интенсивной терапии (ОРИТ).
Анамнез жизни: COVID-19 (КТ-2) в 2021 г., не вакцинирована. Операции, травмы указаны выше. Гемотрансфузии (2021, 2022). Непереносимости лекарств и пищевых продуктов нет. Вредных привычек нет.
Данные осмотра в ОРИТ: состояние тяжелое. Температура тела 38 °С. Нормостенического телосложения. Сознание ясное, поведение спокойное. Зрачки сужены, симметричны; фотореакция сохранена. Менингеальные знаки отрицательные. Острой очаговой симптоматики не отмечается. Кожные покровы чистые, сухие, теплые. Постоперационные рубцы, рубцы от винтов Шанца в области левого предплечья, наружной поверхности правого бедра в нижней трети, обоих надколенников. Зон нарушения целостности кожного покрова не обнаружено. Молочные железы без особенностей. Область правого коленного сустава с умеренной дефигурацией, зон гиперемии, локального повышения температуры не отмечено. Пассивные движения в правом коленном суставе безболезненные. Риск образования пролежней умеренный. Дыхание самостоятельное с частотой дыхания 16–17/мин, аускультативно дыхание жесткое, выслушивается над всеми легочными полями, равномерно и симметрично, хрипов нет. Экскурсия грудной клетки равномерная, вспомогательная мускулатура в акте дыхания не участвует. Сатурация кислорода на атмосферном воздухе 95–96%. Спонтанное откашливание адекватное, откашливаемый секрет слизистый, прозрачный, кровохарканья нет. Гемодинамика стабильна без вазо- и инотропной поддержки с АД 115–120/55–60 мм рт.ст., ритм синусовый, частота сердечных сокращений (ЧСС) 75–80/мин; за время мониторного наблюдения срабатываний КДФ не регистрировалось. Признаков системной гипоперфузии нет. Тоны сердца приглушены, ритмичные; в проекции трикуспидального клапана пансистолический шум. Центральный венозный катетер в правой внутренней яремной вене функционирует, кожа вокруг него без воспалительных изменений. Язык по центральной линии, не обложен, не прикушен; глотание свободное, питание пероральное. Живот мягкий, на пальпацию не реагирует. Перистальтика выслушивается. Мочеиспускание по уретральному катетеру, моча светло-желтая.
Данные лабораторных исследований:
- ПКТ от 19.06.2023: >10 нг/мл;
- клинический анализ крови от 20.06.2023: лейкоциты – 32,60×109/л; лимфоциты – 7%; моноциты – 3%; эритроциты – 3,17×1012/л; гемоглобин – 84 г/л; гематокрит – 26,0%; тромбоциты – 148,0×109/л; эозинофилы – 1,0%; палочкоядерные нейтрофилы – 8,0%; сегментоядерные нейтрофилы – 81,0%;
- общий анализ мочи от 19.06.2023: удельная плотность – 1030 г/л; прозрачность – мутная; цвет – светло-желтый; кислотность (рН) – 1,0; белок – 1,000 г/л; глюкоза – 0,00 ммоль/л; кетоны – 0,00 ммоль/л; уробилиноген – 0,00 ммоль/л; эпителий плоский – умеренное количество; лейкоциты – 50–55 в поле зрения; эритроциты неизмененные – 3–5 в поле зрения; цилиндры – обнаружены; слизь – много; бактерии – умеренное количество.
- коагулограмма от 19.06.2023: активированное частичное тромбопластиновое время (АЧТВ) – 37,70 с; тромбиновое время – 11,70 с; протромбин – 53,90%; международное нормализованное отношение (МНО) – 1,34; фибриноген – 3,99 г/л;
- биохимический скрининг от 19.06.2023: общий белок – 82 г/л; мочевина – 9,4 ммоль/л; креатинин – 122 мкмоль/л; холестерин – 4,31 ммоль/л; общий билирубин – 6,6 мкмоль/л; аспартатаминотрансфераза (АСТ) – 17,7 Ед/л; аланинаминотрансфераза (АЛТ) – 9,2 Ед/л; глюкоза – 7,81 ммоль/л; калий – 4,72 ммоль/л; натрий – 137,9 ммоль/л; С-реактивный белок (СРБ) – 59,4мг/л;
- СРБ от 20.06.2023: 95,5 мг/л;
- группа крови, резус, антитела, KELL от 20.06.2023: группа крови – III; резус-фактор положительный; резус-антитела – не обнаружены; антиген Келл – отрицательно; фенотипы эритроцитов – С+, с+, Е+, е+;
- общий анализ крови от 22.06.2023: лейкоциты – 14,30×109/л; эритроциты – 3,38×1012/л; гемоглобин – 84 г/л; гематокрит – 27,0%; тромбоциты – 162,0×109/л;
- общий анализ мочи от 22.06.2023: удельная плотность – 1025 г/л; прозрачность – мутная; цвет – желтая; кислотность (рН) – 0,0; белок – 0,3 г/л; глюкоза – 0,00 ммоль/л; кетоны – 0,00 ммоль/л; уробилиноген – 0,00 ммоль/л; эпителий плоский – умеренное количество; эпителий переходный – отсутствует; эпителий почечный – отсутствует; лейкоциты – 2–4 в поле зрения; эритроциты неизмененные – 5–7 в поле зрения; эритроциты измененные – отсутствуют в поле зрения; цилиндры – отсутствуют; слизь – умеренно; соли мочевой кислоты – отсутствуют; степень камнеобразования – 0–I; бактерии – отсутствуют; дрожжевые клетки – отсутствуют; мицелий гриба – отсутствует; простейшие – не обнаружены;
- ПКТ от 23.06.2023: 2 нг/мл;
- биохимический скрининг от 23.06.2023 : мочевина – 3,9 ммоль/л; креатинин – 78 мкмоль/л; глюкоза – 4,63 ммоль/л; калий – 4,29 ммоль/л; натрий – 136,5 ммоль/л; СРБ – 97,8 мг/л;
- биохимический скрининг от 26.06.2023: креатинин – 68 мкмоль/л; глюкоза – 4,75 ммоль/л; калий – 4,14 ммоль/л; натрий – 137,6 ммоль/л; СРБ – 34,9 мг/л;
- иммуноглобулины A, М, G от 27.06.2023: IgA – 2,50 г/л; IgM – 1,40 г/л; IgG – 27,00 г/л;
- С3 компонент комплемента от 27.06.2023: 94.0 ммоль/л;
- С4 компонент комплемент от 27.06.2023: 17.0 ммоль/л;
- тиреотропный гормон (ТТГ), тироксин (Т4) свободный от 27.06.2023: ТТГ – 3,700 мМЕ/л; Т4 – 14,80 пмоль/л;
- ПКТ от 27.06.2023: 0,5 нг/мл;
- анализы крови от 27.06.2023: железо – 7,6 мкмоль/л; ферритин – 223,0 нг/мл; цинк – 9,5 мкмоль/л; общий белок – 83 г/л; ревматоидный фактор – 33,6 МЕ/мл; НbsAg, HCV, BИЧ, RW: антитела к ВИЧ – отрицательно; поверхностный антиген вирусного гепатита B (HBs-антиген) – отрицательно; антитела к вирусу гепатита С – отрицательно; реакция Вассермана – отрицательно;
- клинический анализ крови от 27.06.2023: лейкоциты – 14,93×109/л; лимфоциты – 9%; моноциты – 3%; эритроциты – 3,88×1012/л; гемоглобин – 101 г/л; гематокрит – 30,5%; средний объем эритроцита – 78,50 фл; среднее содержание гемоглобина – 26,1пг ; средняя концентрация гемоглобина в эритроците – 333 г/л; коэффициент анизотропии эритроцитов – 20,3%; тромбоциты – 278,0×109/л; эозинофилы – 1,0%; палочкоядерные нейтрофилы – 8,0%; сегментоядерные нейтрофилы – 79,0%; скорость оседания эритроцитов (СОЭ) – 71 мм/ч; гипохромия эритроцитов – 0; анизоцитоз эритроцитов – 1,0; микроцитоз эритроцитов – 1,0;
- белковые фракции от 30.06.2023: альбумин-глобулиновый коэффициент – 0,68; глобулины – 59,64%; альбумин – 40,36%; альфа1-глобулин – 6,27%; альфа2-глобулин – 13,44%; бета-глобулин – 10,46 %; гамма-глобулин – 29,47%; общий белок в сыворотке крови – 83 г/л;
- циркулирующие иммунные комплексы (ЦИК) от 27.06.2023: ЦИК CIC-C1q – 1,000 МЕ/мл; ЦИК C3d – 26,0 мкг/мл;
- общий анализ мочи от 27.06.2023: удельная плотность – 1006 г/л; прозрачность – полная; цвет – светло-желтая; кислотность (рН) – 5,0; белок – 0,000 г/л; глюкоза – 0,00 ммоль/л; кетоны – 0,00 ммоль/л; уробилиноген – 0,00 ммоль/л; эпителий плоский – незначительное количество; эпителий переходный – отсутствует; эпителий почечный – отсутствует; лейкоциты – 1–2 в поле зрения; эритроциты измененные – 2–3 в поле зрения; цилиндры – отсутствуют; слизь – незначительное количество; соли – отсутствуют; бактерии – отсутствуют;
- СРБ от 28.06.2023: 27,0 мг/л;
- гемокультура от 19.06.2023: Enterococcus faecalis (чувствителен к ванкомицину, кубицину, имипенему/циластатину, резистентен к левофлоксацину, тетрациклину, фосфомицину, эритромицину).
Данные инструментальных исследований:
- электрокардиограмма (ЭКГ). Заключение: ЧСС 71/мин; синусовый ритм; увеличение обоих предсердий; неспецифические изменения зубца T;
- ЭхоКГ. Заключение: полости сердца не расширены; признаки умеренной гипертрофии миокарда ЛЖ; глобальная сократимость миокарда удовлетворительная; митральная регургитация 1 степени; трикуспидальная регургитация 1–2 степени; легочная регургитация 1–2 степени; в правых отделах сердца лоцированы гиперэхогенные линейные структуры – электроды электрокардиостимулятора; в правом предсердии выявлены гипоэхогенные, относительно подвижные преимущественно овальной формы образования, вероятно, фиксированные к электродам и, возможно, к месту ушивания дефекта межпредсердной перегородки в средней трети, с максимальным размером до 15–16 мм×19 мм – вегетации?
- ультразвуковое ангиосканирование вен нижних конечностей. Заключение: данных в пользу тромбоза вен не выявлено;
- мультиспиральная компьютерная томография (МСКТ) органов брюшной полости. Заключение: печень – без очаговых изменений; желчные протоки, желчный пузырь, поджелудочная железа, селезенка, надпочечники, почки, чашечно-лоханочная система почек, мочеточники без особенностей; свободного газа и жидкости не выявлено; увеличенные лимфатические узлы не обнаружены; периневральные кисты на уровне копчика до 12 мм; на уровне сканирования – жидкостное образование в правых отделах малого таза до 27 мм – вероятно, киста; на фоне кинетических артефактов данных в пользу острой хирургической патологии не получено;
- МСКТ правого коленного сустава. Заключение: состояние после металлоостеосинтеза правой бедренной кости на фоне оскольчатого перелома со смещением фрагментов; синовит; выраженный артроз правого коленного сустава; тяжистость и уплотнение параартикулярных мягких тканей; признаки остеопороза;
- Холтеровское мониторирование ЭКГ. Заключение: регистрировался синусовый ритм и ритм искусственного водителя ритма в режимах предсердной стимуляции с редкими эпизодами секвенциальной стимуляции; средняя ЧСС 62 уд/ мин, минимальная ЧСС 59 уд/мин, максимальная ЧСС 89 уд/мин; нарушений функции стимулирующей системы не выявлено; единичные желудочковые и наджелудочковые экстрасистолы; значимых изменений конечной части желудочкового комплекса не наблюдалось;
- МСКТ органов грудной клетки. Заключение: признаки верхнедолевой пневмонии справа; локальный пневмофиброз; субсегментарные ателектазы S9,4; лимфаденопатия; минимальный гидроперикард; жидкость в правой плевральной полости; косвенные признаки легочной гипертензии.
Результаты консультаций специалистов:
- консультация травматолога-ортопеда. Заключение: убедительных данных в пользу наличия остеомиелита нет;
- консультация аритмолога. Заключение: Батарея = ОК, ориентировочный срок службы батареи 8 лет; импеданс левожелудочкового электрода более 3000 ОМ, при амплитуде стимуляции 8В×1 с эффективной стимуляции нет; измерение порога стимуляции правожелудочкового электрода затруднено в связи с индуцируемой стимуляцией желудочковой экстрасистолией; процент бивентрикулярной стимуляции 1%; зафиксировано 3 неустойчивых эпизода желудочковой тахикардии; эпизоды частой желудочковой экстрасистолии – до 101/ч;
- консультация врача – клинического фармаколога. Рекомендации: пациентка нуждается в продолжении антибактериальной терапии со сменой схемы по антибиотикограмме в соответствии с клиническими рекомендациями по ведению пациентов с ИЭ; приоритетная схема по сумме критериев – ампициллин по 3 г каждые 6 ч внутривенно капельно и цефтриаксон по 2 г каждые 12 ч внутривенно капельно до достижения полных 6 нед терапии, включая текущую схему; при стабилизации состояния или абсолютной невозможности применения парентеральной схемы может быть применена схема – амоксициллин по 1 г каждые 6 ч перорально и рифампицин по 600 мг каждые 12 ч перорально.
Проведенное лечение: цефазолин 2 г в 8 ч; с 19.06.2023 по 02.07.2023 – ванкомицин 1 г в 12 ч внутривенно капельно; 20.06.2023 – эритроцитная взвесь лейкоредуцированная (2 дозы); эноксапарин натрия 0,6 подкожно 2 раза/сут, амиодарон 200 мг по 1/2 таблетки утром, омепразол 20 мг вечером, эритроцитная взвесь лейкоредуцированная (2 дозы).
Больная выписалась 02.07.2023 в относительно удовлетворенном состоянии с заключительным клиническим диагнозом:
- основной: вторичный подострый инфекционный эндокардит, ассоциированный с имплантированным кардиовертером-дефибриллятором (Enterococcus faecalis);
- фоновое заболевание: врожденный порок сердца: дефект межжелудочковой перегородки, открытый артериальный проток. Перевязка открытого артериального протока, ушивание дефекта межпредсердной перегородки в 1978 г. Ассиметричная гипертрофия левого желудочка без обструкции выносящего тракта. Нарушения ритма сердца: пароксизмальная желудочковая тахикардия, частая наджелудочковая и желудочковая экстрасистолия. Имплантация трехкамерного КДФ Medtronic Brava CRT-D DTBC2D4 № SNBLZ605889S с предсердным эндокардиальным электродом Medtronic 5076/52snPJN8039872 (активной фиксации), дефибриллирующим правожелудочковым электродом Medtronic 6947М/62cmTDK286145V (активной фиксации) от 10.11.2020;
- конкурирующее заболевание: последствия перенесенной автодорожной тяжелой сочетанной травмы от 07.10.2021 Консолидированный остеосинтезированный титановой пластиной LC-DCP и винтами перелом левых локтевой и лучевой костей. Консолидированный остеосинтезированный спицами и винтами перелом правой бедренной кости. Консолидированный остеосинтезированный перелом левого надколенника с последующим демонтажем металлоконструкций. Постоперационная сгибательная контрактура правого коленного сустава. Спицевой остеомиелит внутрисуставных структур правого коленного сустава от марта 2023, разрешение. Удаление металлоконструкций, остеонекрэктомия наружного мыщелка правой бедренной кости 15.03.2023 г. Удаление металлоконструкций из левого надколенника 15.03.2023;
- осложнения основного заболевания: септическая эмболическая полисегментарная пневмония верхней доли правого легкого. Сепсис. Синдром системного воспалительного ответа. Анемия хронического заболевания средней степени тяжести. Дыхательная недостаточность 1–2 ст. Хроническая сердечная недостаточность 1 ст., функциональный класс (ФК) 2. Умеренная легочная гипертензия;
- сопутствующие заболевания: последствия перенесенной новой короанвирусной инфекции COVID-19 в октябре 2021 г. Хронический гастродуоденит.
ОБСУЖДЕНИЕ
В приведенном наблюдении больная 50 лет поступила в плановом порядке для реабилитационных мероприятий по поводу посттравматической сгибательной контрактуры правого коленного сустава, перенесенного спицевого остеомиелита мыщелков правой бедренной кости. В числе сопутствующих заболеваний оказался хирургически скорректированный врожденный порок сердца, в 2020 г. был установлен КФД. В течение первых суток у пациентки развились гипертермия, гипотензия, в крови были обнаружены лейкоцитоз и увеличение уровня ПКТ. В связи с наличием потенциального источника инфицирования в структурах правого коленного сустава и установленного интракардиального устройства был заподозрен электрод-ассоциированный ИЭ.
Пациентка прошла комплексное обследование, в ходе которого были выявлены ЭхоКГ-признаки поражения эндокарда правого предсердия на фоне имплантированного эндокардиального устройства в сочетании с лихорадкой и системной воспалительной реакцией, а также обнаружен одиночный инфильтрат верхней доли правого легкого (септическая эмболическая пневмония). Эти изменения позволили считать диагноз ИЭ определенным.
19.06.2023 была начата эмпирическая антимикробная терапия. По результатам гемокультуры антибактериальная терапия была скорректирована. На фоне проводимого лечения наблюдалась положительная динамика состояния пациентки: нормотермия, снижение маркеров системного воспаления, отсутствие признаков септического органного повреждения, достижение стабильных гемодинамических показателей, отсутствие признаков активного инфекционного процесса экстракардиальной локализации, в частности рецидива остеомиелита, септического артрита. Пациентке проводились телемедицинские консультации с сотрудниками НМИЦ сердечно-сосудистой хирургии им. А.Н. Бакулева, в результате которых ей было рекомендовано решение вопроса об эксплантации электрокардиостимулятора в условиях многопрофильного стационара с наличием специалистов по сердечно-сосудистой хирургии, аритмологии и травматологии-ортопедии. Также была проведена консультация с сотрудниками Федерального научного центра трансплантологии и искусственных органов им. академика В.И. Шумакова: пациентке показано удаление системы в электрокардиостимулятор-электрод с применением метода эксимерного лазера.
ЗАКЛЮЧЕНИЕ
В настоящее время КИЭУ часто используется при различной сердечно-сосудистой патологии. В последние годы наблюдается неуклонный рост КИЭУ, что привело к увеличению заболеваемости инфекциями, связанными с имплантируемыми электронными устройствами [5, 11, 15]. Точная диагностика инфекций, обусловленных КИЭУ, имеет важное значение, учитывая необходимость удаления инфицированного устройства и длительной антимикробной терапии [5, 13, 15]. Клинические и лабораторные данные в этом случае служат полезными диагностическими инструментами, но часто требуются методы мультимодальной визуализации, которые в настоящее время рекомендованы российскими клиническими руководствами для диагностики инфекций КИЭУ [15].
Представленное нами клиническое наблюдение свидетельствует о сложностях диагностики ИЭ у больных с наличием имплантированных электронных кардиоустройств. Наличие у таких пациентов рецидивирующей лихорадки требует в первую очередь исключения инфекций, связанных с данными устройствами. При этом в процессе диагностического поиска, а в последующем и при выработке тактики лечения необходимо следовать общепринятым клиническим рекомендациям.



