ВВЕДЕНИЕ
Острые нарушения мозгового и коронарного кровообращения – два самых тяжелых заболевания сердечно-сосудистой системы. Несмотря на некоторые общие факторы риска, причины, звенья патогенеза и подходы к терапии, они находятся в достаточно сложной взаимосвязи друг с другом. Не вызывает сомнения вклад кардиальной патологии в развитие ишемического инсульта: одним из самых частых его подтипов является кардиоэмболический. Кроме того, при остром инфаркте миокарда, пароксизме фибрилляции предсердий или иной острой патологии сердца, ведущей к падению системного артериального давления (АД), может возникнуть гемодинамический подтип ишемического инсульта [1]. О сложностях дифференциальной диагностики этих двух состояний говорили уже более 40 лет назад [2], однако создание специализированных сосудистых центров, определение четких алгоритмов диагностики и лечения [3], введение в рутинную практику экстренной нейровизуализации, аппаратов ультразвукового исследования (УЗИ) экспертного класса, автоматизированных систем лабораторной диагностики не упростили задачи клинициста в этой части ургентной терапии [4].
В последние годы появилось много исследований цереброкардиального синдрома – состояния, когда на фоне острой церебральной патологии возникают инфарктоподобные изменения, которые нужно отличать от инфаркта миокарда [5]. Значительно меньше сообщений об обратной ситуации – сосудистой мозговой недостаточности при остром инфаркте миокарда. Это состояние даже по-разному называется специалистами: кардиологами – «церебральная форма инфаркта миокарда» в ряду его атипичных форм [6, 7], а неврологами – «псевдоинсульт» [2, 8]. Встречаются и другие названия этих же состояний: «кардиоцеребральный синдром» [9], в англоязычной литературе – «имитаторы инсульта» (strokemimics) [10], правда, инфаркты миокарда чаще всего не входят в этот список состояний-имитаторов. Именно этой проблеме было посвящено настоящее исследование.
Цель – изучить особенности клиники, лабораторных и инструментальных исследований пациентов, у которых клиника ишемического инсульта явилась «маской» инфаркта миокарда.
МАТЕРИАЛ И МЕТОДЫ
Был проведен ретроспективный анализ летальных клинических случаев пациентов, поступивших в Региональный сосудистый центр (РСЦ) для больных с острым нарушением мозгового кровообращения (ОНМК) ОГАУЗ «Томская областная клиническая больница» в 2016–2023 гг.
Критерии выбора (включения)
1. Клиника инсульта, включающая наличие яркой очаговой неврологической симптоматики при поступлении в стационар, или однозначные указания на нее в дебюте заболевания в случае поступления уже в крайне тяжелом состоянии, т.е. с преобладанием общемозговой симптоматики.
2. Летальный исход, наступивший в срок не более 2 сут (чаще всего несколько часов).
3. Выявление макроскопических и микроскопических признаков острого инфаркта миокарда при патологоанатомическом исследовании.
4. Отсутствие признаков острого инсульта при патологоанатомическом исследовании.
Критерии исключения
1. Нелетальные случаи.
2. Летальные случаи, когда не было проведено патологоанатомическое исследование.
3. Отсутствие клиники инсульта.
4. Наличие подтверждения одновременно и инфаркта миокарда, и церебрального инсульта при патологоанатомическом исследовании.
5. Наличие подтверждения инсульта при патологоанатомическом исследовании.
6. Отсутствие признаков инфаркта миокарда при патологоанатомическом исследовании.
7. Случаи, когда клиника инфаркта миокарда развилась более чем через двое суток после госпитализации по поводу инсульта.
Случаев, отвечающих вышеуказанным критериям, было немного – 50 за 8 лет. В некоторых из них не удалось полностью оценить анамнез; из-за краткости пребывания не всем пациентам были выполнены необходимые лабораторные и инструментальные исследования; в некоторых же случаях отсутствовали данные по микроскопическому исследованию. Из-за этого адекватный статистический анализ не представляется возможным. Однако даже по имеющимся данным можно оценить наиболее типичные особенности анамнеза, клиники, результаты исследований и анализов у выбранной группы пациентов.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Анамнез. При анализе паспортных и анамнестических данных у этой группы пациентов обращает на себя внимание их средний возраст – 74,4 года. 24 пациента (почти половина) были старше 80 лет. Это на 3,4 года больше среднего возраста всех умерших в РСЦ (он составляет около 71 года в течение уже нескольких лет) и значительно выше возраста всех поступивших в РСЦ (67,5 лет). Это согласуется с литературными данными, авторы которых почти всегда отмечают рост атипичных форм острого инфаркта миокарда у пациентов пожилого и старческого возраста [6–8]. Это не удивительно, так как с увеличением возраста «накапливается багаж» хронических или перенесенных острых заболеваний, в том числе сердечно-сосудистой системы.
По половому составу анализируемая группа распределилась практически поровну: 23 мужчины и 27 женщин, т.е. явной гендерной диспропорции выявлено не было, хотя в литературе есть упоминания о преобладании женщин в группе с церебральной формой инфаркта миокарда [6]. Гипертоническая болезнь была диагностирована практически у всех пациентов, кроме тех, у кого сбор анамнеза был невозможен и отсутствовали данные по этому поводу в архиве медицинской информационной системы БАРС. У 11 пациентов (22%) в анамнезе были указания на перенесенный инфаркт миокарда, у 11 – на мерцательную аритмию, 12 перенесли инсульт. Указания на сахарный диабет имелись у 12 пациентов. Другие тяжелые соматические заболевания (онкологические, желудочно-кишечные, пневмония, анемия) и дегенеративные (болезнь Паркинсона, деменция) отмечались еще в 13 случаях. Таким образом, очевидно, что данная выборка представляет собой наиболее тяжелую группу коморбидных пациентов, что также согласуется с литературными данными.
Время от первых симптомов до госпитализации составило в среднем 14 ч, 40 пациентов (80%) были доставлены в течение первых суток после ухудшения их состояния. Это говорит о достаточно остром начале заболевания, но не дает возможности дифференцировать конкретный вид острой патологии: и острый инфаркт миокарда, и инсульт, и еще многие заболевания имеют острое начало. У половины пациентов (n=25) в дебюте заболевания была полная или частичная утрата сознания, а характерные для острого коронарного синдрома жалобы наблюдались только у одного пациента. Артериальная гипотензия была выявлена у 6 пациентов, одышка – у 3, после клинической смерти и успешных реанимационных мероприятий в РСЦ для больных с ОНМК были доставлены 4 пациента. Вместе с тем очаговая неврологическая симптоматика на догоспитальном этапе определялась у 32 пациентов (64%): левосторонний гемипарез был выявлен у 14, правосторонний – у 14, нарушения речи – у 13 (причем только в 5 случаях расстройства речи сочетались с правосторонним гемипарезом и всего в 2 – с расстройством сознания), другие неврологические симптомы – еще в 3 случаях.
Объективный статус при поступлении. При поступлении ясное сознание было только у 5 пациентов, средний балл по Шкале комы Глазго (ШКГ) составил 11,3, что соответствует глубокому оглушению. В глубокой и терминальной коме (3–6 баллов по ШКГ) доставлено 6 пациентов. У остальных была возможность прямо или косвенно оценить очаговую неврологическую симптоматику – она была выявлена у 21 пациента (почти у половины, находящихся в сознании, сопоре или поверхностной коме). Из них гемипарезы были определены у 12 пациентов слева, у 9 – справа, нарушения речи – у 11 человек, причем в 8 случаях они выявлялись в сочетании с правосторонним гемипарезом, в 3 – с левосторонним. Другие неврологические симптомы (парез взора, глазодвигательные расстройства, асимметрия лица) были обнаружены еще в 11 случаях. Средний балл по шкале тяжести инсульта Национальных институтов здоровья CША (NIHSS) составил в этой группе 17,7 баллов, а в общей группе, включая крайне тяжелых, – 19,6 баллов; это соответствует грубой неврологической симптоматике, или тяжелому инсульту.
Обследование при поступлении. Согласно Порядку [3] и клиническим рекомендациям [11], все поступающие пациенты с подозрением на ОНМК проходят компьютерную томографию (КТ) головного мозга. Она была выполнена у 49 пациентов (у одного проводились реанимационные мероприятия уже при поступлении). Признаков внутричерепного кровоизлияния не было выявлено ни у одного, у 32 пациентов не было обнаружено никаких очаговых изменений вещества головного мозга. Признаки хронической ишемии мозга (расширение желудочковой системы, углубление конвекситальных борозд, лейкоареоз) были установлены практически у всех пациентов. В 11 случаях были выявлены признаки кистозно-глиозных изменений вещества головного мозга как остаточных явлений перенесенных ранее инсультов. Следует напомнить, что признаки ишемического инсульта в первые часы после его начала на нативной КТ чаще всего не обнаруживаются, поэтому их отсутствие не служит основанием для исключения диагноза ишемического инсульта [8, 11]. Отдельное внимание на себя обращает выявление в 9 случаях (18,4%) очагов, похожих на ишемические и топически соответствующие клиническим проявлениям неврологической симптоматики. Их значительное число исключает случайные единичные ошибки радиолога. Зная, что ни у одного из пациентов этой группы не было обнаружено макроскопических и микроскопических признаков острого ишемического поражения мозга при патологоанатомическом исследовании, этот факт вызывает множество вопросов и требует отдельного обсуждения. Самое простое объяснение этого феномена: Qui quaerit, reperit (лат. «Кто ищет – находит»).
В 5 случаях КТ головного мозга проводилось повторно за первые-вторые сутки, в 4 из них было подтверждено отсутствие ишемических очагов, а в одном – выявленный при поступлении ишемический очаг.
Электрокардиография (ЭКГ) также входит в обязательный набор исследований при поступлении [3], однако в 14 случаях проанализировать ее результаты не удалось. Тахикардия была установлена в 14 случаях (38,9%), фибрилляция предсердий – еще в 14, признаки повышенной нагрузки на левый желудочек – в 11 (30,6%), блокада левой ножки пучка Гиса и ее ветвей – в 7 (19,4%), правой – в 5 (13,9%), нарушение процессов реполяризации и диффузные изменения миокарда желудочков – в 4 (11,1%), экстрасистолия – в 2. Признаки постинфарктного кардиосклероза (рубцовых изменений) были выявлены у 9 пациентов, а признаки острого нарушения коронарного кровообращения (ОНКК) в виде характерного подъема или депрессии сегмента ST – еще у 9 больных (у 3 из них – на фоне рубцовых изменений). Это составило лишь четверть всех пациентов. Учитывая это, а также то, что и при тяжелом инсульте у большинства пациентов регистрируются изменения на ЭКГ [5], этот метод исследования не является решающем в дифференциально-диагностическом процессе.
Эхокардиография (ЭхоКГ) также входит в обязательный набор исследований при инсульте, но Порядком [3] не регламентирована хронометрия ее проведения. Чаще всего она проводится вместе с обязательным УЗИ сосудов шеи в течение первых 3 ч после поступления. Это исследование было выполнено 34 пациентам (остальные 16 либо были в крайне тяжелом состоянии в процессе проведения реанимационных мероприятий, либо умерли раньше трех часов). Локальная гипокинезия миокарда была обнаружена в 18 случаях (более чем у половины), причем только в 3 случаях эти изменения были у пациентов с признаками ОНКК по ЭКГ, в 1 – с рубцовыми изменениями по ЭКГ, и еще в 2 случаях на ЭКГ регистрировались и признаки ОНКК, и рубцовых изменений. Еще у 4 пациентов с выявленной локальной гипокинезией без признаков ОНКК и рубцов по ЭКГ фиксировались признаки блокады левой ножки (2) и правой ножки (2) пучка Гиса. Таким образом, в 12 случаях ЭхоКГ была единственным инструментальным способом верификации острой коронарной патологии, и только в одном случае выявленные на ЭКГ признаки ОНКК не нашли своего подтверждения на ЭхоКГ.
Лабораторные анализы выявили у большинства пациентов признаки неспецифической катехоламиновой реакции в виде лейкоцитоза и гипергликемии, а также отклонения, характерные для преморбидной или сопутствующей соматической патологии: анемия (5), дисэлекторлитемия (3) и др. Повышение кардиоспецифичных маркеров было выявлено в 6 случаях, однако эти исследования проводятся только по показаниям – при подозрении на острый коронарный синдром (ОКС), а оно было далеко не во всех случаях. Специфичность этого метода диагностики снижает тот факт, что их повышение описано и при остром инсульте [5, 9, 12], а также при другой тяжелой соматической патологии. Интересно, что соответствующие ОНКК изменения у пациентов с повышением ферментов были только у двух пациентов по данным ЭКГ и у одного – по данным ЭхоКГ.
Признаки отека легких по результатам рентгенографии органов грудной клетки (ОГК) или КТ ОГК были выявлены в 7 случаях, гидроторакса – еще в 8. Таким образом, почти в трети случаев имели место признаки левожелудочковой недостаточности (условно острой в случае отека легких и хронической в случае гидроторакса).
Кардиологом не было осмотрено 16 пациентов, остальные больные были проконсультированы этим специалистом. Из осмотренных 34 пациентов кардиолог поставил диагноз ОКС или острый инфаркт миокарда только в 5 случаях (2 – на основании данных ЭКГ и ЭхоКГ, в 1 случае были повышены кардиоспецифические маркеры, в 1 – только по данным ЭКГ).
Танатогенез. Смерть пациентов наступала в среднем через 17,3 ч после поступления. 7 пациентов (14%) прожили менее 4 ч после госпитализации; это была наиболее тяжелая группа, которой практически сразу после поступления проводились реанимационные мероприятия, она же оказалась наименее обследованной. Стойкое снижение АД, требующее введения вазопрессоров, фиксировалось в 18 случаях (36%). В 14 случаях (28%) смерть произошла вследствие внезапной остановки сердечной деятельности. Этот вид смерти не совсем характерен для отека мозга с дислокацией в большое затылочное отверстие: в этом случае последовательно и в течение нескольких часов или суток происходит угнетение сознания, артериальная гипертензия в сочетании с брадикардией и нарушением функции внешнего дыхания (триада Кушинга [13]); только в терминальной стадии фиксируется артериальная гипотензия. Средний койко-день всех умерших пациентов с ОНМК в РСЦ составил в 2022 г. 8,5 койко-дней, что явно больше исследуемой группы.
Клинический диагноз. На основании имевшихся анамнестических, клинических, лабораторных и инструментальных данных формировался посмертный диагноз. В 22 случаях (44%) основной патологией был установлен диагноз ишемического инсульта, а диагноз инфаркта миокарда не был установлен. В 5 случаях неврологом был выставлен основным диагнозом только инфаркт миокарда, а инсульта – нет (в двух случаях на основании характерных изменений ЭКГ, в одном – ЭхоКГ, и только в одном случае после консультации кардиолога). В остальных 23 случаях был установлен комбинированный основной диагноз, где конкурирующими заболеваниями были указаны ишемический инсульт и острый инфаркт миокарда (из них только в 4 случаях этот диагноз был поставлен кардиологом). Основанием для такой формулировки чаще всего являлась клиника мозгового инсульта и характерный для инфаркта миокарда быстрый и внезапный летальный исход вследствие остановки сердца при отсутствии признаков злокачественного отека мозга.
Патологоанатомические исследования. Как следует из критериев выборки, во всех случаях при патологоанатомическом исследовании был установлен диагноз острого инфаркта миокарда, а макроскопических признаков инсульта при аутопсии и микроскопических признаков инфаркта мозга при гистологическом исследовании выявлено не было. В 4 случаях были обнаружены кистозно-глиозные изменения ткани мозга вследствие перенесенных инсультов, еще в 6 случаях – рубцовые изменения миокарда левого желудочка. Почти во всех случаях при гистологическом исследовании головного мозга наблюдались гистологические признаки его хронической ишемии.
ОПИСАНИЕ КЛИНИЧЕСКОГО ПРИМЕРА
Пациентка Т., 80 лет, поступила в РСЦ 24.04.2023 в экстренном порядке в тяжелом состоянии.
Данные архива медицинской информационной системы БАРС о заболеваниях, которыми ранее страдала пациентка и по поводу которых наблюдалась у специалистов по месту жительства: гипертоническая болезнь, ишемическая болезнь сердца (ИБС), стенокардия напряжения, функциональный класс (ФК) II, постоянная форма фибрилляции предсердий неуточненной давности, хроническая ишемия мозга, синдром Паркинсона, когнитивные расстройства, глаукома (грубое снижение остроты зрения, по поводу чего инвалид 2-й группы), хронический холецистит, полиостеоартроз суставов нижних конечностей с контрактурами. Из лекарственных средств пациента принимала ацетилсалициловую кислоту + магния оксид и метопролол. В течение нескольких месяцев примерно раз в неделю у пациентки бывали эпизоды с потерей сознания («трясло, закатывала глаза»), но по этому поводу она обследовалась, и причина установлена не была. По совокупности вышеперечисленной патологии за последние полгода пациентка не вставала, уход осуществляли родственники. В течение двух дней до обращения у нее нарастала общая слабость, стала заторможенной, не принимала пищу и воду. Вызов бригады скорой помощи в связи с нарушением сознания. На адресе уровень сознания – сопор, АД 70/40 мм рт.ст., SpO2 93%; были назначены инфузионная терапия, вазопрессоры, инсуффляция увлаженного кислорода. В неврологическом статусе были выявлены ротация головы и взора влево, отсутствие речи и движений в правых конечностях, в связи с чем пациентка была доставлена в РСЦ для лечения больных с ОНМК с подозрением на инсульт.
При поступлении АД равнялось 100/60 мм рт.ст., угнетение сознания сохранялось на уровне сопора, показатель по шкале Глазго составил 10 баллов. Продуктивному контакту пациентка была не доступна, отмечались ротация взора и головы влево, в правых конечностях – гипотония и отсутствие движений на болевые раздражители, симптом Бабинского справа. Показатель по шкале NIHSS – 32 балла.
Данные ЭКГ: ритм фибрилляции предсердий, тахисистолическая форма, средняя частота сокращений желудочков 92/мин, 2 желудочковые экстрасистолы. Нормальное положение электрической оси сердца. Снижение амплитуды зубцов комплекса QRS в стандартных и усиленных отведениях. Отдельные признаки нагрузки на правый желудочек. Локальное нарушение внутрижелудочковой проводимости. Признаки рубцовых изменений переднеперегородочной стенки, области верхушки левого желудочка. Неспецифическое нарушение реполяризации нижней стенки левого желудочка (зубец Т слабоотрицательный, на изолинии).
Данные КТ головного мозга: в теменной доле парасагиттально определяется участок пониженной плотности, с нечеткими контурами, размером 20×18 мм. Участки глиозных изменений в лобной доле слева, паравентрикулярно с двух сторон. Снижение плотности мозгового вещества головного мозга, перивентрикулярный лейкоареоз. Симметрично неравномерно расширены ликворные пространства: боковые и третий желудочки, конвекситальные борозды углублены. Заключение: признаки хронической ишемии мозга и участок ишемии в теменной доле слева (рис. 1).
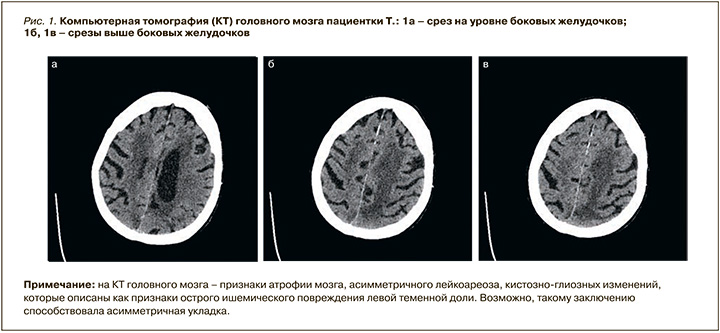
С диагнозом «ишемический инсульт в системе средней мозговой артерии» слева пациентка была госпитализирована в отделение анестезиологии и реанимации РСЦ, где ей была продолжена интенсивная базисная терапия.
ЭхоКГ была проведена через 3 ч после поступления: стенки аорты значительно склерозированы, створки клапанов уплотнены, кальцинированы. Умеренный аортальный стеноз со средним градиентом 26 мм рт. ст. Симметричная гипертрофия левого желудочка. Общая сократимость снижена, фракция выброса 51%. Выраженная дилатация полостей обоих предсердий. Повышение систолического давления в правом желудочке до 38 мм рт.ст. Участков гипокинезии не выявлено. Перикард в норме, жидкости нет.
Данные рентгенографии органов грудной клетки: легочный рисунок умеренно усилен в прикорневых отделах за счет сосудистого компонента, деформирован за счет диффузного пневмофиброза. Признаков инфильтрации легочной ткани не выявлено.
Данные лабораторных анализов: гипергликемия (10,3 ммоль/л); повышение уровня азотистых шлаков: креатинин – 323,6 мкмоль/л, мочевина – 41,6 ммоль/л; снижение общего белка до 53,7 г/л и альбуминов до 21,6 г/л; умеренная гипернатриемия (до 149,6 ммоль/л) и гиперкалиемия (до 6,0 ммоль/л); повышение аланинаминотрансферазы (АЛТ) – 45,9 Е/л, аспартатаминотрасферазы (АСТ) – 116,1 Е/л; свертывающая система (протромбиновый индекс, протромбиновое время, международное нормализованное отношение, активированное частичное тромбопластиновое время) в пределах нормы; показатели красной крови также в пределах нормы (эритроциты – 4,02×1012/л), лейкоцитоза нет (5,74×109/л). Повышение скорости оседания эритроцитов (СОЭ) до 20 мм/ч. Снижение уровня тромбоцитов до 34×109/л. Дисэлектролитемия и гипопротеинемия трактовались как проявления алиментарной недостаточности и гиповолемии, повышение СОЭ и гипергликемия – как закономерная катехоламиновая реакция, повышение азотистых шлаков – в рамках нефросклероза.
Пациентка была осмотрена кардиологом, сформулирован фоновый диагноз, признаков ОКС выявлено не было, в связи с чем не имелось и показаний для исследования кардиоспецифических маркеров.
Состояние пациентки сохранялось тяжелым: уровень сознания – сопор, дыхание самостоятельное, эпизодов десатурации не было, ЭКГ по монитору – фибрилляция предсердий, АД на уровне 90/60 мм рт.ст., несмотря на вазопрессорную поддержку и волемическую нагрузку.
Через 4,5 ч после поступления у пациентки произошла внезапная остановка сердечной деятельности, мероприятия сердечно-легочной реанимации, выполненные в полном объеме в течение 30 мин, не дали эффекта, биологическая смерть пациентки была зафиксирована через 5 ч после поступления.
Посмертный диагноз: ишемический инсульт в системе средней мозговой артерии слева от 24.04.2023, кардиоэмболический подтип, правосторонняя гемиплегия. Фоновое заболевание: ИБС, постинфарктный кардиосклероз неуточненной давности, постоянная форма фибрилляции предсердий, нормо-тахиформа, хроническая сердечная недостаточность 2А, гипертоническая болезнь III стадии, дислипидемия, атеросклероз сонных артерий, аорты, клапанов, нефроангиосклероз, хроническая болезнь почек (по KDIGO) С 5 (скорость клубочковой фильтрации по формуле CKD-EPI 11 мл/мин/1,73м2). Осложнение: отек головного мозга, вклинение в большое затылочное отверстие.
Реанимационные мероприятия: искусственная вентиляция легких (ИВЛ) мехом Амбу, непрямой массаж сердца, фармакоподдержка – адреналин 0,1% 6 мл.
Причина смерти: отек мозга.
Таким образом, учитывая наличие четкой очаговой неврологической симптоматики поражения левого полушария, данные КТ головного мозга, клинический диагноз ишемического инсульта не вызывал сомнения. Низкое АД в дебюте заболевания, при поступлении и за весь период наблюдения можно было объяснить гиповолемией, а быстрый летальный исход – массивным поражением мозговой ткани (описанный небольшой очаг мог быть только первым проявлением злокачественной полушарной ишемии).
На аутопсии: макроскопически признаков острого ишемического или геморрагического повреждения мозга не выявлено, миокард по передней стенке – с признаками ишемии (участок неравномерного кровенаполнения по передней стенке левого желудочка с мелкими линейными участками миокарда красновато-серого цвета), более характерными для острого периода инфаркта миокарда (рис. 2). Признаки атеросклероза всех коронарных артерий и окклюзии передней нисходящей артерии. На микропрепаратах – передней стеки левого желудочка видны мелкие и крупные участки некробиоза и некроза кардиомиоцитов с перифокальными диапедезными кровоизлияниями в строму и инфильтрацией единичными лейкоцитами; прилегающие сосуды паретически расширены и резко полнокровны, что характерно для инфаркта миокарда давностью 12–24 ч (рис. 3). Гистологическое исследование головного мозга: дистрофические изменения нейронов, утолщение, склероз и кальциноз стенок сосудов, паретическое расширение сосудов, периваскулярно – участки энефалолиза. Морфологических признаков инфаркта мозга не выявлено (рис. 4).

Патологоанатомический диагноз: острый трансмуральный инфаркт миокарда передней стенки левого желудочка; стенозирующий атеросклероз коронарных артерий тяжелой степени, 5–6-й тип бляшек, кровоизлияние в атеросклеротическую бляшку с окклюзией передней нисходящей артерии до 100%. Фоновое заболевание: гипертоническая болезнь (толщина стенки левого желудочка 1,9 см, гипертензивная ангиоэнцефалопатия). Осложнения основного заболевания: кардиогенный шок: универсальные расстройства микроциркуляции, диффузно-очаговый тубулонекроз, отек легких. Причина смерти: кардиогенный шок.
Клинико-патологоанатомический эпикриз: в данном случае имеет место расхождение основного клинического и патологоанатомического диагнозов. В качестве основного заболевания выступает острый инфаркт миокарда передней стенки левого желудочка вследствие стенозирующего атеросклероза коронарных артерий с окклюзией передней нисходящей артерии до 100%. Давность инфаркта миокарда 12–24 ч. Основное заболевание осложнилось кардиогенным шоком, что и учтено непосредственной причиной смерти. В качестве фоновой патологии выступает гипертоническая болезнь с гипертензивной ангиоэнцефалопатией. Морфологических данных в пользу инфаркта мозга не получено, мозговая симптоматика в данном случае обусловлена гипертензивной ангиоэнцефалопатией на фоне гемодинамических нарушений, связанных острым инфарктом миокарда. Основное заболевание и его смертельное осложнение в стационаре не были распознаны по причине краткости пребывания и тяжести состояния, категория расхождения 1.
ЗАКЛЮЧЕНИЕ
В результате проведенного исследования были выявлены следующие проблемы
1. Дифференциальный диагноз ОНМК и острого инфаркта миокарда вызывает значительные трудности, особенно у пациентов пожилого возраста, с коморбидной патологией.
2. Поступление пациентов в тяжелом состоянии с угнетением сознания, особенно при необходимости неотложного начала реанимационных мероприятий, значительно ограничивает время и набор диагностических тестов и манипуляций, а также не позволяет проводить наблюдение и необходимые исследования в динамике, что значительно снижает точность диагностики.
3. При наличии очаговой неврологической симптоматики и отсутствии убедительной клиники острого инфаркта миокарда клиницист склоняется, скорее, к диагнозу ОНМК, чем к другим диагнозам.
Наряду с этим были выявлены некоторые признаки, которые позволяют усомниться в диагнозе ОНМК и предположить диагноз церебральной формы острого инфаркта миокарда
1. Анамнез: пожилой возраст, перенесенные инсульты и инфаркты миокарда, дебют заболевания с угнетения сознания и снижения АД. Для инсульта дебют с угнетения сознания и артериальная гипотензия менее характерны.
2. Состояние при поступлении: угнетение сознания. Для ишемического инсульта угнетение сознания в первые часы заболевания менее характерно.
3. Обследование при поступлении: КТ головного мозга и повышение кардиоспецифических маркеров при любых их результатах не может служить решающим методом дифференциальной диагностики ишемического инсульта и острого инфаркта миокарда. ЭКГ также редко (всего в четверти случаев) выявляет специфические признаки ОНКК. Кроме того, они могут быть «завуалированы» другими изменениями. Более информативна ЭхоКГ, которая позволяет выявить локальные зоны гипокинезии миокарда в половине случаев.
4. В связи с этими трудностями консультация кардиолога чаще всего не позволяет заподозрить и верифицировать острый инфаркт миокарда.
5. В некоторых случаях на мысль об остром инфаркте миокарда могут натолкнуть признаки сердечной недостаточности – гидроторакс и отек легких.
6. Стойкое снижение АД и смерть в ближайшие часы после госпитализации вследствие внезапной остановки сердца наиболее часто служат основанием для установления острого инфаркта миокарда или как основного, или конкурирующего заболевания в рамках комбинированного диагноза.
Таким образом, строго специфических методов дифференциальной диагностики острого ишемического инсульта и церебральной формы острого инфаркта миокарда при кратковременном пребывании в стационаре пациентов в тяжелом состоянии не существует. Однако учет некоторых наиболее характерных анамнестических, инструментальных и клинических данных может позволить врачу уменьшить число диагностических ошибок в этой наиболее сложной части ургентной терапии.
Авторы выражают благодарность врачу патологоанатому ОГБУЗ «Патологоанатомическое бюро» Вадиму Геннадьевичу Милешину за неоценимую помощь в подготовке материала статьи.



