Важным показателем для выбора этапа и объёма реабилитационных мероприятий является интегральный показатель – шкалы реабилитационной маршрутизации (ШРМ), которая помогает экспертам в назначении вида реабилитации или в отказе в ней [3-5] (Приложение 1).
Ключевыми принципами медицинской реабилитации больных с COVID-19 являются: этапность (маршрутизация больных в рамках трехэтапной системы реабилитации), индивидуальность (ориентир на потребности, цели и желания конкретного больного), мультидисциплинарность (привлечение мультидисциплинарной команды), обоснованность, непрерывность, доступность [1,3].
Этапы медицинской реабилитации больных с COVID-19 [1]
Мероприятия медицинской реабилитации рекомендуется организовывать в медицинских организациях 4-х уровней с учетом особенностей оказания помощи пациентам с НКИ в 3 этапа в соответствии с Порядком организации медицинской реабилитации и Письмом Министерства здравоохранения РФ и Федерального фонда обязательного медицинского страхования от 12 декабря 2019 г. NN 11-7/И/2-11779, 17033/26-2/и "О методических рекомендациях по способам оплаты медицинской помощи за счет средств обязательного медицинского страхования».
- Первый этап реабилитации — ранняя реабилитация в отделении реанимации и интенсивной терапии (ОРИТ) и профильном (инфекционном) отделении с учетом соблюдения противоэпидемических требований. Мероприятия по медицинской реабилитации на 1-м этапе включают в себя оказание медицинской помощи по медицинской реабилитации в отделениях интенсивной терапии и инфекционных/терапевтических отделениях с оценкой по шкале реабилитационной маршрутизации (ШРМ) 5-6 баллов.
В ОРИТ специалисты по медицинской реабилитации в составе мультидисциплинарной реабилитационной бригады (врач ЛФК, инструктор-методист по ЛФК, врач физиотерапевт, по показаниям, медицинский психолог и логопед) работают в сотрудничестве с врачом реаниматологом, медицинской сестрой ОРИТ и должны быть обеспечены средствами индивидуальной защиты (СИЗ) в необходимом для работы объеме.
- Второй этап реабилитации — ранняя стационарная реабилитации в специализированном стационарном отделении медицинской реабилитации. Реабилитация организуется также с учетом соблюдения противоэпидемических требований (изоляции пациентов в палатах, полного или частичного отказа от групповых занятий и перехода на дистанционную форму общения с больным).
Второй этап медицинской реабилитации организовывается в отделениях медицинской реабилитации для пациентов с соматическими заболеваниями и состояниями в соответствии с Порядком организации медицинской реабилитации с оценкой по шкале реабилитационной маршрутизации (ШРМ) – 4–5 баллов;
Критерии для госпитализации в отделение медицинской реабилитации 2 этапа для пациентов с COVID-19:
- имеющие реабилитационный потенциал (пациент может быть безопасно отлучен от ИВЛ, стабилен по витальным показателям);
- ≥7 дней с момента постановки диагноза COVID-19;
- не менее 72 ч без лихорадки и жаропонижающих средств;
- стабильные показатели интервала RR по ЭКГ и SpO2;
- клинические и / или рентгенологические доказательства стабильности (по данным КТ или УЗИ легких);
- оценка по шкале реабилитационной маршрутизации (ШРМ)- 4 и 5 баллов;
- пациенты, с оценкой по ШРМ 3 и 2 балла, нуждающиеся в реабилитации и подходящие по критериям для 3-го этапа, но НЕ желающие или НЕ способные посещать поликлинику, в том числе по социальным и эпидемическим причинам;
- подписавшие информированное добровольное согласие на стационарное лечение.
Последующие этапы определяются состоянием пациента реализацией предшествующих целей и задач реабилитационного лечения. Длительность 2 этапа реабилитации должна составлять не менее 14 дней (2 недели). Пациент получивший медицинскую помощь по медицинской реабилитации на первом и/или втором этапах медицинской реабилитации и имеющий значения показателя ШРМ 3-2 балла - направляется на третий этап медицинской реабилитации
- Третий этап реабилитации — рекомендуется организовывать в отделениях медицинской реабилитации дневного стационара, амбулаторных отделениях медицинской реабилитации для пациентов с соматическими заболеваниями, а так же на дому с использованием телемедицинских технологий. Рекомендуется направлять пациентов на 3 этап реабилитации: имеющих реабилитационный потенциал, а так же с оценкой по шкале ШМР 3-2 балла. Для достижения наилучшего результата можно рекомендовать организовать выполнение комплекса упражнений пациентами на третьем этапе медицинской реабилитации 3 раза в неделю. Два раза в неделю под наблюдением специалистов, один раз - без наблюдения (в домашних условиях).
На 2 и з этапе реабилитации в комплекс следует включать как минимум 12 занятий под наблюдением специалистов. Рекомендованная длительность программ реабилитации составляет от 6 до 12 недель.
При наличии показаний и отсутствии значимых проявлений дыхательной недостаточности через 4–6 месяцев после перенесенного COVID-19 пациенты могут продолжить реабилитацию в условиях санаторно-курортных организаций. Предпочтение следует отдавать местным санаториям или находящимся в схожих климатических условиях.
Особенности организации реабилитации при COVID-19 [1,3]
Рекомендации, представленные в документе, в значительной степени базируются на материалах по реабилитации пациентов с COVID-19, опубликованных специалистами ВОЗ, анализе отечественных и зарубежных научных публикаций, клинических наблюдениях, нормативно-правовых документах Минздрава России и Роспотребнадзора. Несмотря на схожесть общих принципов реабилитации, при работе с пациентами, перенесшими НКИ, имеются особенности[1-7]:
- реабилитация сопровождает лечебный процесс, начинается рано (после завершения острейшей фазы COVID-19), но не позднее 48-72 ч от развития заболевания с учетом реабилитационного потенциала и противопоказаний к отдельным методам реабилитации;
- с целью безопасности и достижения лучшего эффекта от реабилитации необходимо идентифицировать потенциально значимые факторы тяжелой формы COVID-19, учитывать сопутствующие заболевания и коморбидность, снижающие реабилитационный потенциал пациента и возможность его вовлечение в программу реабилитации;
- широко использовать контролируемые дистанционные методы реабилитации (телереабилитацию), обучающие видеоролики, брошюры, дистанционное консультирование для предупреждения перекрестного инфицирования между больными и заражения медперсонала;
- соблюдать противоэпидемические требования, обеспечить медицинский персонал соответствующими средствами индивидуальной защиты (СИЗ), разделять реабилитационное оборудование для инфицированных и неинфицированных, обеспечивая его санитарную обработку; любая реабилитационная процедура - это высокий риск передачи инфекции (вирус SARS-CoV-2 отнесен ко 2-му уровню патогенности), при проведении процедур пациенты могут выделять аэрозоль с вирусом и оставаться контагиозными даже в период реконвалесценции [1,5,8].
Основными направлениями в реабилитации пациентов с COVID-19 являются:
- реабилитация респираторной функции;
- реабилитация мышечной дисфункции;
- реабилитация неврологических, психологических и когнитивных функций;
- нутритивная реабилитация;
- реабилитация коморбидных расстройств;
- медикаментозная реабилитация (профилактика поздних тромбозов и тромбоэмболий,ускорение разрешения консолидатов в легких, терапия бронхообтруктивного синдрома).
Методами контроля эффективности реабилитации являются [1,7-8]:
- оценка SpO2 в покое и при физической нагрузке;
- оценка переносимости физической нагрузки по шкале Борга;
- оценка выраженности одышки по шкале MRC (одышка) – для 2-го этапа;
- оценка силы мышц по шкале MRC (мышцы);
- оценка модифицированного индекса мобильности Ривермид (mRMI-ICU);
- оценка когнитивного статуса по шкале MMSE или MoCA;
- оценка интенсивности тревоги и депрессии по Госпитальной шкале тревоги и депрессии (HADS);
- оценка качества жизни по результатам Европейского опросника качества жизни EQ-5.
Учитывая, что работа по оказанию помощи пациентам с НКИ сопряжена с психо- эмоциальным и физическим перенапряжением медицинского персонала, рекомендовано организовать помощь по профилактическим оздоровительным мероприятиям, связанным с восстановлением работоспособности сотрудников, регулярно работающих в «Красной» зоне. С целью работы по восстановлению работоспособности сотрудников необходимо предусмотреть МДБ в составе: врач терапевт, врач реабилитолог (возможно врач специалист - ЛФК, ФЗТ или др.), специалист по ЛФК (инструктор или инструктор- методист), медицинской сестры по физиотерапии массажу, 2 психолога – специалистов по кризисной психологии (для индивидуальной работы). Следует предусмотреть возможность привлечения к работе специалистов МДБ так же и в дистанционном режиме в соответствии с действующим законодательством.
Понятие легочной реабилитации (ЛР)
Методы ЛР являются стандартным дополнением к медикаментозной терапии у людей с заболеваниями легких. При ЛР улучшается качество жизни пациентов, уменьшается одышка, сокращается число госпитализаций и их продолжительность (уровень доказательности А); улучшается толерантность к физической нагрузке и увеличивается выживаемость, наблюдается бронходилатационный эффект (уровень доказательности В) [1,7-11].
Легочная реабилитация пациентов, перенесших новую коронавирусную инфекцию COVID-19
Целью реабилитации у пациентов, перенесших новую коронавирусную инфекцию (COVID-19), является улучшение дыхательной функции, облегчение симптомов, снижение возможной тревожности и депрессии, снижение и минимизация вероятных осложнений, нормализация работы дыхательной и скелетной мускулатуры, стабилизация нутритивного статуса [1,3,6-11]
Для достижения существенного результата, длительность курсов легочной реабилитации составляет не менее 8 недель по 2-3 сеанса в день продолжительностью 15-20 мин. Более длительные программы дают лучшие результаты [1,3,5,21].
Формы проведения респираторной реабилитации:
- дистанционная форма с использованием телемедицинских технологий, девайсов, медиаформатов;
- амбулаторная форма (в условиях, не предусматривающих круглосуточного медицинского наблюдения и лечения);
- дневной стационар (в условиях, предусматривающих медицинское наблюдение и лечение в дневное время, но не требующих круглосуточного медицинского наблюдения и лечения);
- круглосуточный стационар (в условиях, обеспечивающих круглосуточное медицинское наблюдение и лечение).
Целостная система работы мультидисциплинарной бригады показана на рисунке 1 [29].
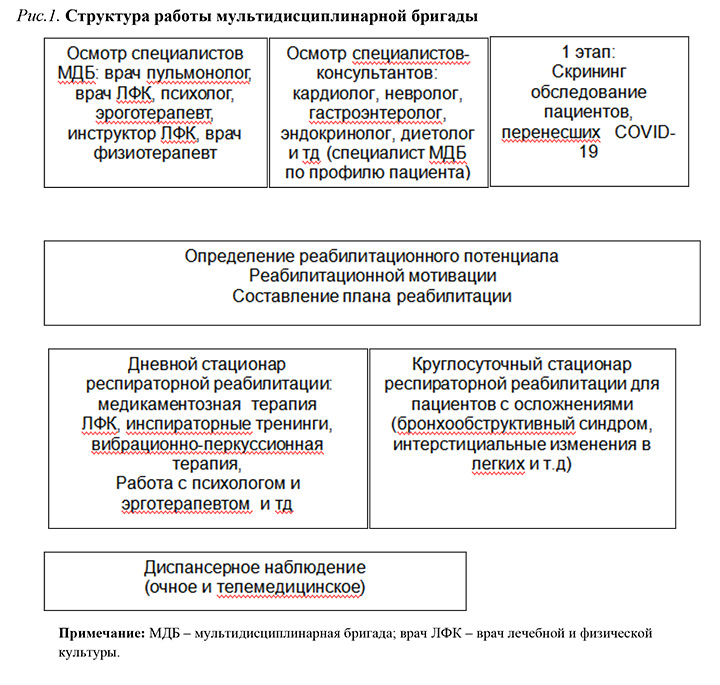
Работа с пациентом, перенесшим новую коронавирусную инфекцию начинается с этапа скрининг-обследования. Все пациенты проходят необходимый объем обследования с дальнейшим осмотром специалистов МДБ и врачей консультантов по профилю жалоб пациента. В дальнейшем определяется реабилитационный потенциал, мотивация пациента, составляется план и форма проведения восстановительных мероприятий с учетом индивидуальных особенностей [1,28,29]. Проводимые методы реабилитации и медикаментозной терапии составляют единый комплекс лечения для каждого отдельного пациента. Мероприятия по медицинской реабилитации проводятся в соответствии с Порядком организации медицинской реабилитации и Письмом Минздрава России №11- 7/И/2-20691, ФФОМС №00-10-26-2-04/11-51 от 30.12.2020.
Задачи респираторной реабилитации определяются как: уменьшение симптомов одышки, улучшение вентиляции и эластичности легочной ткани, улучшение бронхиального клиренса, восстановление нормального тонуса дыхательных мышц, силы и выносливости вспомогательной дыхательной мускулатуры и функции диафрагмы, восстановление правильного дыхательного паттерна [1].
В процессе медицинской реабилитации осуществляется ежедневный мониторинг жалоб и клинического состояния пациентов (особое внимание обращали на появление или усугубление одышки, кашля), измерение температуры тела, уровня сатурации кислорода в крови (методом пульсоксиметрии), частоты дыхательных движений (ЧДД), частоты сердечных сокращений (ЧСС), контролировали артериальное давление (АД). Все физические воздействия (лечебная гимнастика, физические тренировки, расширение режима двигательной активности) контролировались “стоп-сигналами” пациента [5].
Переносимость комплекса ЛФК и физической тренировки оценивается по модифицированной шкале Борга (10-балльная шкала, Borg CR10, Category Ratio scale) или оригинальной шкале Борга (20-бальная шкала, Borg RPE, Rating of Perceived Exertion), а выраженность одышки по шкале одышки Борга (по 10-балльной шкале) [1,3]. Важно оценивать патологию сердечно-сосудистой системы, систему кровообращения и нутритивный статус пациента.
Методы легочной реабилитации пациентов, перенесших COVID-19
Сроки восстановления больного, перенесшего COVID-19, напрямую зависят от проводимых мер респираторной реабилитации. Отказ от нее в ранние сроки может негативно повлиять на регресс последствий вирусного повреждения легочной ткани. Необходимо в кратчайшие сроки нормализовать паттерн дыхания, восстановить физическую активность и работу остальных органов и систем. Объем нагрузки строго зависит от функционального статуса пациента. Контроль переносимости нагрузки осуществляется постоянно по SpO2 и субъективным данным. При появлении СТОП- сигналов занятия прекращаются. Во время проведения процедуры должна быть возможность предоставления пациенту кислорода по требованию [1,5,7,13-14].
К основным методам легочной реабилитации относятся [1-7,29]:
-
Инспираторный тренинг: дыхательные упражнения. При коронавирусной инфекции, вследствие повреждения альвеол для улучшения вентиляционной способности легких необходимо повлиять на инспираторную мускулатуру, чтобы уменьшить перфузионные нарушения и снизить дыхательные объемы. Главное в тренировочных упражнениях влияние на все механизмы респираторной системы. Инспираторные мышцы являются активными в акте дыхания, они влияют на все аспекты легочной вентиляции.
Воздействую на паттерн дыхания (рисунок дыхания), мы можем уменьшить нагрузку на альвеолы, за счет снижения сопротивления в бронхах и улучшения вентиляции. Особенно это важно для пациентов, которым приходиться находиться в прон-позиции, при которой, страдает инспираторная мускулатура. Учитывая, что вирусная пневмония процесс острый, то восстановление физической активности не всегда необходимо, так как за время заболевания не всегда происходят повреждения скелетной мускулатуры. Однако, при тяжелом течении пневмонии или длительном нахождении в стационаре (более 10 дней) возникает необходимость в восстановлении силы скелетной мускулатуры. Пациенты стремительно теряют мышечную силу. Для этого используют тренировку скелетной мускулатуры. Для тренировки можно использовать гантели, утяжелители, степперы, велоэргометры и тредмил. Во время тренировки необходимо делать акцент на паттерн дыхания (рисунок дыхания), все упражнения надо делать медленно с длительным вдохом и выдохом с сопротивлением. - Форсированный экспираторный маневр с форсированным выдохом. Наиболее эффективная методика при необходимости мобилизации секрета легких. Данный вид упражнений применяется при наличии непродуктивного кашля, хронической гиперсекреции слизи, отсутствии кашлевого рефлекса.
- Метод активного циклического дыхания. Методика широко применяется при недостаточном отхождении мокроты для очистки дыхательных путей. Это наиболее адаптированный метод под индивидуальные особенности пациента. Данный вид терапии можно применять в любом положении тела, но позиция сидя наиболее эффективна.
- Постуральный дренаж. Данный метод применим для облегчения отхождения мокроты посредством принятия специально заданного положения тела, при котором зона поражения легких находится выше места бифуркации трахеи.
- Вибрационно-перкуссионная терапия. Учитывая патологический, воспалительный процесс, происходящий в результате развития вирусной пневмонии, отложение фибрина в альвеолах, использование инспираторного тренинга мало. Патологический процесс затрагивает большое количество структур в легких и для восстановления вентиляционной способности легких, уменьшения фиброзных изменений эффективно использовать высокочастотную осцилляцию грудной клетки совместно с компрессией. Данный метод сочетает в себе механическое воздействие высокочастотной вибрацией и компрессией на грудную клетку в результате которого, происходит восстановление дренажной функции легких, улучшения кровоснабжения в легких. Прибор, осуществляющий данной воздействие, не только влияет на улучшение отхождения мокроты за счет вибрационного воздействия, но и может влиять на функциональные и объемные показатели легких за счеткомпрессионного воздействия положительным давлением, улучшать вентиляцию в альвеолах.
Противопоказания к проведению вибрационно-перкуссионной терапии являются:
- наличие лихорадки (выше 38 °С);
- наличие булл в лёгких;
- кровотечения различной локализации;
- тромбоэмболия легочной артерии, развитие тромбозов;
- дыхательная недостаточность III ст.;
- сердечная недостаточность III ст., тяжёлые нарушения ритма сердца, имплантированный электрокардиостимулятор;
- наличие злокачественных новообразований любой локализации;
- тяжелые реакции на экзогенные и эндогенные факторы: шок, коллапс, аллергия, анафилаксия и др.; нарушение сознания; ОИМ; ОНМК;
- наличие кожных повреждений в зоне воздействия;
- наличие переломов позвоночника и ребер, травм шеи и головы;
- беременность и лактация.
- Электромиостимуляция. Нейромышечная электрическая стимуляция (НМЭС) скелетных мышц является альтернативным методом в реабилитации, влияющим на сокращение мышц, их работу без применения физических тренировок. НМЭС происходит согласно протоколу, в котором интенсивность (амплитуда), частота возбуждения, продолжительность и форма электрической волны выбраны так, чтобы достичь желаемого эффекта. Электрическая амплитуда (интенсивность) стимула определяет силу сокращения мышц. Сокращение мышц, вызванное электронной стимуляцией, не приводит к одышке, имеет минимальные требования к работе сердечно-сосудистой системы, обходит мотивационные и психологические аспекты, которые возникают при обычных физических тренировках. НМЭС используется, в первую очередь, у больных с выраженной слабостью периферических мышц; это прикованные к постели пациенты, как правило, получающие механическую вентиляцию, с выраженной дисфункцией периферических мышц. Для пациентов с тяжелой дыхательной недостаточностью, плохой переносимостью к физическим тренировкам из-за тяжести состояния, применение НМЭС улучшает силу верхних и нижних конечностей, уменьшает одышку при физической нагрузке, а уменьшая время на восстановление пациента.
Противопоказания к проведению электромиостимуляции:
- гнойные и другие инфекционные процессы в острой стадии;
- повышенная электровозбудимость мышц;
- патологические сокращения мышц;
- тромбоэмболия легочной артерии, развитие тромбозов;
- наличие кожных повреждений в зоне воздействия;
- наличие переломов позвоночника и ребер, травм шеи и головы;
- сердечная недостаточность III ст., тяжёлые нарушения ритма сердца, имплантированный электрокардиостимулятор;
- наличие злокачественных новообразований любой локализации;
- тяжелые реакции на экзогенные и эндогенные факторы: шок, коллапс, аллергия, анафилаксия и др.; нарушение сознания; ОИМ; ОНМК.
Реабилитация пациентов, перенесших новую коронавирусную инфекцию у больных с бронхообструктивным синдромом.
Все принципы легочной реабилитации для пациентов с хроническими респираторными заболеваниями сохраняются.
Для пациентов с обструктивными заболеваниями легких, особенности реабилитации на фоне переносимой новой коронавирусной инфекции нет, главное — продолжение той терапии, которую пациент проводил до коронавирусной инфекции или ее назначение. . Респираторная вирусная инфекция, в т.ч. коронавирусы и грипп считаются одними из основных факторов, способных вызывать обструкцию дыхательных путей. Они рассматривались в качестве, как триггеров обострения бронхиальной астмы (БА), так и этиологических факторов, формирующих БА у предрасположенных к ней людей. По данным эпидемиологических исследований, 75–80 % обострений БА связаны с острыми респираторными вирусными инфекциями. В 89 % случаев вирусная инфекция при БА вызывает ее обострение [18-19]. Основным патогенетическим механизмом обструктивного поражения ранее интактных нижних дыхательных путей (ДП) при ОРВИ у взрослых является развитие бронхиальной гиперреактивности на фоне повреждения эпителия, повышения чувствительности кашлевых рецепторов трахеобронхиального дерева [20-22]. Имеются результаты некоторых проспективных исследований о том, что бронхиолит, вызываемый вирусные инфекциями, является самым существенным фактором риска развития бронхиальной астмы у детей и взрослых. Риск максимален при отягощенном аллергологическом семейном анамнезе и генетической предрасположенности к БА [18,28]. Подчеркивается, что вирусы могут провоцировать формирование бронхиальной астмы и в отсутствие атопии [18-19]. Вирусиндуциорванный бронхообструктивный синдром (ВИ БОС) определяется, как универсальный синдром и возникает при наиболее распространенных хронических обструк-тивных заболеваниях (БА и ХОБЛ). Таким образом, синдром, являющийся типичным для таких заболеваний, как БА и ХОБЛ, требует стандартного подхода при назначении терапии в соответствии с клиническими рекомендациями [18-19]. С учетом имеющихся рекомендаций по терапии бронхообструктивного синдрома, пациентам с БОС показано лечение бронхолитическими препаратами и ингаляционными ГКС в качестве симптоматического и патогенетического [28-29]. При выборе терапии важно учитывать характеристики молекулы и средства доставки: респирабельная фракция, легочная депозиция, противовоспалительная активность и тд. Так же имеет значение приверженность пациента к терапии [20,29]. На фоне проводимой терапии имеет значение и оценка профиля безопасности назначаемого лечебного средства с учетом мультиситемности воздействия вируса на организм человека [29].
Физические упражнения (лечебная физкультура) отражены в приложениии.
В таблицах 1 и 2 представлены основные методы легочной реабилитации на различных этапах реабилитационной программы.
|
Таблица 1. Основные методы легочной реабилитации |
||
|
Методики |
Длительность выполнения |
Упражнения |
|
Инспираторный тренинг |
3-4 раза в день, продолжительностью от 5 до 20 минут. Упражнения выполняются в медленном темпе, постепенно увеличивают глубину вдоха и выдоха, не используются упражнения с напряженным вдохом и выдохом, стараются избегать задержки дыхания как на вдохе, так и на выдохе. Не рекомендуется форсировать увеличение объема движения и нагрузки. Не рекомендуется специальное стимулирование выделения мокроты. |
• На выдох с небольшим сопротивлением через сомкнутые губы; • С удлинённым вдохом; • Направленные на тренировку диафрагмы (диафрагмальное дыхание |
|
Форсированный экспираторный маневр с форсированным выдохом |
Дозировка нагрузки и интенсивность зависят от индивидуальных способностей человека, 2-4 раза в день. |
Глубокий вдох, резкий выдох с открытым ртом и с открытой голосовой щелью с использованием мышц живота и груди. Затем расслабленное «диафрагмальное дыхание» 1 мин. Цикл 2-4 раза, 2-4 раза в день |
|
Метод активного циклического дыхания |
Продолжительность 10-30 мин в день, 2-4 раза в день. |
Исходное положение: сидя или полусидя (положение Фаулера). Несколько минут расслабленного |
|
|
|
«диафрагмального дыхания». Глубокий вдох с длительным выдохом, 3-4 раза. Затем расслабленное «диафрагмальное дыхание» 1 мин. Глубокий вдох, резкий выдох с открытым ртом и с открытой голосовой щелью с использованием мышц живота и груди, 2-3 раза. Снова расслабленное «диафрагмальное дыхание», цикл 2-4 раза |
|
Постуральный дренаж |
Постуральный дренаж с откашливанием производится всегда натощак утром, при обилии мокроты – утром и вечером Начало дренажа следует проводить со стороны пораженного легкого, заканчивать со стороны здорового. Продолжительность с 5-10 минут в день с постепенным увеличением до 30-40 минут. |
Исходное положение: лежа на боку на наклонной плоскости или свесившись с кровати. Выполнение диафрагмального дыхания с чередованием откашливания мокроты, при котором возможно применение сдавления грудной клетки в момент кашля, поколачивание или вибромассаж. Смена левого и правого боков, до 40 мин |
|
Вибрационно- перкуссионная терапия |
Частота цикла задается с помощью ручной настройки прибора индивидуально для каждого пациента |
Данный метод сочетает в себе механическое воздействие высокочастотной вибрацией и компрессией, в результате чего происходит восстановление дренажной функции легких и улучшение кровоснабжения [25, 26]. |
|
Нейромышечная электрическая стимуляция (НМЭС) скелетных мышц |
Частота цикла задается с помощью ручной настройки прибора индивидуально для каждого пациента: форма импульсных токов прямоугольная или экспоненциальная, амплитуда - 20-40 В, длительность импульсов 0,5-10 мс, частота следования - 18-20 в минуту. Четыре электрода, соединённые эластической лентой, закрепляют на грудной клетке в области проекции диафрагмы. Передние электроды располагают между окологрудинной и передней подмышечной линиями и соединяют с катодом, а задние – по околопозвоночным линиям на уровне ThIX-XII и подключают к аноду. Продолжительность процедуры до 30 минут, по 10-12 упражнений за раз. |
Постепенное увеличение частоты и амплитуды волны, приводящие к возбуждению мышечных волокон |
|
Таблица 2. Методы легочной реабилитации на различных этапах реабилитационной программы [1,7] |
|||||
|
Этапы восстановления |
Тренировка дыхательных мышц |
Инспиратор ные тренажеры |
Электромиос тимуляция |
Вибрационно - компрессион ная терапия |
Тренировка верхней и нижней группы мышц |
|
Стационарный этап: реанимация |
Нет |
Нет |
Да |
Нет |
Ограниченно, да |
|
Инфекционное отделение |
Да |
Да |
Да |
Да |
Да |
|
Амбулаторный этап |
Да |
Да |
Да |
Да |
Да |
|
Санаторно-курортный этап |
Да |
Да |
Нет |
Нет |
Да |
Реабилитация пациентов, перенесших новую коронавирусную инфекцию у больных с бронхообструктивным синдромом [1-7]
Все принципы легочной реабилитации для пациентов с хроническими респираторными заболеваниями сохраняются.
Физиотерапия
При назначении физиотерапевтических процедур необходимо руководствоваться противопоказаниями к применяемому методу. Не рекомендуется использовать процедуры, стимулирующие отделение мокроты, разговорные клапаны и разрабатывать речь в острый период заболевания, до полного купирования острой инфекции и снижения риска ее передачи. Ингаляционное введение лекарственных средств назначается по показаниям при наличии коморбидной патологии. Применение физиотерапевтического оборудования возможно при условии строгого выполнения требований санитарной обработки после каждого пациента. Рекомендуется в комплекс реабилитационных мероприятий включать мобилизацию грудной клетки и ребер методами мануальной терапии, остеопатии, миофасциальный релиз дыхательных мышц, коррекцию мышечных триггеров дыхательной мускулатуры [1-3,7,25,28,29].
Физиотерапия на различных этапах реабилитации отражена в таблице 3 [1,3,5, 7,25,28,29].
|
Таблица 3. Физиотерапия на различных этапах реабилитации |
|||||
|
Метод |
Реабилитацион ные мероприятия |
Время проведения и кратность |
Комментарии |
Противопоказания |
Этап проведения |
|
Электростимуля ция диафрагмы и межреберных мышц |
Для пациентов с затрудненным отлучением от ИВЛ и сохраняющейся слабостью диафрагмы и межреберных мышц |
6-10 процедур по 10-15 минут ежедневно (использован ие электродов с силой тока до легкого визуального сокращения мышц) |
В рамках протокола электростимуляц ии диафрагмы и межреберных мышц |
- Повышенная возбудимость и патологическое сокращение мышц. - ТЭЛА. - Кожные повреждения в зоне воздействия. - Переломы позвоночника и ребер, травм шеи и головы. - Имплантированный ЭКС. -Нарушение сердечного ритма |
1 этап: ОРИТ, инфекционно е отделение многопрофил ьного стационара |
|
Лазеротерапия (красного, инфракрасного диапазона) |
Время воздействия 12- 30 минут № 8-10 ежедневно или два дня подряд с одним днем перерыва |
Время воздействия 12-30 минут № 8-10 ежедневно или два дня подряд с одним днем перерыва |
Назначается с учетом индивидуальной переносимости метода |
|
1 этап: ОРИТ, инфекционно е отделение многопрофил ьного стационара. 2 этап |
|
Низкочастотная электростатическ ая терапия |
Проводится локально на область грудной клетки с помощью перчаток или аппликаторов |
Ежедневно: начинают с 7- 12 минут, в дальнейшем 10-15 минут, 8-12 процедур |
|
- Кожные повреждения в зоне воздействия. - Электронные имплантируемые приборы. - Индивидуальная непереносимость электростатического поля. - Наличие в зоне воздействия металлических конструкций или предметов |
1 этап: инфекционно е отделение многопрофил ьного стационара |
|
Импульсные токи |
Локально на область грудной клетки, исключая область сердца |
Ежедневно 8- 10 процедур |
|
- Гнойный воспалительный процесс. - Нарушение сердечного ритма. |
2 этап |
|
|
|
|
|
- Кожные повреждения в зоне воздействия. - Электронные имплантируемые приборы. - Индивидуальная непереносимость электростатического поля. - Наличие в зоне воздействия металлических конструкций или предметов |
|
|
Локальная вибротерапия |
Локальное воздействие на область грудной клетки, контактно |
10-15 минут 4-5 процедур в неделю № 8-10 |
|
- Гнойный воспалительный процесс. - Нарушение сердечного ритма. - Кожные повреждения в зоне воздействия |
На всех этапах |
Нутритивная поддержка [1-3,7,8-10,25]
Задачи нутритивной поддержки: коррекция метаболических нарушений, обеспечение энергетических и пластических потребностей организма, поддержание активной белковой массы, функционирования органов и тканей, особенно иммунной системы, скелетных и дыхательных мышц, компенсация имеющихся потерь. Рекомендуется питание состоящие достаточного количества белка и калорий (если пациент склонен к кахексии), а при необходимости, использовать специальные белковые смеси. Если пациент склонен к ожирению, то рациональное питание, содержащее достаточное количества белка, низкокалорийное [10,25].
Оценка пищевого статуса в динамике включает оценку антропометрических показателей, анализ крови (количество лимфоцитов) и биохимические показатели крови (общий белок, альбумин, трансферрин, ферритин, креатинин, глюкоза, электролиты, общий билирубин, АЛТ, АСТ, ЩФ, ГГТП). Недостаточность питания и ее степень диагностируются при наличии одного и более критериев, представленных в таблице 4. Рекомендуется заполнять дневники питания для регистрации приемов пищи и жидкости в динамике.
Всем пациентам рекомендуется проводить оценку функции глотания.
|
Таблица 4. Оценка степени недостаточности питания |
|||
|
Степень недостаточности питания |
Легкая |
Средняя |
Тяжелая |
|
Альбумин, г/л |
30–35 |
25–30 |
<25 |
|
Трансферрин, г/л |
1,8–2,0 |
1,6–1,8 |
<1,6 |
|
Лимфоциты, клеток в 1 мл3 |
1500–1800 |
800–1500 |
<800 |
|
Индекс массы тела, кг/м2 |
17,5–19 1 |
5,5–17,5 |
<15,5 |
Согласно рекомендациям ESPEN (European Society for Clinical Nutrition and Metabolism, 2020) потребности в жирах и углеводах должны быть адаптированы к потребностям в энергии: для больных без дыхательной недостаточности соотношения энергии от жиров и углеводов — 30:70, для больных на ИВЛ — 50:50 [3,5, 25]. Назначаются стандартные или другие варианты диет, витаминно-минеральные комплексы – до 100 % от физиологической нормы, в соответствии с Приказом Минздрава РФ от 5 августа 2003 г. № 330, Приказом Минздрава России от 21.06.2013 № 395н «Об утверждении норм лечебного питания»*. Проводится адекватная гидратация с учетом сопутствующих заболеваний. При выраженной дыхательной недостаточности рекомендуется дробный прием пищи небольшими порциями под контролем уровня SpO2.
Схемы диетотерапии и нутритивной поддержки [1-5,7-10,25]
|
Таблица 5. Оценка индивидуальных потребностей в энергии и питательных веществах макро- и микронутриентах |
|
|
Потребность в энергии |
Методы оценки: 1. Непрямая калориметрия – «золотой» стандарт (при наличии возможности). 2. Расчетные формулы (Харриса–Бенедикта, Айретона – Джонса, Ли и др.). Уравнение Харриса – Бенедикта: ДРЭ = ОЭО х ФА x ФТ x ТФ x ДМТ, где ДРЭ – действительные расходы энергии (ккал/сут.); ОЭО – основной энергетический обмен; ФА – фактор активности; ФТ – фактор травмы; ТФ – температурный фактор; ДМТ – дефицит массы тела. ОЭО (мужчины) = 66 + (13,7 х МТ) + (5 x Р) – (6,8 x В) ОЭО (женщины) = 655 + (9,6 х МТ) + (1,8 x Р) – (4,5 x В) где МТ – масса тела (кг); Р – рост (см); В – возраст (лет). 3. Формула на основе массы тела Суточная потребность должна оцениваться из расчета 27–30 ккал фактической массы тела, адаптированная на индивидуальный пищевой статус, уровень физической активности и сопутствующие заболевания. |
|
Потребность в макронутриентах |
Потребность в белке. В случае отсутствия хронической почечной недостаточности потребление белка > 1 г/кг/сут. (до 1,5 г г/кг/сут). Должна быть адаптирована аналогично потребности в энергии, чтобы предотвратить потерю веса, снизить риск осложнений и оптимизировать выздоровление. Потребность в углеводах и жирах. Соотношение жиры: углеводы от 30:70 (пациенты без дыхательной недостаточности) до 50:50 (пациенты с дыхательной недостаточностью). |
|
Потребность в |
1. Рассмотреть необходимость назначения витаминов и минералов в |
|
микронутриентах |
адекватных дозах. Целевой уровень потребления – 100 % рекомендуемой суточной дозы, если нет особых указаний или повышенной потребности. 2. Рассмотреть необходимость назначения незаменимых аминокислот и аминокислот с разветвленной боковой цепью (БЦАА). 3. Обсудить применение пробиотиков, особенно при наличии кишечных расстройств. 4. Решить вопрос о необходимости назначения специализированных пищевых продуктов и/или искусственного питания в случае, если потребление питательных веществ и энергии составляет всего 50–60 % от рекомендуемого. |
Реабилитация мышечной дисфункции [1-3,5-7]
При тяжелом течении инфекции или длительном нахождении в стационаре (более 10 дней) возникает необходимость в восстановлении силы скелетной мускулатуры из-за стремительной ее потери. Для тренировки можно использовать гантели, утяжелители, степперы, велоэргометры и тредмилл. Во время занятий необходимо обращать внимание на паттерн дыхания, все упражнения делаются медленно с длительным вдохом и выдохом с сопротивлением (упражнения для верхней и нижней группы мышц).
К основным методам реабилитации мышечной дисфункции относятся:
- Физические упражнения.
- Инспираторный тренинг посредством использования тренажеров.
- Вибрационно-перкуссионная терапия.
- Электромиостимуляция.
Методы немедикаментозной терапии представлены в таблице 6 [5-7,25].
|
Таблица 6. Немедикаментозная терапия |
|||
|
Вид терапии |
Методики |
Противопоказания |
Особенности проведения |
|
Физические упражнения |
1. Упражнения для верхней группы мышц. 2. Упражнения для нижней группы мышц |
• Кровотечения различной локализации. • Дыхательная недостаточность III ст. • Сердечная недостаточность III ст. • Гнойные и другие инфекционные процессы в острой стадии. • Развитие тромбоза и тромбоэмболии. • Тяжелые реакции на экзогенные и эндогенные факторы: интоксикация, шок, коллапс, аллергия, |
|
|
|
|
анафилаксия и др. • Выраженный болевой синдром |
|
|
Инспираторный тренинг с использованием тренажеров |
Инспираторный тренинг с использованием тренажеров, создающих сопротивление с пороговой нагрузкой отрицательного давления на выдохе, способствующий откашливанию мокроты |
• Буллезная эмфизема. • Наличие в анамнезе пневмоторакса |
Тренировочный режим составляет по 5 мин 3 раза в день, при недостаточной физической подготовке – по 20 дыхательных движений 3-4 раза в день |
|
Вибрационно- перкуссионная терапия |
Механическое воздействие высокочастотной вибрации и компрессии на грудную клетку, в результате которого происходит восстановление дренажной функции легких |
• Лихорадка (выше 38 °С). • Буллы в легких. • Кровотечения различной локализации. • Тромбоэмболия легочной артерии, развитие тромбозов. • Дыхательная недостаточность III ст. • Сердечная недостаточность III ст., тяжелые нарушения ритма сердца, имплантированный электрокардиостимулятор. • Злокачественные новообразования любой локализации. • Тяжелые реакции на экзогенные и эндогенные факторы: шок, коллапс, аллергия, анафилаксия и др.; нарушение сознания; ОИМ; ОНМК. • Кожные повреждения в зоне воздействия. • Переломы позвоночника и ребер, травм шеи и головы. • Беременность и лактация |
Частота вибраций и давления создается с помощью настройки прибора: частота от 1-20 Гц, давление от 1-12 Бар. Время процедуры до 30 минут 2-4 раза в день. Во время процедуры перерыв каждые 5 минут для проведения форсированного экспираторного маневра с форсированным выдохом |
|
Электромиостимуляция |
Для пациентов с выраженной слабостью периферических |
• Гнойные и другие инфекционные процессы в острой стадии. • Повышенная |
Форма импульсных токов прямоугольная или экспоненциальная, |
|
|
мышц |
электровозбудимость мышц. • Патологические сокращения мышц. • Тромбоэмболия легочной артерии, развитие тромбозов. • Кожные повреждения в зоне воздействия. • Переломы позвоночника и ребер, травм шеи и головы. • Сердечная недостаточность III ст., тяжелые нарушения ритма сердца, имплантированный электрокардиостимулятор. • Злокачественные новообразования любой локализации. • Тяжелые реакции на экзогенные и эндогенные факторы: шок, коллапс, аллергия, анафилаксия и др.; нарушение сознания; ОИМ; ОНМК |
амплитуда - 20-40 В, длительность импульсов 0,5-10 мс, частота следования - 18-20 в минуту. Четыре электрода, соединённые эластической лентой, закрепляют на грудной клетке в области проекции диафрагмы. Передние электроды располагают между окологрудинной и передней подмышечной линиями и соединяют с катодом, а задние – по околопозвоночным линиям на уровне ThIX-XII и подключают к аноду. Продолжительность процедуры до 30 минут, по 10-12 упражнений за раз |
Психологическая и когнитивная реабилитация [1-4,25-27]
Факторы, провоцирующие состояния психоэмоционального напряжения, могут быть связаны с:
- неопределенностью методов лечения и меняющихся протоколов лечения;
- сложностью маршрутизации пациентов с COVID-19;
- сложностью усвоения ежедневно поступающей информации о новых правилах ограничения в период пандемии;
- высокой степенью риска заражения близких людей.
Для людей, находящихся в стрессовой ситуации в связи с COVID-19, могут быть следующие реакции:
- страх смерти;
- страх потери средств к существованию, неспособность работать во время изоляции, быть уволенным с работы;
- страх социального исключения, нахождения на карантине длительное время;
- растерянность и бессилие;
- тревога за своих близких;
- страх повторного заражения;
- интерпретация любых изменений в физическом самочувствии как ухудшение динамики картины болезни;
- чувство одиночества и сниженного настроения из-за изоляции.
Для исключения когнитивных последствий (особенно, у лиц, перенесших COVID-19 в тяжелой/очень тяжелой формах, получавших помощь в ОРИТ) до начала реабилитации рекомендуется оценить когнитивную функцию. С этой целью можно использовать Краткую шкалу оценки психического статуса — MMSE (Mini-Mental State Examination) и/или Монреальскую шкалу оценки когнитивных функций — МоСА (Montreal Cognitive Assessment). При выявлении когнитивных нарушений необходимо проводить специальные реабилитационные мероприятия (например, когнитивные тренинги, когнитивно-поведенческую терапию и т.п.).
Образовательные программы для пациентов
Важным и актуальным вопросом является образовательный аспект медицинской реабилитации. В условиях пандемии и изоляции наличие достоверной информации, определённых знаний и навыков является необходимым и важным фактором в лечении и восстановлении пациентов. Эффективность различных интернет-технологий признают большинство врачей [27]. В современных условиях одним из оптимальных решений является организация для пациентов онлайн-школ, которые позволяют одновременно обучить и донести необходимую информацию до большого числа людей. Обучение больного (и его родственников) играет ключевую роль в любой программе реабилитации и формировании позитивной мотивации. Важная задача образования – научить пациента самоконтролю состояния, выполняемых физических тренировок и самопомощи.
Появление новых возможностей, связанных с телемедицинским образованием населения, включая образовательные мероприятия для пациентов, их интеграция в системы оказания медицинской помощи открывают новые перспективы для улучшения клинической помощи, направленной на укрепление здоровья и профилактику заболеваний [1, 26-27].
Литература
- Временные методические рекомендации «Медицинская реабилитация при новой коронавирусной инфекции (COVID-19)». Версия 1 (май 2020 года).
- Richardson, S.; Hirsch, J.S.; Narasimhan, M.; Crawford, J.M.; McGinn, T.; Davidson, K.W. The Northwell COVID-19 Research Consortium. Presenting Characteristics, Comorbidities, and Outcomes among 5700 Patients Hospitalized with COVID-19 in the New York City Area. JAMA 2020, 323, 2052–2059. [CrossRef] [PubMed]
- COVID-19 Rapid Guideline: Managing the Long-Term Effects of COVID-19. Available online: https://www.nice.org.uk/ guidance/ng188 (accessed on 13 January 2021).
- Lapostolle, F.; Schneider, E.; Vianu, I.; Dollet, G.; Roche, B.; Berdah, J.; Michel, J.; Goix, L.; Chanzy, E.; Petrovic, T.; et al. Clinical features of 1487 COVID-19 patients with outpatient management in the Greater Paris: The COVID-call study. Intern. Emerg. Med. 2020, 15, 813– 817 [CrossRef].
- Lechien, J.R.; Chiesa-Estomba, C.M.; Place, S.; Van Laethem, Y.; Cabaraux, P.; Mat, Q.; Huet, K.; Plzak, J.; Horoi, M.; Hans, S.; et al. Clinical and epidemiological characteristics of 1420 European patients with mild-to-moderate coronavirus disease 2019. J. Intern. Med. 2020, 288, 335–344. [CrossRef]
- Milanese, M.; Corsico, A.G.; Bellofiore, S.; Carrozzi, L.; Di Marco, F.; Iovene, B.; Richeldi, ; Sanna, A.; Santus, P.; Schisano, M.; et al. Suggestions for lung function testing in the context of COVID-19. Respir. Med. 2021, 177, 106292. [CrossRef] [PubMed]
- Rimmer, A. Covid-19: Impact of long term symptoms will be profound, warns BMA. BMJ 2020, 370, m3218. [CrossRef] [PubMed]
- Argenziano, M.G.; Bruce, S.L.; Slater, C.L.; Tiao, J.R.; Baldwin, M.R.; Barr, R.G.; Chang, P.; Chau, K.H.; Choi, J.J.; Gavin, N.; et al. Characterization and clinical course of 1000 patients with coronavirus disease 2019 in New York: Retrospective case series. BMJ 2020, 369, m1996. [CrossRef] [PubMed]
- Guan, J.; Liang, W.H.; Zhao, Y.; Liang, H.-R.; Chen, Z.-S.; Li, Y.-M.; Liu, X.-Q.; Chen, R.-C.; Tang, C.-L.; Wang, T.; et al. Comorbidity and its impact on 1590 patients with COVID-19 in China: A nationwide analysis. Eur. Respir. J. 2020, 55, 2000547. [CrossRef] [PubMed]
- Zhang, J.; Wang, X.; Jia, X.; Li, J.; Hu, K.; Chen, G.; Wei, J.; Gong, Z.; Zhou, C.; Yu, H.; et Risk factors for disease severity, unimprovement, and mortality in COVID-19 patients in Wuhan, China. Clin. Microbiol. Infect. 2020, 26, 767–772. [CrossRef] [PubMed]
- Sudre, C.H.; Lee, K.; Ni Lochlainn, M.; Varsavsky, T.; Murray, B.; Graham, M.S.; Menni, ; Modat, M.; Bowyer, R.; Nguyen, L.; et al. Symptom clusters in Covid19: A potential clinical prediction tool from the COVID Symptom study app. medRxiv 2020. [CrossRef]
- Rubio-Rivas, M.; Corbella, X.; Mora-Luján, J.M.; Loureiro-Amigo, J.; Sampalo, A.L.; Bergua, C.Y.; Atiénzar, P.J.E.; García, L.F.D.; Ferrer, R.G.; Canteli, S.P.; et al. Predicting Clinical Outcome with Phenotypic Clusters in COVID-19 Pneumonia: An Analysis of 12,066 Hospitalized Patients from the Spanish Registry SEMI-COVID-19. J. Clin. Med. 2020, 9, 3488. [CrossRef] [PubMed]
- Greenhalgh, T.; Knight, M.; A’Court, C.; Buxton, M.; Husain, L. Management of post-acute covid-19 in primary care. BMJ 2020, 370, m3026. [CrossRef] [PubMed] 26. Ramos-Casals, M.; Brito-Zerón, P.; Mariette, X. Systemic and Organ-Specific Immune-Related Manifestations of COVID-19. Rev. Rheumatol. 2021, in press.
- Tenforde, M.W.; Kim, S.S.; Lindsell, C.J.; Billig Rose, E.; Shapiro, N.I.; Files, D.C.; Gibbs, W.; Erickson, H.L.; Steingrub, J.S.; Smithline, H.A.; et al. Symptom Duration and Risk Factors for Delayed Return to Usual Health Among Outpatients with COVID-19 in a Multistate Health Care Systems Network-United States, March-June 2020. MMWR Morb. Mortal. Wkly Rep. 2020, 69, 993–998. [CrossRef] [PubMed]
- Daher, A.; Balfanz, P.; Cornelissen, C.; Müller, A.; Bergs, I.; Marx, N.; Müller-Wieland, D.; Hartmann, B.; Dreher, M.; Müller, T. Follow up of patients with severe coronavirus disease 2019 (COVID-19): Pulmonary and extrapulmonary disease sequelae. Med. 2020, 174, 106197. [CrossRef] [PubMed]
- Rosales-Castillo, A.; Ríos, C.G.D.L.; García, J.D.M. Persistent symptoms after acute COVID-19 infection: Importance of follow-up. Medicina clinica. Med. Clínica 2021, 35–36. [CrossRef] [PubMed]
- Cheung D.S., Ehlenbach S.J., Kitchens R.T. et al. Cutting edge: CD49d+ neutrophils induce FcepsilonRI expression on lung dendritic cells in a mouse model of postviral asthma. J. 2010; 185 (9): 4983-4987. https://doi.org/10.4049/jimmunol.1002456.
- Oliver B.G., Robinson P., Peters M., Black J. Viral infections and asthma: an inflammatoryinterface? Respir. J. 2014; 44 (6):1666-1681 https://doi.org/10.1183/09031936.00047714.
- Carfì, A.; Bernabei, R.; Landi, F. Persistent Symptoms in Patients after Acute COVID-19. JAMA [CrossRef] [PubMed]
- Mandal, ; Barnett, J.; E Brill, S.; Brown, J.S.; Denneny, E.K.; Hare, S.S.; Heightman, M.; E Hillman, T.; Jacob, J.; Jarvis, H.C.; et al. ‘Long-COVID’: A cross-sectional study of persisting symptoms, biomarker and imaging abnormalities following hospitalisation for COVID-19. Thorax 2021, 76, 396–398. [CrossRef]
- Zhao, Y.-M.; Shang, Y.-M.; Song, W.-B.; Li, Q.-Q.; Xie, H.; Xu, Q.-F.; Jia, J.-L.; Li, L.-M.; Mao, H.-L.; Zhou, X.-M.; et al. Follow-up study of the pulmonary function and related physiological characteristics of COVID-19 survivors three months after recovery. EClinicalMedicine 2020, 25, 100463. [CrossRef]
- Garrigues, E.; Janvier, P.; Kherabi, Y.; Le Bot, A.; Hamon, A.; Gouze, H.; Doucet, L.; Berkani, S.; Oliosi, E.; Mallart, E.; et al. Post-discharge persistent symptoms and health-related quality of life after hospitalization for COVID-19. J. 2020, 81, e4–e6. [CrossRef]
- Townsend, L.; Dyer, A.H.; Jones, K.; Dunne, J.; Mooney, A.; Gaffney, F.; O’Connor, L.; Leavy, D.; O’Brien, K.; Dowds, J.; et al. Persistent fatigue following SARS-CoV-2 infection is common and independent of severity of initial infection. PLoS ONE 2020, 15, e0240784. [CrossRef]
- Carvalho-Schneider, C.; Laurent, E.; Lemaignen, A.; Beaufils, E.; Bourbao-Tournois, C.; Laribi, S.; Flament, T.; Ferreira-Maldent, N.; Bruyère, F.; Stefi, K.; et al. Follow-up of adults with non-critical COVID-19 two months after symptoms’ onset. Clin. Microbiol. Infect. 2020. [CrossRef] [PubMed]
- Lambert, N.J.; Survivor Corps. COVID-19 “Long Hauler” Symptoms Survey Report. Indiana University School of Medicine, Indianapolis, USA. Available online: https://dig.abclocal.go.com/wls/documents/2020/072720-wls-covid-symptom-study-doc. pdf (accessed on 25 January 2021).
- Cho, R.H.W.; To, Z.W.H.; Yeung, Z.W.; Tso, E.Y.K.; Fung, K.S.C.; Chau, S.K.Y.; Leung, Y.L.; Hui, T.S.C.; Tsang, S.W.C.; Kung, K.N.; et al. COVID-19 Viral Load in the Severity of and Recovery from Olfactory and Gustatory Dysfunction. Laryngoscope 2020, 130, 2680–2685. [CrossRef] [PubMed].
- Теплякова О.В., Лещенко И.В., Эсаулова Н.А., Сарапулова А.В. Ключевые аспекты организации телемедицинских школ для пациентов как технологии современного здравоохранения. Здравоохранение Российской Федерации. 2022; 66(2): 107-113.
- Лещенко И.В., Эсаулова Н.А. Постковидный бронхообструктивный синдром в практике врача-терапевта и пульмонолога: широкомасштабное исследование. Пульмонология. 2022; 32 (4): 539–547. DOI: 18093/0869-0189-2022-32-4-539-547.
- Лещенко И. В., Эсаулова Н.А. Основные аспекты респираторной реабилитации последствий новой коронавирусной инфекции. Практическая пульмонология. 2022; 1:10- 16. DOI: 10.24412/2409-6636-2022-12831.



